“侯氏制碱法”是我国著名制碱专家侯德榜经过多年研究做出的杰出贡献,其最大的优点是降低了成本,大大提高了NaCl的利用率。
(1)“侯氏制碱法”的原理可表示为: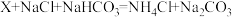 ,X的化学式是
,X的化学式是_______ ,X中一种元素的质量分数为__________ (精确到0.1%)。
(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成 的质量是多少?
的质量是多少?
(1)“侯氏制碱法”的原理可表示为:
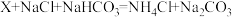 ,X的化学式是
,X的化学式是(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成
 的质量是多少?
的质量是多少?
2023·山西·中考真题 查看更多[10]
2023年山西省中考化学真题(已下线)第16讲 化学方程式的书写与应用-【暑假自学课】2023年新九年级化学暑假精品课(沪教版)(已下线)专题23 化学计算(第02期)-学易金卷:2023年中考化学真题分项汇编(全国通用)(已下线)2023年山西省中考化学真题变式题(非选择题15~17)(已下线)第五单元 课题3 利用化学方程式的简单计算-【巅峰课堂】2023-2024学年九年级化学上册同步精品讲+练(人教版)(已下线)4.4 化学方程式(第2课时)(同步练习)-九年级化学上册同步精品课堂(科粤版2012)专题六 综合计算题分类训练(已下线)第十二单元 化学与生活A卷-2023-2024学年九年级化学下册同步测试优选卷(人教版)(已下线)2024年中考风向标-山西-计算题(已下线)押广东省卷非选择题第21题 有关物质推断及化学方程式的综合计算-备战2024年中考化学临考题号押题(广东省卷专用)
更新时间:2023/06/22 23:33:44
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】我国科学家发明了一种将甲烷中的氢转化为氢气的工艺,其反应原理可表示为 。
。
(1) 中氢元素的质量分数为
中氢元素的质量分数为________ ,X的化学式是________ 。
(2)当甲烷的转化率为80%时,理论上1.0t甲烷反应生成氢气的质量是多少?
 。
。(1)
 中氢元素的质量分数为
中氢元素的质量分数为(2)当甲烷的转化率为80%时,理论上1.0t甲烷反应生成氢气的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】过氧化氢是一种强氧化剂,其水溶液(俗称双氧水)适用于医用伤口消毒及环境消毒和食品消毒。
(1)过氧化氢能与高锰酸钾溶液反应,反应的化学方程式为: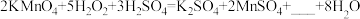 。空白处应填
。空白处应填______ 。该反应中高锰酸钾不是催化剂,理由是______ 。
(2)过氧化氢在常温下会分解成水和氧气,但分解速率极慢,过氧化氢分解过程中氧元素的化合价会______ (填“升高”、“降低”或“既有升高又有降低”)。为加快其反应速率,可以加入二氧化锰。实验室用34g双氧水和1g二氧化锰制取氧气,实验的相关数据如图。请回答:______ g。
②34g双氧水中溶质质量分数为______ 。
(1)过氧化氢能与高锰酸钾溶液反应,反应的化学方程式为:
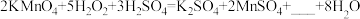 。空白处应填
。空白处应填(2)过氧化氢在常温下会分解成水和氧气,但分解速率极慢,过氧化氢分解过程中氧元素的化合价会

②34g双氧水中溶质质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)四种铁矿石的主要成分是:①Fe2O3 ②Fe3O4 ③FeCO3 ④FeS2,这四种化合物含铁的质量分数由高到低的顺序是_____________ (填序号)。
(2)近年来,有不法分子利用假金欺骗群众,假金外观像黄金,但它是一种铜与金属M的合金。某同学想确定金属M,已知金属M为+2价,他取用3.5 g这种假金样品,把15.0g含HCl14.6%的稀盐酸分3次加入,充分反应后剩余固体质量见表:
①计算该假金样品中铜的质量分数;
②通过计算确定M是何种金属。
(2)近年来,有不法分子利用假金欺骗群众,假金外观像黄金,但它是一种铜与金属M的合金。某同学想确定金属M,已知金属M为+2价,他取用3.5 g这种假金样品,把15.0g含HCl14.6%的稀盐酸分3次加入,充分反应后剩余固体质量见表:
| 第1次 | 第2次 | 第3次 | |
| 稀盐酸的用量/g | 5.0 | 5.0 | 5.0 |
| 剩余固体质量/g | 2.85 | 2.2 | 2.0 |
①计算该假金样品中铜的质量分数;
②通过计算确定M是何种金属。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】某反应 2Na2O2+2H2O =4NaOH+O2↑,现将 10 克 Na2O2 样品,放入 100 克水中,完全反应后剩余质量为 108.4 克。请计算
(1)求生成氧气的质量
(2)样品中 Na2O2 的纯度(质量分数)。
(1)求生成氧气的质量
(2)样品中 Na2O2 的纯度(质量分数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】化肥对提高农作物的产量具有重要作用。硝酸铵(NH4NO3)是一种常见的氮肥。计算
(1)硝酸铵由___________种元素组成(填数字);
(2)硝酸铵中氮元素和氧元素的质量比为___________(填最简比);
(3)硝酸铵中氮元素的质量分数___________;
(4)若有160g硝酸铵,则含有氮元素的质量为___________g。
(1)硝酸铵由___________种元素组成(填数字);
(2)硝酸铵中氮元素和氧元素的质量比为___________(填最简比);
(3)硝酸铵中氮元素的质量分数___________;
(4)若有160g硝酸铵,则含有氮元素的质量为___________g。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】核糖是人类生命不可缺少的一种有机物,它的化学式是C5H10O5。计算:
(1)核糖中碳、氢、氧三种元素的质量比。
(2)核糖中碳元素的质量分数。
(1)核糖中碳、氢、氧三种元素的质量比。
(2)核糖中碳元素的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】 是研发超级电容器电极的重要材料,工业上制备
是研发超级电容器电极的重要材料,工业上制备 的流程如图1所示。已知碱式碳酸钴可以看作
的流程如图1所示。已知碱式碳酸钴可以看作 和
和 结合而成的化合物。
结合而成的化合物。 之外,还生成了
之外,还生成了______ 、______ 。(均填化学式)
(2)过程2:化学方程式为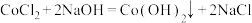 ,用
,用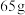 溶质质量分数为20%的
溶质质量分数为20%的 溶液,理论上可以制备
溶液,理论上可以制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)
(3)过程3:将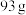 的
的 在空气中加热,固体质量随温度变化关系如图2所示。
在空气中加热,固体质量随温度变化关系如图2所示。
①1000 ℃时,剩余固体中钴元素的质量为______ 。
②290 ℃时,剩余固体 为一种氧化物,其化学式为
为一种氧化物,其化学式为______ 。
 是研发超级电容器电极的重要材料,工业上制备
是研发超级电容器电极的重要材料,工业上制备 的流程如图1所示。已知碱式碳酸钴可以看作
的流程如图1所示。已知碱式碳酸钴可以看作 和
和 结合而成的化合物。
结合而成的化合物。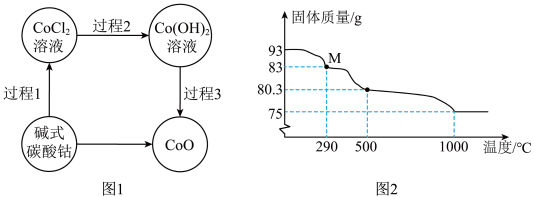
 之外,还生成了
之外,还生成了(2)过程2:化学方程式为
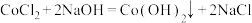 ,用
,用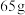 溶质质量分数为20%的
溶质质量分数为20%的 溶液,理论上可以制备
溶液,理论上可以制备 的质量是多少?(写出计算过程)
的质量是多少?(写出计算过程)(3)过程3:将
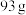 的
的 在空气中加热,固体质量随温度变化关系如图2所示。
在空气中加热,固体质量随温度变化关系如图2所示。①1000 ℃时,剩余固体中钴元素的质量为
②290 ℃时,剩余固体
 为一种氧化物,其化学式为
为一种氧化物,其化学式为
您最近一年使用:0次

 2CaSO4+2X。
2CaSO4+2X。

