铝是地壳中含量最高的金属,作为材料新秀,薄如蝉認的铝箔应用广泛。
(1)铝材能加工成薄如蝉翼的铝箔,是因为铝具有很好的____ 性,铝箔用作空调热交换器翅片是利用了铝的____ 性。
(2)铝具有很好的抗腐蚀性能,是因为铝在空气中发生反应生成的保护膜阻止其进一步被氧化,保护膜的成分是____ 。
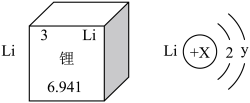
(3)在新能源汽车的动力锂电池中,铝管作正极集流体,承载电极活性物质LiFePO4。元素周期表中,Li的相关信息如图所示,则x、y的值分别为___ 。__ 。
(4)铝、钛等金属与稀土形成的特种合金常用于航空、航天领域。关于稀土资源,下列说法正确的是____(填字母)。
(1)铝材能加工成薄如蝉翼的铝箔,是因为铝具有很好的
(2)铝具有很好的抗腐蚀性能,是因为铝在空气中发生反应生成的保护膜阻止其进一步被氧化,保护膜的成分是
(3)在新能源汽车的动力锂电池中,铝管作正极集流体,承载电极活性物质LiFePO4。元素周期表中,Li的相关信息如图所示,则x、y的值分别为
(4)铝、钛等金属与稀土形成的特种合金常用于航空、航天领域。关于稀土资源,下列说法正确的是____(填字母)。
| A.稀土的开采与环境、生态问题无关 |
| B.稀土广泛应用于新材料领域 |
| C.我国的稀土储量目前居世界第一位 |
更新时间:2024/05/09 21:57:52
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】按要求用化学用语填空:
(1)标出H2S中硫元素的化合价______ ;
(2)锶(Sr)原子38号元素第五周期第二主族,失去2个电子后形成离子,离子符号为______ ;
(3)天然气的主要成分______ ;
(4)工业上制取二氧化碳的原理是:CaCO3 CaO+CO2↑,正确读法:
CaO+CO2↑,正确读法:______ 。
(1)标出H2S中硫元素的化合价
(2)锶(Sr)原子38号元素第五周期第二主族,失去2个电子后形成离子,离子符号为
(3)天然气的主要成分
(4)工业上制取二氧化碳的原理是:CaCO3
 CaO+CO2↑,正确读法:
CaO+CO2↑,正确读法:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】芯片是电脑、手机等的核心部件,碳基芯片采用石墨烯碳纳米管工艺,性能比硅基芯片更好,我国已突破半导体碳纳米管关键材料的技术瓶颈,请回答:
(1)石墨烯碳纳米管具有良好的________ 性。
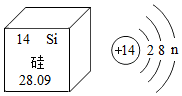
(2)如图是硅元素在元素周期表中的部分信息及原子结构示意图,图中n=_____ ,硅的相对原子质量是______ ,硅元素位于元素周期表中的第____ 周期。
(3)化学反应中元素化合价升高的物质是还原剂,元素化合价降低的物质是氧化剂。在制硅反应 中还原剂是
中还原剂是______ ,发生还原反应的物质是______ 。

(1)石墨烯碳纳米管具有良好的
(2)如图是硅元素在元素周期表中的部分信息及原子结构示意图,图中n=
(3)化学反应中元素化合价升高的物质是还原剂,元素化合价降低的物质是氧化剂。在制硅反应
 中还原剂是
中还原剂是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】南昌大学研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖,请回答下列问题:
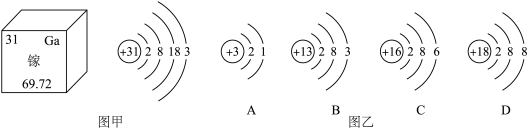
(1)图甲是镓在元素周期表中的信息以及原子结构示意图。镓的相对原子质量为:_____ ;如图乙原子结构示意图所对应的元素与镓元素的化学性质相似的是_____ (填序号);
(2)图乙中属于金属元素的原子结构示意图是_____ (填序号,下同)。达到稳定结构的粒子是_____ 。B和C两种元素的原子构成的化合物的化学式为_____ 。
(3)传统制备氮化镓的化学原理是: ,其中X的化学式为
,其中X的化学式为_____ 。

(1)图甲是镓在元素周期表中的信息以及原子结构示意图。镓的相对原子质量为:
(2)图乙中属于金属元素的原子结构示意图是
(3)传统制备氮化镓的化学原理是:
 ,其中X的化学式为
,其中X的化学式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】人类文明发展与金属材料的使用有着密切联系。
(1)生活中使用的铝制品具有很好的抗腐蚀性,其原因是___________ (用化学方程式表示)。
(2)金可制成金箔,拉成金丝,说明金具有良好的___________ 性。
(3)现有甲、乙、丙三种金属,把甲和乙分别放入稀硫酸中,甲溶解并产生气泡,乙无明显现象;把乙和丙分别放入硝酸银溶液中,乙表面有银白色固体析出,而丙无明显变化,则这三种金属的活动性由强到弱的顺序为___________ 。
(4)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如图:
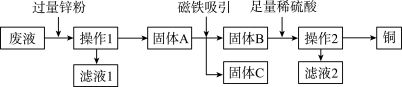
①废液中加入过量锌粉时,与CuSO4发生的化学反应方程式为___________ ,该反应的基本反应类型为___________ 反应。
②操作1的名称为___________ ,用到的玻璃仪器有烧杯,玻璃棒和___________ 。
③除水外,滤液1和滤液2还含有相同的物质,该物质是___________ (填化学式)。
(1)生活中使用的铝制品具有很好的抗腐蚀性,其原因是
(2)金可制成金箔,拉成金丝,说明金具有良好的
(3)现有甲、乙、丙三种金属,把甲和乙分别放入稀硫酸中,甲溶解并产生气泡,乙无明显现象;把乙和丙分别放入硝酸银溶液中,乙表面有银白色固体析出,而丙无明显变化,则这三种金属的活动性由强到弱的顺序为
(4)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如图:

①废液中加入过量锌粉时,与CuSO4发生的化学反应方程式为
②操作1的名称为
③除水外,滤液1和滤液2还含有相同的物质,该物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】金属在生产和生活中有广泛的应用。
(1)下列金属制品中,利用金属导电性的是______ (填字母序号)

(2)收藏家收藏清朝末年的铝制品至今仍保存完好,原因是在常温下,其表面形成了一层致密的氧化铝薄膜: (用化学方程式表示)_________
(3)铁制品在沙漠地区不易锈蚀的原因是_________
(4)人们在焊接铁制品时先要用稀盐酸处理一下表面的铁锈,其原理是(用化学方程式表示):_______ 。
(1)下列金属制品中,利用金属导电性的是

(2)收藏家收藏清朝末年的铝制品至今仍保存完好,原因是在常温下,其表面形成了一层致密的氧化铝薄膜: (用化学方程式表示)
(3)铁制品在沙漠地区不易锈蚀的原因是
(4)人们在焊接铁制品时先要用稀盐酸处理一下表面的铁锈,其原理是(用化学方程式表示):
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】金属汞俗名水银,滴到铝板上,能溶解铝,形成液态合金(铝汞齐),使表层的铝原子浓度变低,从而使铝与氧气反应时无法形成致密氧化膜,内部的铝原子不停地与氧气反应(出现“长毛”现象如图甲),变化过程的微观模型如图乙。

(1)铝汞齐属于_____ (填“单质”、“化合物”和“混合物”)。
(2)写出图乙中铝被氧化的化学方程式_____ 。
(3)中国民航局规定,工业水银温度计不允许携带(温馨提示:飞机的机体主要是铝制的)。原因是水银一旦泄露,除了汞蒸气本身剧毒外,更主要是因为_____ 。
(4)汞在空气蒸发,从微观的角度看是因为汞原子的_____ 。
(5)若在表面清洁的铝板上滴上HgCl2溶液。也会出现“长毛”现象。该现象说明铝的金属活泼性比汞_____ (填“强”或“弱”),涉及反应方程式为:_____ 。

(1)铝汞齐属于
(2)写出图乙中铝被氧化的化学方程式
(3)中国民航局规定,工业水银温度计不允许携带(温馨提示:飞机的机体主要是铝制的)。原因是水银一旦泄露,除了汞蒸气本身剧毒外,更主要是因为
(4)汞在空气蒸发,从微观的角度看是因为汞原子的
(5)若在表面清洁的铝板上滴上HgCl2溶液。也会出现“长毛”现象。该现象说明铝的金属活泼性比汞
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】人类生活生产离不开金属,不仅因为其物理性能优良,还与化学性质密切相关。

(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高。钛和钛合金是新型的结构材料,主要用于航天和航海工业。上述描述中属于钛化学性质的是_______ 。
(2)某小组用如图甲所示装置对铁生锈的条件进行探究。4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是_______ 。
(3)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学反应方程式_______ 。
(4)在金属活动顺序表中,金属位置越靠前,越容易失去电子。Ca、Mg、K三种金属失去电子能力由强到弱的顺序是K、Ca、Mg,如图乙是三种原子的结构示意图,据此推测金属失去电子能力的强弱除与最外层电子数有关外,还可能与_______ 有关。

(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高。钛和钛合金是新型的结构材料,主要用于航天和航海工业。上述描述中属于钛化学性质的是
(2)某小组用如图甲所示装置对铁生锈的条件进行探究。4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是
(3)工业生产常用10%的稀盐酸来除铁锈,写出除锈的化学反应方程式
(4)在金属活动顺序表中,金属位置越靠前,越容易失去电子。Ca、Mg、K三种金属失去电子能力由强到弱的顺序是K、Ca、Mg,如图乙是三种原子的结构示意图,据此推测金属失去电子能力的强弱除与最外层电子数有关外,还可能与
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】请你根据对金属和金属材料的认识,回答下列问题:
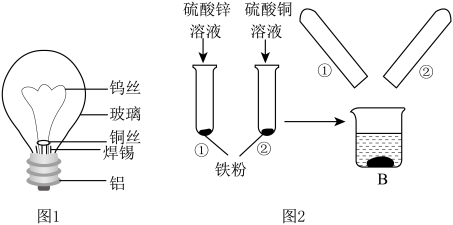
(1)如图1标出的是组成灯泡的物质,所标出的物质中不属于金属材料的是___________ 。
(2)钢铁厂以赤铁矿为原料冶炼生铁的原理为___________ (用化学方程式表示)。很多大型场馆的建设使用了大量的钢材,主要是因为钢比纯铁具有___________ 的优良性能。
(3)某化学兴趣小组的同学在探究锌、铜、铁三种金属的有关性质时,进行了如图2所示实验:
①在A实验中发生反应的化学方程式为___________ 。
②将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤,同学们向滤渣中滴加稀盐酸,结果没有气泡产生,那么滤液中一定含有的溶质是___________ 。

(1)如图1标出的是组成灯泡的物质,所标出的物质中不属于金属材料的是
(2)钢铁厂以赤铁矿为原料冶炼生铁的原理为
(3)某化学兴趣小组的同学在探究锌、铜、铁三种金属的有关性质时,进行了如图2所示实验:
①在A实验中发生反应的化学方程式为
②将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,一段时间后过滤,同学们向滤渣中滴加稀盐酸,结果没有气泡产生,那么滤液中一定含有的溶质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属在生产和生活中应用广泛。请回答下列问题:
(1)5G基站供电系统多用铜作导线,是因为铜具有良好的___________ 性和延展性;
(2)铝制品耐腐蚀的原因是表面生成了一层致密的___________薄膜(填化学式);
(3)木炭与氧化铜反应化学方程式为2CuO+C 2Cu+CO2↑,该反应中发生了还原反应的物质是
2Cu+CO2↑,该反应中发生了还原反应的物质是___________ 。
(4)除去FeCl2溶液中的CuCl2,可以加入适量的___________,充分反应后过滤。
(1)5G基站供电系统多用铜作导线,是因为铜具有良好的
(2)铝制品耐腐蚀的原因是表面生成了一层致密的___________薄膜(填化学式);
(3)木炭与氧化铜反应化学方程式为2CuO+C
 2Cu+CO2↑,该反应中发生了还原反应的物质是
2Cu+CO2↑,该反应中发生了还原反应的物质是(4)除去FeCl2溶液中的CuCl2,可以加入适量的___________,充分反应后过滤。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】钢铁是重要的金属材料,在生产、生活中有广泛的用途。
(1)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的水及_______________ 共同作用的结果。
(2)为了防止钢铁锈蚀,人们常采用在其表面涂刷植物油或镀上其他金属等覆盖保护膜的方法。这些方法都能防止锈蚀的共同原理是__________________
(3)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出第②步反应的化学方程式:________
(4)目前世界上已有50%以上的废铁得到回收利用,其目的是____________ 填“合理开采矿物”或“节约金属资源”)。
(1)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的水及
(2)为了防止钢铁锈蚀,人们常采用在其表面涂刷植物油或镀上其他金属等覆盖保护膜的方法。这些方法都能防止锈蚀的共同原理是
(3)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出第②步反应的化学方程式:
(4)目前世界上已有50%以上的废铁得到回收利用,其目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属和化石燃料等都是宝贵的自然资源,需要珍惜。请回答下列问题:
(1)防止金属生锈是保护金属资源的有效途径,除此之外,还有哪些_____ 。(写1条即可)
(2)燃料充分燃烧可节约化石燃料。请指出哪些因素能使燃料充分燃烧_____ (写1条即可)。
(3)最清洁的燃料是_____ ,写出1条它作为燃料的优点_____ 。
(4)如图是探究燃烧条件的实验,回答下列问题:
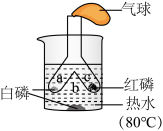
①燃烧现象发生在_____ (填“a”、“b”或“c”)处,现象是_____ ,反应的化学方程式为_____ 。
②对比a、b两处,得出结论是_____ 。
③小气球的作用是_____ 。
(1)防止金属生锈是保护金属资源的有效途径,除此之外,还有哪些
(2)燃料充分燃烧可节约化石燃料。请指出哪些因素能使燃料充分燃烧
(3)最清洁的燃料是
(4)如图是探究燃烧条件的实验,回答下列问题:

①燃烧现象发生在
②对比a、b两处,得出结论是
③小气球的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氢氧燃料电池汽车是一种真正意义上的“零排放,无污染”载运工具,是利用原电池原理,将氢气与氧气通过反应形成电流,并为电动机供电驱动车辆行驶。请回答问题:

(1)一些汽车车体采用铝合金制成,是因为铝合金与铁合金相比,其在物理性质上具有的优点是______ (填字母)。
A 抗腐蚀性好
B 密度小
C 硬度大
(2)氢氧燃料电池汽车在行驶过程中的能量转化过程是________ (用“→”表示)。
(3)工业上制取铝通常采用电解法,氧化铝在通电和催化剂条件下分解生成两种单质,请写出电解氧化铝的化学方程式________ 。
(4)氢氧燃料电池汽车相对于燃油汽车,不仅节约了________ 还减少了汽车尾气的排放。
(5)电动汽车中的导线材质都是铜。某兴趣小组同学想从铁和硫酸铜反应后的废液中回收金属铜,设计了如下方案,
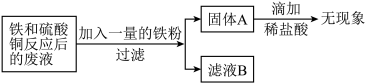
试回答:
①固体A中一定不含________ (填化学式)
②滤液B中一定含有的溶质________ (填化学式)

(1)一些汽车车体采用铝合金制成,是因为铝合金与铁合金相比,其在物理性质上具有的优点是
A 抗腐蚀性好
B 密度小
C 硬度大
(2)氢氧燃料电池汽车在行驶过程中的能量转化过程是
(3)工业上制取铝通常采用电解法,氧化铝在通电和催化剂条件下分解生成两种单质,请写出电解氧化铝的化学方程式
(4)氢氧燃料电池汽车相对于燃油汽车,不仅节约了
(5)电动汽车中的导线材质都是铜。某兴趣小组同学想从铁和硫酸铜反应后的废液中回收金属铜,设计了如下方案,

试回答:
①固体A中一定不含
②滤液B中一定含有的溶质
您最近一年使用:0次



