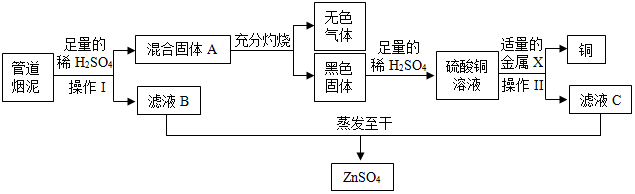
下图是实验室模拟“侯氏制碱法”生产纯碱的工艺流程图。________ (填实验名称),通过步骤Ⅲ所得滤渣的成分是________ 。
(2)步骤Ⅰ和步骤Ⅱ的顺序不能颠倒,否则___________ 。
(3)用实际参加反应的离子符号表示化学反应的式子叫做离子方程式,复分解反应的实质就是反应物的离子间结合生成了沉淀、气体或水。请用离子方程式表示步骤Ⅱ的反应___________ 。
(4)步骤Ⅳ与步骤Ⅴ之间还有一步重要操作,其名称是___________ ;步骤Ⅴ若先通入CO2再通入NH3,造成的后果是___________ 。

(2)步骤Ⅰ和步骤Ⅱ的顺序不能颠倒,否则
(3)用实际参加反应的离子符号表示化学反应的式子叫做离子方程式,复分解反应的实质就是反应物的离子间结合生成了沉淀、气体或水。请用离子方程式表示步骤Ⅱ的反应
(4)步骤Ⅳ与步骤Ⅴ之间还有一步重要操作,其名称是
2024·江苏宿迁·二模 查看更多[2]
更新时间:2024/05/10 11:00:38
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学工业上人们常说的“三酸两碱”就是指硫酸、盐酸、硝酸和烧碱、纯碱。一个国家酸碱盐的产量在一定程度上反映了化学工业的发展水平。酸碱盐在工业农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展。下面是我国化学科技领域中引起世界关注的两个领军人物。请分析图文信息,解答11-14题的相关问题。
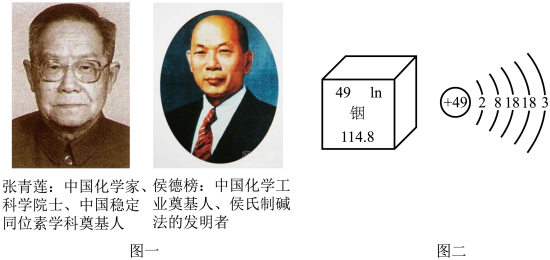

(1)中国科学院院士张青莲教授为相对原子质量的测定做出了卓越贡献。他主持测定了铟、铱、锑、铈、锌等几种元素的相对原子质量的新值,被国际原子量委员会采用为国际新标准。由图文信息可知,铟的相对原子质量为______ ;铟在化学反应中易______ 电子(填“得”或“失”)。
(2)侯德榜-我国杰出化学家,“侯氏制碱法”的创始人,中国重化学工业的开拓者、近代化学工业的奠基人之一,是世界制碱业的权威。1926年他生产的“红三角”牌纯碱,获得美国费城万国博览会金质奖章。下面是“侯氏制碱法”的部分反应原理:
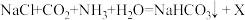 ;
;
①其中物质X的化学式为______ 。在农业上,物质X常用作一种化肥是______ 。
②侯氏制碱法中的“碱”指的物质是______ 。
(3)了解常见酸碱盐的性质可以更好的在日常生活中广泛应用。
①HCl、H2SO4溶液有许多共同性质的原因是溶液中都有______ (填离子符号)。试举一例说明:______ 。
②常用含氢氧化镁的胃药治疗胃酸过多,有关反应的化学方程式是______ 。
(4)烧碱是一种亚要的化工原料,使用时要特别小心,因为______ 。列举烧碱在日常生活中的一种用途:______ 。


(1)中国科学院院士张青莲教授为相对原子质量的测定做出了卓越贡献。他主持测定了铟、铱、锑、铈、锌等几种元素的相对原子质量的新值,被国际原子量委员会采用为国际新标准。由图文信息可知,铟的相对原子质量为
(2)侯德榜-我国杰出化学家,“侯氏制碱法”的创始人,中国重化学工业的开拓者、近代化学工业的奠基人之一,是世界制碱业的权威。1926年他生产的“红三角”牌纯碱,获得美国费城万国博览会金质奖章。下面是“侯氏制碱法”的部分反应原理:
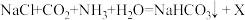 ;
;
①其中物质X的化学式为
②侯氏制碱法中的“碱”指的物质是
(3)了解常见酸碱盐的性质可以更好的在日常生活中广泛应用。
①HCl、H2SO4溶液有许多共同性质的原因是溶液中都有
②常用含氢氧化镁的胃药治疗胃酸过多,有关反应的化学方程式是
(4)烧碱是一种亚要的化工原料,使用时要特别小心,因为
您最近一年使用:0次
【推荐2】下图是 NH4Cl、NaCl、NaHCO3(碳酸氢钠)三种物质的溶解度曲线,回答下列问题:

(1)60℃时,NH4Cl 的溶解度是______ g/100g 水;
(2)能将接近饱和的 NaHCO3溶液转化为饱和溶液的一种方法是______ ;
(3)60℃的饱和 NH4Cl 溶液中含有少量的 NaCl,提纯 NH4Cl 的方法是______ ;
(4)20℃时,将 NH3、CO2通入饱和 NaCl 溶液中,可生成 NaHCO3和 NH4Cl,反应的化学方程式为: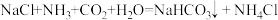
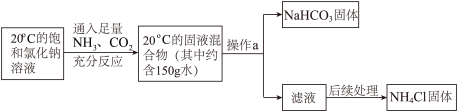
Ⅰ、以上过程中,操作 a 是______ ,产物中可作氮肥的是______ ;
Ⅱ、经测定,以上反应中,参加反应的 NaCl 的物质的量为 1mol,20℃的固液混合物中,NaHCO3固体首先析出,而 NH4Cl 固体不析出,请结合相关数据分析说明______ 。

(1)60℃时,NH4Cl 的溶解度是
(2)能将接近饱和的 NaHCO3溶液转化为饱和溶液的一种方法是
(3)60℃的饱和 NH4Cl 溶液中含有少量的 NaCl,提纯 NH4Cl 的方法是
(4)20℃时,将 NH3、CO2通入饱和 NaCl 溶液中,可生成 NaHCO3和 NH4Cl,反应的化学方程式为:
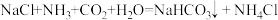

Ⅰ、以上过程中,操作 a 是
Ⅱ、经测定,以上反应中,参加反应的 NaCl 的物质的量为 1mol,20℃的固液混合物中,NaHCO3固体首先析出,而 NH4Cl 固体不析出,请结合相关数据分析说明
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E均为初中化学中不同类别的物质,它们的变化关系如图所示,其中A是胃液中含有的酸,C是红棕色的固体,D是侯德榜制碱法生产的物质,E溶液的pH大于7.“﹣”表示相连的两种物质能发生反应,“→”表示物质转化的方向,则:

(1)自然界中为了防止B→C的发生可以采取的措施是_____ .
(2)A和C反应的化学方程式是_____ .
(3)A与D反应的化学方程式是_____ .

(1)自然界中为了防止B→C的发生可以采取的措施是
(2)A和C反应的化学方程式是
(3)A与D反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐1】用如图实验方法分离NaCl和CaCl2两种固体的混合物A,根据操作流程完成下列问题:
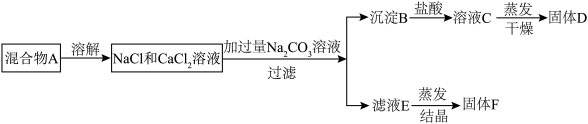
(1)B物质是_______ ;
(2)过滤操作中玻璃棒的作用是______ ;
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善_____________ ;
(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量_______ 和______ 的质量求解。

(1)B物质是
(2)过滤操作中玻璃棒的作用是
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善
(4)若用原操作方法,要测出混合物A中NaCl和CaCl2的质量比,不称量D,可通过称量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】醋酸钙是常用的补钙剂。每年我国鸡蛋有上千万吨的产量,会产生数以万吨的废弃蛋壳(主要成分为CaCO3),如图是以废弃蛋壳作为原料回收膜并制备醋酸钙的一种工艺流程。
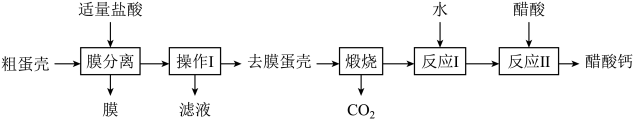
(1)鸡蛋壳中CaCO3中碳元素的化合价为__________________ 。
(2)操作I的名称是___________________________ ,玻璃棒的作用__________________ 。
(3)写出煅烧蛋壳的化学方程式__________________ 。此反应的基本类型是__________________ 。
(4)膜分离时,盐酸要加入适量,不能过量的主要原因是__________________ 。

(1)鸡蛋壳中CaCO3中碳元素的化合价为
(2)操作I的名称是
(3)写出煅烧蛋壳的化学方程式
(4)膜分离时,盐酸要加入适量,不能过量的主要原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水氯化钙(CaCl2·2H2O)的流程如图。原料石灰石中含有杂质主要是MgCO3、MgSO4和A12O3。

(1)过滤操作用到的玻璃仪器有烧杯、玻璃棒、___________ 。
(2)石灰石粉溶解时,Al2O3发生反应的化学方程式为___________ 。
(3)加入BaCl2除去的杂质离子是___________ ;图中滤渣的成分有___________ 。
(4)检验“滤液”酸碱性,如果显碱性,还需加入适量的___________ (填化学式)提高产品纯度。

(1)过滤操作用到的玻璃仪器有烧杯、玻璃棒、
(2)石灰石粉溶解时,Al2O3发生反应的化学方程式为
(3)加入BaCl2除去的杂质离子是
(4)检验“滤液”酸碱性,如果显碱性,还需加入适量的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】毒重石的主要成分BaCO3(还含有CaCO3、MgO、Fe2O3),实验室利用毒重石制备BaCl2·2H2O的流程如下:
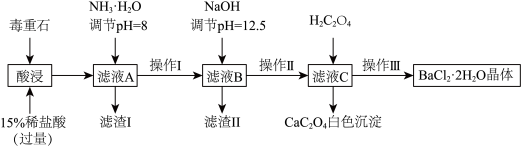
已知:①草酸H2C2O4能与BaCl2反应生成BaC2O4白色沉淀;
②碳酸钡和稀盐酸反应与碳酸钙相似。
(1)毒重石用盐酸浸取前需充分研磨,目的是___________ ;写出碳酸钡和稀盐酸反应的方程式___________ 。
(2)实验室配置370g15%的盐酸,需要37%的盐酸溶液质量为___________ g,除量筒、胶头滴管外,还需使用下列仪器中的___________ 。
a、烧杯 b、漏斗 c、玻璃棒 d、蒸发皿
(3)经过酸浸之后,滤液A中含有的阳离子有___________ 种。
(4)操作Ⅲ主要包括蒸发浓缩、___________ 、过滤、95%乙醇洗涤、干燥。
(5)加入NH3·H2O调节pH=8,是为了除去滤液A中H+和___________ ,滤渣Ⅱ中含有Mg(OH)2和___________ ,加入H2C2O4时应避免过量,原因是___________ 。

已知:①草酸H2C2O4能与BaCl2反应生成BaC2O4白色沉淀;
②碳酸钡和稀盐酸反应与碳酸钙相似。
(1)毒重石用盐酸浸取前需充分研磨,目的是
(2)实验室配置370g15%的盐酸,需要37%的盐酸溶液质量为
a、烧杯 b、漏斗 c、玻璃棒 d、蒸发皿
(3)经过酸浸之后,滤液A中含有的阳离子有
(4)操作Ⅲ主要包括蒸发浓缩、
| 项目 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
(5)加入NH3·H2O调节pH=8,是为了除去滤液A中H+和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】在除杂质的操作中,为了将杂质完全去除,通常需加入过量的除杂试剂。为了除去NaCl样品中混有少量的Na2SO4和MgCl2,某校化学课外活动小组设计了提纯NaCl的流程图:
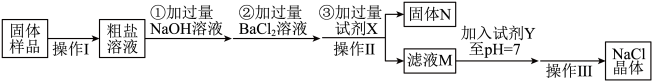
(1)加入过量的氢氧化钠可除去的阳离子是___________ (写离子符号),写出①的化学方程式:___________ 。
(2)试剂X的化学式为___________ ,溶液M中所含有的全部阴离子有___________ (写离子符号)。
(3)试剂Y的名称是___________ ,它的作用是___________ 。
(4)操作Ⅱ的名称是___________ ,操作Ⅰ、Ⅱ、Ⅲ都要用到的同一种玻璃仪器是___________ 。

(1)加入过量的氢氧化钠可除去的阳离子是
(2)试剂X的化学式为
(3)试剂Y的名称是
(4)操作Ⅱ的名称是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】粗盐中通常含有泥沙等难溶性杂质及 、
、 和
和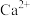 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的___________ 溶液→过量的氢氧化钠溶液→过量的___________ 溶液→适量稀盐酸。加入稀盐酸之前应进行的操作是___________ 。
 、
、 和
和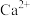 等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的
等可溶性杂质离子。为除去上述可溶性杂质离子,将粗盐溶解,并依次加入下列试剂:过量的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
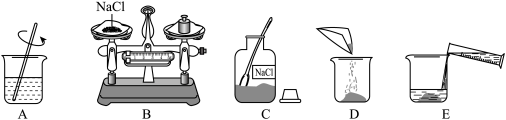
【推荐2】配制一定浓度氯化钠溶液的过程如下图所示。__________ 。
(2)正确的实验步骤为__________ 。
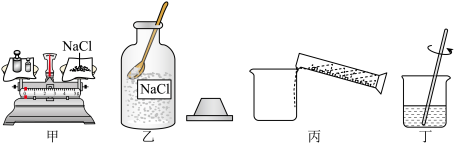
(2)正确的实验步骤为
您最近一年使用:0次