题型:填空与简答-填空题
难度:0.65
引用次数:7
题号:22937956
现配制100g质量分数为10%的NaOH 溶液用于制作叶脉书签,需称量氢氧化钠固体的质量为_______ g;若配制的 NaOH 溶液的质量分数小于10%,可能的原因是_______ (任写一点)。
2024·河南·模拟预测 查看更多[1]
(已下线)2024年河南省中原名校中考联盟测评(三)化学试卷
更新时间:2024/05/27 10:37:44
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】溶液在化学学习和科学研究中具有广泛的用途。
(1)碘酒是家庭常备药,碘酒中的溶剂是_______ 。
(2)农业上常用溶质质量分数为16%的氯化钠溶液进行选种,实验室用氯化钠固体配制100g溶质质量分数为16%的氯化钠溶液。
①所配溶液中溶质与溶剂的质量比为_______ (填最简整数比)。
②若称量氯化钠时所用砝码生锈,则所配溶液的溶质质量分数会_______ (填“偏大”、“偏小”或“不变”)。
(3)对上述配制好的溶液进行恒温蒸发操作,实验记录如下:

①乙中的溶液为_______ (填“饱和”“不饱和”或“不确定”)溶液。
②甲、乙、丙、丁四种溶液中,溶质质量分数由大到小的顺序为_______ 。
(1)碘酒是家庭常备药,碘酒中的溶剂是
(2)农业上常用溶质质量分数为16%的氯化钠溶液进行选种,实验室用氯化钠固体配制100g溶质质量分数为16%的氯化钠溶液。
①所配溶液中溶质与溶剂的质量比为
②若称量氯化钠时所用砝码生锈,则所配溶液的溶质质量分数会
(3)对上述配制好的溶液进行恒温蒸发操作,实验记录如下:

①乙中的溶液为
②甲、乙、丙、丁四种溶液中,溶质质量分数由大到小的顺序为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】请用所化学知识解释下列现象或原理。
(1)“南水北调”工程,跨越半个多世纪的调水梦于2014年12月12日正式通水,该工程的开通重组了中国水资源格局,方便了1.1亿人。有些村庄打深井取用地下水,食用前可用_______ 区分地下水是软水还是硬水,常用_______ 的方法来降低水的硬度,以防止结石病的发生。
(2)“釜底抽薪”涉及的化学原理是_____________________________________ 。
(3)有NaOH溶液,NaCl溶液,稀硫酸三种物质,用一种试剂就能将他们鉴别出来,该试剂是______ 。
(4)在检查胃部疾病之前,医生常让病人饮用一种含有硫酸钡的白色牛奶状液体,形象的称作“钡餐”,“钡餐”中的主要物质是硫酸钡,而不能用碳酸钡,其原因可用化学方程式解释为_________________ 。
(5)合成材料的应用和发展,大大方便了人类的生活,但是废弃塑料带来的“白色污染”也很严重,为了解决这个问题,我们可以采取的措施有_________ (答一条即可)。
(6)在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作:

①上图操作中有错误的是_______ (填序号)。
②改正错误后,表示正确的操作顺序是_______ (填序号)。
(1)“南水北调”工程,跨越半个多世纪的调水梦于2014年12月12日正式通水,该工程的开通重组了中国水资源格局,方便了1.1亿人。有些村庄打深井取用地下水,食用前可用
(2)“釜底抽薪”涉及的化学原理是
(3)有NaOH溶液,NaCl溶液,稀硫酸三种物质,用一种试剂就能将他们鉴别出来,该试剂是
(4)在检查胃部疾病之前,医生常让病人饮用一种含有硫酸钡的白色牛奶状液体,形象的称作“钡餐”,“钡餐”中的主要物质是硫酸钡,而不能用碳酸钡,其原因可用化学方程式解释为
(5)合成材料的应用和发展,大大方便了人类的生活,但是废弃塑料带来的“白色污染”也很严重,为了解决这个问题,我们可以采取的措施有
(6)在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作:

①上图操作中有错误的是
②改正错误后,表示正确的操作顺序是
| A.⑤②①③④ | B.⑤①②③④ | C.⑤③②④① | D.⑤③①④② |
您最近一年使用:0次
【推荐1】溶液在工农业生产和科学研究中具有广泛的用途。请依据题意回答下列问题。
【资料】NaCl和Na2CO3两种物质在不同温度时的溶解度
(1)生活在盐湖、碱湖附近的人们传承下来的劳动经验是“夏天晒盐,冬天捞碱”。
①Na2CO3俗称苏打或_______ 。分析表中数据,冬天更适合“捞碱”的原因是:____________________ ,有利于Na2CO3的析出。
②夏天“晒盐”,当有大量盐析出后,所得溶液为该温度下NaCl的_______ (填“饱和”或“不饱和”)溶液。
(2)在实验室进行粗盐提纯时,使用蒸发皿蒸发过程中,有时会出现液滴飞溅现象_____________ (答一点即可)。
(3)在实验室用质量分数为6%的NaCl溶液(密度约为1.04g/m3)配制80g质量分数为3%的NaCl溶液。
①计算所需质量分数为6%的NaCl溶液的质量为_______ g。
②在配制该溶液的过程中,下列实验仪器不需要选用的是_____ (填字母序号)。_________ (填“10mL”或“50mL”)的量筒量取所需水(密度约为1g/cm3)的体积。
【资料】NaCl和Na2CO3两种物质在不同温度时的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 | 53.2 | |
(1)生活在盐湖、碱湖附近的人们传承下来的劳动经验是“夏天晒盐,冬天捞碱”。
①Na2CO3俗称苏打或
②夏天“晒盐”,当有大量盐析出后,所得溶液为该温度下NaCl的
(2)在实验室进行粗盐提纯时,使用蒸发皿蒸发过程中,有时会出现液滴飞溅现象
(3)在实验室用质量分数为6%的NaCl溶液(密度约为1.04g/m3)配制80g质量分数为3%的NaCl溶液。
①计算所需质量分数为6%的NaCl溶液的质量为
②在配制该溶液的过程中,下列实验仪器不需要选用的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】KNO3和KCl的溶解度曲线如下图所示:
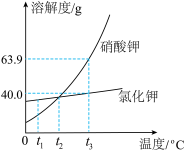
(1)t3°C时,KNO3的溶解度为____________ 。
(2)将t3°C时KCl的饱和溶液420.0g稀释成质量分数为20.0%的KCl溶液,请计算需加水____________ g。查阅相关物质的密度后,在实验室完成该实验通常要的玻璃仪器有胶头滴管、玻璃棒、____________ (填字母)。
a.托盘天平 b.烧杯 c.药匙 d.量筒 e.漏斗
(3)现有t2℃时KNO3的饱和溶液和KCl的饱和溶液。不考虑水的蒸发,下列关系一定成立的是_________ (填字母)
a.分别降温到t1°C,两溶液中溶质的质量分数相等
b.分别升温至t3°C,各自加入对应溶质至溶液饱和,所加KNO3质量大于KCl质量
c.保持t2°C不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
d.分别升温至t3°C,两溶液中溶质的质量分数相等

(1)t3°C时,KNO3的溶解度为
(2)将t3°C时KCl的饱和溶液420.0g稀释成质量分数为20.0%的KCl溶液,请计算需加水
a.托盘天平 b.烧杯 c.药匙 d.量筒 e.漏斗
(3)现有t2℃时KNO3的饱和溶液和KCl的饱和溶液。不考虑水的蒸发,下列关系一定成立的是
a.分别降温到t1°C,两溶液中溶质的质量分数相等
b.分别升温至t3°C,各自加入对应溶质至溶液饱和,所加KNO3质量大于KCl质量
c.保持t2°C不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
d.分别升温至t3°C,两溶液中溶质的质量分数相等
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下:
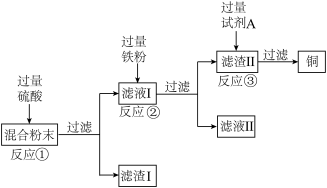
(1)写出下列反应的化学方程式:
反应①:____________________________________________ ;
反应②:____________________________________________ 。
(2)反应①所用的硫酸的质量分数为24.5%。现要配制40 g 24.5%的硫酸,需______ g 98%的硫酸和______ g水。实际操作时,用10 mL量筒取98%的硫酸(密度为1.84 g/cm3),请在图中表示出所取硫酸的体积_____ 。

(3)在进行“反应①”“反应②”“反应③” 的操作时,可将反应物加入________ (填仪器名称)中,然后______________________ (填操作),使反应充分进行。
(4)试剂A可选用__________ (填化学式)溶液。
(5)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)______________________________________________________ 。

(1)写出下列反应的化学方程式:
反应①:
反应②:
(2)反应①所用的硫酸的质量分数为24.5%。现要配制40 g 24.5%的硫酸,需

(3)在进行“反应①”“反应②”“反应③” 的操作时,可将反应物加入
(4)试剂A可选用
(5)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
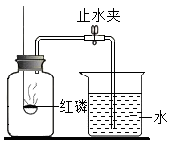
(1)红磷在集气瓶中发生反应的文字表达式为______________________ .该实验中红磷稍过量,目的是___________________________________________ ;
(2)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,进水量约是_________ 由本实验还可以推知氮气的哪一性质?试写出其中一种_______ 。
(3)若将红磷换成炭粉,该实验能否获得成功?________ ,理由是________________ ;
若将红磷换成铁丝,该实验能否获得成功?________ ,理由是________________ 。

(1)红磷在集气瓶中发生反应的文字表达式为
(2)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,进水量约是
(3)若将红磷换成炭粉,该实验能否获得成功?
若将红磷换成铁丝,该实验能否获得成功?
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组利用氯酸钾与二氧化锰制取氧气后,欲从固体混合物中分离氯化钾和二氧化锰,进行了以下流程图所示实验。请根据实验流程及相关实验数据回答下列问题:

(1)操作X的名称为______ 。
(2)检验滤渣是否洗净的方法是:取少许最后一次洗涤液至试管,滴加________ (填化学式)溶液,若无明显现象,则滤渣已洗涤干净。
(3)理论上4.90g氯酸钾完全分解可得到氯化钾________ g。
(4)实验中导致氯化钾实际产量与理论产量存在差别的原因可能是_____(填字母)。

(1)操作X的名称为
(2)检验滤渣是否洗净的方法是:取少许最后一次洗涤液至试管,滴加
(3)理论上4.90g氯酸钾完全分解可得到氯化钾
(4)实验中导致氯化钾实际产量与理论产量存在差别的原因可能是_____(填字母)。
| A.加入的水不足 |
| B.蒸发过程中没有用玻璃棒搅拌 |
| C.蒸发后烘干不彻底 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
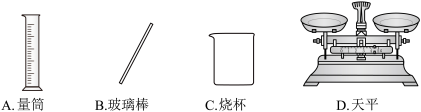
【推荐3】食盐(氯化钠)是生活必需品。提纯含少量泥沙的粗盐,经过以下操作流程:
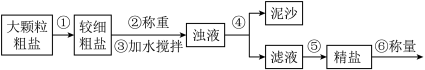
(1)整个流程中不需要用到的仪器是______(选填序号)。
(2)操作④中,所用玻璃仪器有_______ 、玻璃棒、烧杯。
(3)操作⑤中,当蒸发皿中出现较多固体时,应该_______(选填序号)。
(4)实验最后称量获得的精盐并计算精盐的产率(用所得精盐质量除以原粗盐质量),发现制得率较低,其可能原因是_______(选填序号)。

(1)整个流程中不需要用到的仪器是______(选填序号)。
| A.研钵 | B.量筒 | C.托盘天平 | D.药匙 |
(2)操作④中,所用玻璃仪器有
(3)操作⑤中,当蒸发皿中出现较多固体时,应该_______(选填序号)。
| A.移去酒精灯,停止搅拌 |
| B.移去酒精灯,用玻璃棒继续搅拌 |
| C.继续加热直至蒸干水分,再移去酒精灯 |
(4)实验最后称量获得的精盐并计算精盐的产率(用所得精盐质量除以原粗盐质量),发现制得率较低,其可能原因是_______(选填序号)。
| A.食盐没全溶解即过滤 | B.过滤时滤纸有破损 | C.蒸发时食盐飞溅剧烈 |
您最近一年使用:0次