名校
解题方法
1 . 偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力。下列叙述中正确的是
| A.偏二甲肼中含有C、H、N三个元素 |
| B.6.02×1023个偏二甲肼分子的质量为60 g |
| C.1 mol偏二甲肼的质量为60 g/mol |
| D.6 g偏二甲肼含有NA个偏二甲肼分子 |
您最近一年使用:0次
2 . 氨气有刺激性气味,结合表中信息,能得出的是
| 物质 | 分子个数 | 体积 | ||
| 0℃/101kPa | 20℃/101kPa | 0℃/202kPa | ||
| 17g氨气 | 约 个 个 | 22.4L | 24.1L | 11.2L |
| A.1mol氨气的体积为22.4L | B.将氮肥与熟石灰混合后研磨能闻到氨味 |
| C.温度升高,氨分子体积变大 | D.压强变大,氨分子间的间隔变小 |
您最近一年使用:0次
24-25九年级上·全国·课后作业
解题方法
3 .  中,氧化剂是
中,氧化剂是__ ,氧化产物是___ ,氧化产物与还原产物质量之比是___ ,被氧化与未被氧化的HCl的质量之比为____ ,电子转移的总数为____ ,若有7.3 g HCl被氧化,产生Cl2的质量为____ g。
 中,氧化剂是
中,氧化剂是
您最近一年使用:0次
4 . 关于物质的量的描述正确的是
| A.1mol氢原子的质量为2g | B.1mol水的质量是18g/mol |
| C.物质的量是基本物理量之一 | D.摩尔是一个物理量的名称 |
您最近一年使用:0次
解题方法
5 . 有关说法正确的是
| A.质量相等的CO和N2所含原子数一样 | B.1molO3比1molO2多1个氧原子 |
| C.氧分子的摩尔质量是16g/mol | D.1个硫原子的质量是32g |
您最近一年使用:0次
6 . 十二水硫酸铝铵[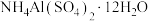 ,相对分子质量为453]是一种提高能源效率的热能存储体材料,一种制备的工艺流程如图。
,相对分子质量为453]是一种提高能源效率的热能存储体材料,一种制备的工艺流程如图。____________________ 。
(2)“结晶器”中的操作顺序:蒸发浓缩、__________ 、过滤。
(3)“反应器2”的反应为 ,若要制得
,若要制得 的十二水硫酸铝铵,至少需消耗
的十二水硫酸铝铵,至少需消耗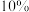 的
的 溶液的质量是多少?
溶液的质量是多少?__________ (写出计算过程)
(4)取 的
的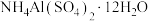 固体加热,固体质量随温度的变化如图。
固体加热,固体质量随温度的变化如图。__________ ,剩余固体质量为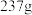 。
。
ii.B点物质为纯净物,化学式为____________________ 。
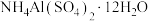 ,相对分子质量为453]是一种提高能源效率的热能存储体材料,一种制备的工艺流程如图。
,相对分子质量为453]是一种提高能源效率的热能存储体材料,一种制备的工艺流程如图。
(2)“结晶器”中的操作顺序:蒸发浓缩、
(3)“反应器2”的反应为
 ,若要制得
,若要制得 的十二水硫酸铝铵,至少需消耗
的十二水硫酸铝铵,至少需消耗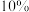 的
的 溶液的质量是多少?
溶液的质量是多少?(4)取
 的
的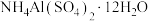 固体加热,固体质量随温度的变化如图。
固体加热,固体质量随温度的变化如图。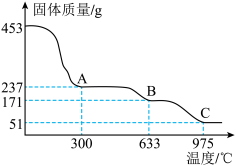
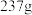 。
。ii.B点物质为纯净物,化学式为
您最近一年使用:0次
解题方法
7 . 青草沙水库拥有大量优质淡水,其规模占上海全市原水供应总规模的50%以上。
(1)1 mol水中约含有_______ 个氧原子,为了除去天然水中的微生物,可通入_______ 。
(2)电解水实验中,产生氢气的体积是氧气的_______ 倍。氢气可液化储存,液化过程中,分子间间隔_______ (选填“变大”、“变小”或“不变”),氢气与液氢_______ (选填“是”或“不是”)同素异形体。
(3)水是一种良好的溶剂,下表是硝酸钾的溶解度。
20℃时,在烧杯中加入50g硝酸钾固体和100mL水,充分溶解后得到的是硝酸钾的_______ (选填“饱和”或“不饱和”)溶液,为了提升溶液的浓度,可进行的实验操作是_______ 。
(1)1 mol水中约含有
(2)电解水实验中,产生氢气的体积是氧气的
(3)水是一种良好的溶剂,下表是硝酸钾的溶解度。
| 温度(℃) | 10 | 20 | 30 | 40 | 60 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 110 |
您最近一年使用:0次
2024-07-13更新
|
30次组卷
|
2卷引用:2024年上海市长宁区九年级中考二模综合测试试题-初中化学
解题方法
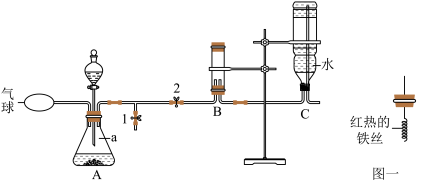
8 . 小顾同学利用创新的实验装置进行实验(装置气密性良好)。
①写出编号a仪器的名称_____ 。
②打开弹簧夹1、关闭弹簧夹2,在尖嘴处观察到带火星的小木条复燃,说明_____ 。
③关闭弹簧夹1、打开弹簧夹2,利用_____ 收集氧气。反应一段时间后,B装置中液面不再发生变化时,关闭弹簧夹2,将红热的铁丝(图一)放入B装置中,观察到的现象是 _____ 。
(2)实验二:制取二氧化碳并验证其性质
①用块状大理石和稀硫酸为原料,利用A装置不可以制取CO2的原因是_____ 。
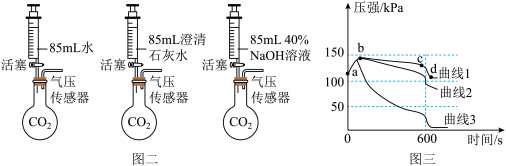
②打开弹簧夹1、关闭弹簧夹2,用3个250mL的烧瓶收集满CO2进行实验。
I、曲线1中导致cd段气压快速变小的操作是_______ 。
II、曲线2中发生反应的化学方程式为_________ 。
Ⅲ、比较曲线2与曲线3的差异,说明原因_____ 。
IV、根据图三所示,可以得出的结论是_____ (填序号)。
A.1体积水中溶解CO2的量小于1体积
B.CO2能与水发生反应
C.CO2能与NaOH溶液发生反应
D.检验CO2用饱和澄清石灰水较合适
V、实验室制取2.2g二氧化碳,至少需要碳酸钙_________ mol。
①写出编号a仪器的名称
②打开弹簧夹1、关闭弹簧夹2,在尖嘴处观察到带火星的小木条复燃,说明
③关闭弹簧夹1、打开弹簧夹2,利用
(2)实验二:制取二氧化碳并验证其性质
①用块状大理石和稀硫酸为原料,利用A装置不可以制取CO2的原因是
②打开弹簧夹1、关闭弹簧夹2,用3个250mL的烧瓶收集满CO2进行实验。
I、曲线1中导致cd段气压快速变小的操作是
II、曲线2中发生反应的化学方程式为
Ⅲ、比较曲线2与曲线3的差异,说明原因
IV、根据图三所示,可以得出的结论是
A.1体积水中溶解CO2的量小于1体积
B.CO2能与水发生反应
C.CO2能与NaOH溶液发生反应
D.检验CO2用饱和澄清石灰水较合适
V、实验室制取2.2g二氧化碳,至少需要碳酸钙
您最近一年使用:0次
2024·广东·模拟预测
解题方法
9 . 设NA为阿伏伽德罗常数的值,下列说法中正确的是
| A.24g质量分数为25%的甲醛水溶液中含有氢原子数目为2.4NA |
B.标准状况下,22.4L正丙醇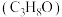 分子中含有C-H的数目为8NA 分子中含有C-H的数目为8NA |
C. 的H2SO4溶液与足量的Zn反应产生的氢气分子数目为 的H2SO4溶液与足量的Zn反应产生的氢气分子数目为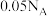 |
D.0.1molFeI2与0.1molCl2反应时,转移电子的数目为 |
您最近一年使用:0次
10 . 随着科学技术的进步,我国航天事业取得巨大成就。
(1)火星大气中含有大量二氧化碳和少量水蒸气等气体,水蒸气中元素的存在状态是_____ (填“游离态”或“化合态”),若地球大气中二氧化碳含量过多会加剧的环境问是_____ 。
(2)2021年10月,神舟十三号三名航天员进驻“太空之家”,开启半年太空生活。为降低太空辐射对航天员产生的伤害,航天员需要适当补充维生素C(化学式为 ),该物质分子中碳、氢、氧原子的物质的量比为
),该物质分子中碳、氢、氧原子的物质的量比为_____ , 维生素C中约含
维生素C中约含_____  碳原子。
碳原子。
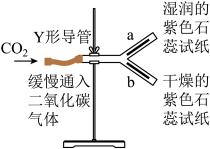
实验室用下图装置制取纯净、干燥的 ,并验证其部分性质。
,并验证其部分性质。_____ 。
(4)为证明装置C中浓硫酸具有吸水性,烧杯D中应放入_____ 。
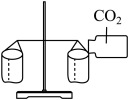
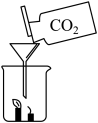
(5)将装置A、E连接,不能证明 的密度比空气大的装置是
的密度比空气大的装置是_____
(1)火星大气中含有大量二氧化碳和少量水蒸气等气体,水蒸气中元素的存在状态是
(2)2021年10月,神舟十三号三名航天员进驻“太空之家”,开启半年太空生活。为降低太空辐射对航天员产生的伤害,航天员需要适当补充维生素C(化学式为
 ),该物质分子中碳、氢、氧原子的物质的量比为
),该物质分子中碳、氢、氧原子的物质的量比为 维生素C中约含
维生素C中约含 碳原子。
碳原子。实验室用下图装置制取纯净、干燥的
 ,并验证其部分性质。
,并验证其部分性质。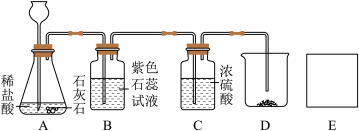
(4)为证明装置C中浓硫酸具有吸水性,烧杯D中应放入
(5)将装置A、E连接,不能证明
 的密度比空气大的装置是
的密度比空气大的装置是
|
|
|
|
| a | b | c | d |
您最近一年使用:0次