1 . NA表示阿伏加德罗常数的值,下列说法不正确的是
| A.32g S2和SO2混合物中的质子数目为16NA |
| B.32g Cu和32g S 充分反应,转移电子数为NA |
| C.精炼铜时,若阳极失去0.1 NA 个电子,则阴极增重3.2g |
| D.等物质的量的钠分别在足量的氧气和氯气中燃烧,转移电子数相等 |
您最近半年使用:0次
解题方法
2 . 设 代表阿伏加德罗常数的值。臭氧能氧化
代表阿伏加德罗常数的值。臭氧能氧化 ,通常用于处理电镀工业含氰废水,其化学原理为
,通常用于处理电镀工业含氰废水,其化学原理为 。下列叙述正确的是
。下列叙述正确的是
 代表阿伏加德罗常数的值。臭氧能氧化
代表阿伏加德罗常数的值。臭氧能氧化 ,通常用于处理电镀工业含氰废水,其化学原理为
,通常用于处理电镀工业含氰废水,其化学原理为 。下列叙述正确的是
。下列叙述正确的是A.处理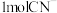 时生成还原产物 时生成还原产物 的分子数为 的分子数为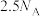 |
B.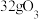 和 和 的混合气体中含氧原子数为 的混合气体中含氧原子数为 |
C.每生成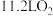 的同时生成 的同时生成 数为 数为 |
D.由离子方程式知每生成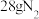 时转移电子数为 时转移电子数为 |
您最近半年使用:0次
名校
3 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.含2mol  的浓硫酸与64g Cu共热,生成 的浓硫酸与64g Cu共热,生成 分子数为 分子数为 |
B.常温下,5.6g铁与足量的浓硝酸反应,转移的电子数为0.3 |
C.0.4mol Fe与足量的S反应,转移的电子数为1.2 |
D.标准状况下,22.4L  中含有的共价键数目为3 中含有的共价键数目为3 |
您最近半年使用:0次
4 . CO与H2S反应可以制得COS,其化学方程式为 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是
 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是| A.2.8g中含有的中子数为1.4NA |
B.pH=3的H2S溶液中 的数目为0.001NA 的数目为0.001NA |
C.0.1molCOS中 键数目为0.4NA 键数目为0.4NA |
| D.生成2.24LH2(标准状况),转移电子数目为0.4NA |
您最近半年使用:0次
名校
5 . 微观探析是认识物质的一种途径。设 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是
 为阿伏加德罗常数,下列有关说法正确的是
为阿伏加德罗常数,下列有关说法正确的是A.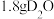 中含有的中子数目为 中含有的中子数目为 |
B.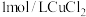 溶液中含有 溶液中含有 的数目小于 的数目小于 |
| C.1 mol CO2分子中含有2NA个σ键和2NA个sp2杂化轨道 |
D.0℃,101kPa,2.24LCl2与NaOH溶液完全反应,转移电子数目为 |
您最近半年使用:0次
名校
6 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.25℃时,1LpH=13的Ba(OH)2溶液中OH-的数目为0.2NA |
| B.密闭容器中1.2molN2与3molH2合成氨,平衡后容器内气体分子总数大于2.2NA |
| C.标准状况下,22.4LCl2与水反应,转移电子数为NA |
| D.1L0.1mol/L的NH4Cl溶液中NH4+的数目为0.1NA |
您最近半年使用:0次
名校
解题方法
7 . 设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,4.48LNH3溶于水得到的溶液中,NH3⋅H2O和 的总数小于0.2NA 的总数小于0.2NA |
| B.常温下,5.6g铁与足量的浓硝酸反应,转移的电子数为0.3NA |
| C.0.4molFe与足量的S反应,转移的电子数为1.2NA |
| D.含2molH2SO4的浓硫酸与64gCu共热,生成SO2分子数为NA |
您最近半年使用:0次
名校
8 . 设 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是
 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是A.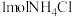 中所含共价键的数目为 中所含共价键的数目为 |
B.pH=2的稀硫酸中 数目为 数目为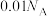 |
C. 和 和 的固体混合物中含有阳离子数目为 的固体混合物中含有阳离子数目为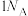 |
D.用惰性电极电解 溶液,当阳极产生标况下的气体体积为224mL时,电路中转移电子数为 溶液,当阳极产生标况下的气体体积为224mL时,电路中转移电子数为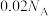 |
您最近半年使用:0次
9 . 高效率和高选择性地将 转化为
转化为 是
是 资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原
资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原 提供了一种可行的转化方案,其原理如图所示,设
提供了一种可行的转化方案,其原理如图所示,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 转化为
转化为 是
是 资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原
资源化利用的途径之一,我国科研工作者开发了一种空腔串联反应器,为电催化还原 提供了一种可行的转化方案,其原理如图所示,设
提供了一种可行的转化方案,其原理如图所示,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是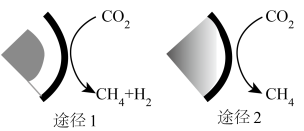
A.44g 中中心原子C的价层电子对数为 中中心原子C的价层电子对数为 |
B.1  中所含中子数一定为10 中所含中子数一定为10 |
C.途径2生成标准状况下22.4L ,反应转移电子数为8 ,反应转移电子数为8 |
D.若利用电解原理实现途径1, 在阳极放电 在阳极放电 |
您最近半年使用:0次
10 .  是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A. 与一定量的稀硝酸反应,转移电子数目一定为 与一定量的稀硝酸反应,转移电子数目一定为 |
B.沸腾炉中 被完全氧化,转移电子的数目为 被完全氧化,转移电子的数目为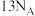 |
C.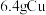 粉与足量S粉加热充分反应转移的电子数为 粉与足量S粉加热充分反应转移的电子数为 |
D.标准状况下,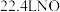 和 和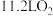 混合后分子总数为 混合后分子总数为 |
您最近半年使用:0次



