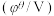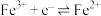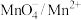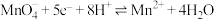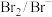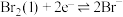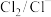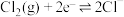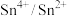名校
解题方法
1 . 已知还原性: ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为
 ,则将
,则将 通入到
通入到 、
、 、
、 的混合溶液中,
的混合溶液中, 、
、 、
、 生成的先后顺序为
生成的先后顺序为A. , , , , | B. , , , , | C. , , , , | D. , , , , |
您最近半年使用:0次
解题方法
2 . 下列离子方程式正确的是
A.向 溶液中加入少量 溶液中加入少量 溶液: 溶液: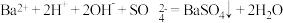 |
B.将SO2通入NaCIO溶液中:SO2+H2O+ClO-=HClO+HSO |
| C.FeBr2与等物质的量氯气在溶液中反应:Cl2+2Br-=Br2+2Cl- |
D.向苯酚钠溶液中通入少量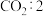 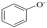 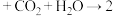 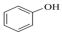  |
您最近半年使用:0次
3 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_______ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是_______ (填序号,下同),发生还原反应的是_______ ,既没发生氧化反应又没发生还原反应的是_______ 。(提示:铬元素的化合价有+6、+3)_______ 。
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目_______ 。
②上述反应中氧化产物和还原产物的质量比为_______ 。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(4)化学实验中,若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。
①在如下图所示步骤中,发生氧化反应的是
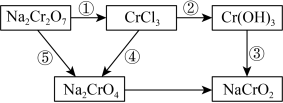
_______K2Cr2O7+_______HCl=_______Cl2↑+_______KCl+_______CrCl3+_______
(5)已知方程式F:KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑。
①请用双线桥法标出电子转移的方向和数目
②上述反应中氧化产物和还原产物的质量比为
您最近半年使用:0次
4 . (一)有以下几种物质:
①碳酸氢钠晶体 ②液态的HCl ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰,试回答(填序号):
(1)以上物质能导电的是___________ 。
(2)以上物质中属于非电解质的是___________ 。
(3)以上物质中溶于水后水溶液能导电的是___________ 。
(二)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(4)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是___________ (填字母)。___________ 。
(6)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:4Ag+2H2S+O2=2X+2H2O。则X的化学式是___________ 。其中H2S在该反应中___________ (填字母)。
A. 氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
①碳酸氢钠晶体 ②液态的HCl ③铁 ④蔗糖 ⑤酒精 ⑥熔融的K2SO4 ⑦干冰,试回答(填序号):
(1)以上物质能导电的是
(2)以上物质中属于非电解质的是
(3)以上物质中溶于水后水溶液能导电的是
(二)虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(4)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是
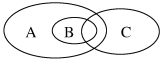
(6)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:4Ag+2H2S+O2=2X+2H2O。则X的化学式是
A. 氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
您最近半年使用:0次
解题方法
5 . 将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O= +2Fe2++4H+;
+2Fe2++4H+;
② +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。
下列有关说法正确的是
①SO2+2Fe3++2H2O=
 +2Fe2++4H+;
+2Fe2++4H+;②
 +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。下列有关说法正确的是
| A.还原性:SO2>Cr3+>Fe2+ | B.氧化性: >SO2>Fe3+ >SO2>Fe3+ |
| C.两个反应中Fe2(SO4)3均是还原剂 | D. 能将Na2SO3氧化成Na2SO4 能将Na2SO3氧化成Na2SO4 |
您最近半年使用:0次
6 . 根据下列实验操作、现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溴乙烷与NaOH乙醇溶液加热反应产生的气体通入盛有酸性高锰酸钾溶液的试管中 | 试管中的溶液紫红色褪去 | 溴乙烷发生了消去反应,生成了乙烯气体 |
| B | 向FeCl2、KBr的混合溶液中滴入少量氯水,充分反应后再加入一定量的CCl4,振荡、静置分层,观察下层颜色;再向上层溶液中滴加KSCN溶液 | 下层溶液呈无色,往上层溶液中滴加KSCN溶液后,溶液变为血红色 | 氧化性:Cl2>Br2>Fe3+ |
| C | 向某溶液中加入NaOH浓溶液并加热,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 该溶液中一定没有 |
| D | 向滴有KSCN的FeCl3溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 纯净物状态下的标准电极电势可用来比较对应氧化剂的氧化性强弱。现有六组标准电极电势数据如表所示:
下列分析正确的是
氧化还原电对(氧化型/还原型) | 电极反应式 | 标准电极电势 |
|
| 0.77 |
|
| 0.54 |
|
| 1.50 |
|
| 1.07 |
|
| 1.36 |
|
| 0.15 |
A.氧化性: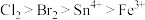 |
B.往含有 的 的 溶液中滴加少量氯水,溶液变红 溶液中滴加少量氯水,溶液变红 |
C.往淀粉- 溶液中加入过量 溶液中加入过量 溶液,溶液变蓝 溶液,溶液变蓝 |
D. 溶液与足量酸性 溶液与足量酸性 溶液反应的离子方程式: 溶液反应的离子方程式: |
您最近半年使用:0次
2024高三下·全国·专题练习
8 . 为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。后者常采用 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是
,下列说法不正确的是
 作还原剂,其反应之一为:
作还原剂,其反应之一为: ,下列说法不正确的是
,下列说法不正确的是| A.氧化产物与还原产物的质量比为3∶4 |
| B.生成1mol水转移电子的物质的量为2mol |
C.可使用 溶液吸收氮氧化物 溶液吸收氮氧化物 |
| D.氮氧化物的排放可形成酸雨 |
您最近半年使用:0次
解题方法
9 . 硒(Se)是一种新型半导体材料。对富硒废料(主要成分为CuSe和Ag2Se)进行综合处理的一种工艺流程如图:
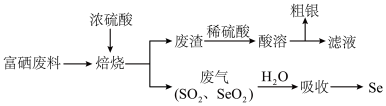
| A.O、S、Se属于同主族元素 |
| B.SeO2既有氧化性又有还原性,其还原性比SO2强 |
C.“焙烧”时的主要反应为CuSe+4H2SO4(浓) CuSO4+SeO2↑+3SO2↑+4H2O CuSO4+SeO2↑+3SO2↑+4H2O |
| D.向“滤液”中滴加过量的氨水,可得到深蓝色的透明溶液 |
您最近半年使用:0次
10 . 氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)人体正常的血红蛋白中含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而使人体中毒,服用维生素C可解毒。
而使人体中毒,服用维生素C可解毒。 转化为
转化为 时,
时, 在反应中被
在反应中被______ (填“氧化”或“还原”);服用维生素C可使血红蛋白中的 转变成
转变成 ,说明维生素C作
,说明维生素C作______ (填“氧化”或“还原”)剂。
(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使 和
和 反应,生成
反应,生成 和
和 。写出该反应的化学方程式并用双线桥法标出电子转移的方向和数目
。写出该反应的化学方程式并用双线桥法标出电子转移的方向和数目______
(3)某届奥运会期间,由于工作人员将84消毒液(有效成分 )与双潮水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
)与双潮水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
______  (填“>”或“<”);当参加反应的,
(填“>”或“<”);当参加反应的, 和
和 分子的个数比为1:1时,该反应的还原产物为
分子的个数比为1:1时,该反应的还原产物为______ (填字母序号)。
A. B.
B. C.
C. D.
D. E.
E. F.
F.
(4)过氧化钙( )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取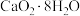 ,再经脱水制得
,再经脱水制得 ,
,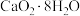 不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水
不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水 ,其制备过程如下:
,其制备过程如下:______
Ⅱ.“沉淀”时发生的反应用化学方程式表示为:______ 。
(1)人体正常的血红蛋白中含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而使人体中毒,服用维生素C可解毒。
而使人体中毒,服用维生素C可解毒。 转化为
转化为 时,
时, 在反应中被
在反应中被 转变成
转变成 ,说明维生素C作
,说明维生素C作(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使
 和
和 反应,生成
反应,生成 和
和 。写出该反应的化学方程式并用双线桥法标出电子转移的方向和数目
。写出该反应的化学方程式并用双线桥法标出电子转移的方向和数目(3)某届奥运会期间,由于工作人员将84消毒液(有效成分
 )与双潮水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
)与双潮水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当参加反应的,
(填“>”或“<”);当参加反应的, 和
和 分子的个数比为1:1时,该反应的还原产物为
分子的个数比为1:1时,该反应的还原产物为A.
 B.
B. C.
C. D.
D. E.
E. F.
F.
(4)过氧化钙(
 )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取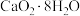 ,再经脱水制得
,再经脱水制得 ,
,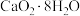 不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水
不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水 ,其制备过程如下:
,其制备过程如下: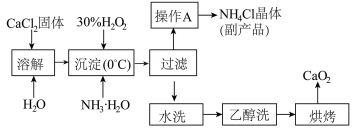
Ⅱ.“沉淀”时发生的反应用化学方程式表示为:
您最近半年使用:0次