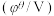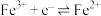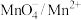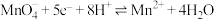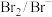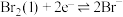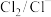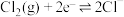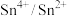解题方法
1 . 为了验证Fe3+的氧化性,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计正确的是
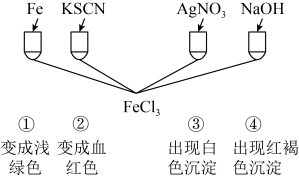
| A.① | B.② | C.③ | D.④ |
您最近半年使用:0次
名校
解题方法
2 . 下列方程式与所给事实相符的是
| A.“84”消毒液不能和洁厕灵混用是因为ClO-+Cl-+2H+=Cl2 ↑+H2O |
| B.Fe和稀硝酸反应:Fe+2H+=Fe2++H2 ↑ |
C.向NaClO溶液中通如少量SO2:2ClO-+SO2+H2O=2HClO+ |
| D.向CuSO4溶液中通入H2S气体:Cu2++S2-=CuS↓ |
您最近半年使用:0次
名校
解题方法
3 . 下列反应既是氧化还原反应,又是吸热反应的是
| A.碳和二氧化碳在高温下的反应 | B.碳酸钙高温分解 |
| C.氢氧化钠和盐酸的反应 | D.铝片和稀硫酸反应 |
您最近半年使用:0次
解题方法
4 . 侯德榜是我国近代著名的化学家,他提出的联合制碱法得到世界各国的认可,其工艺流程如图所示。下列说法正确的是
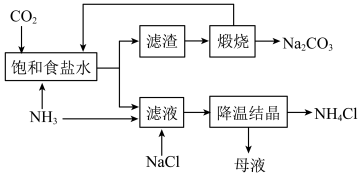
A.向“饱和食盐水”中先通入 ,后通入 ,后通入 |
| B.该工艺流程中涉及了氧化还原反应 |
| C.碳酸氢钠固体中若混有少量碳酸钠,可通过煅烧,除去碳酸钠 |
D.“母液”中溶质的主要成分是 ,可循环利用 ,可循环利用 |
您最近半年使用:0次
解题方法
5 . I.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)FeO 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)请用单线桥表示反应中电子转移情况:___________ 。
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:___________ (填元素符号);它在周期表中的位置为___________ 。
(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是___________ (填化学式),写出该单质与氢氧化钠反应的离子方程式___________ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)FeO
 中铁元素的化合价为
中铁元素的化合价为(2)请用单线桥表示反应中电子转移情况:
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
A.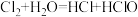 | B. |
C. | D. |
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:

(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是
您最近半年使用:0次
6 . 人体缺乏维生素C(Vc)易得坏血症。下图是维生素C的结构简式。___________ (填官能团名称)。
(2)在维生素C溶液中滴加紫色石蕊试液,溶液颜色变红,说明维生素C具有___________ 性,在维生素C溶液中滴入少量蓝色的含有淀粉的碘溶液,可观察到溶液蓝色褪去,说明维生素C具有 ___________ 性。
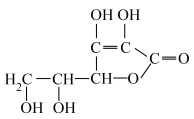
(2)在维生素C溶液中滴加紫色石蕊试液,溶液颜色变红,说明维生素C具有
您最近半年使用:0次
解题方法
7 . 氯气常用于自来水的杀菌消毒,实验室常用MnO2和浓盐酸共热制备氯气。
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。___________ 。
②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是___________ 。
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象___________ 。
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是___________ (填字母)。
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为___________ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是___________ (填序号)。
A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的___________ 倍。(假设ClO2、Cl2全部都被还原为Cl-,没有其它的含氯产物生成)
(1)若0.1mol∙L-1 MnO2和25mL12mol∙L-1盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为___________(不考虑盐酸的挥发)
| A.等于0.15mol | B.小于0.15mol |
| C.大于0.15mol,小于0.3mol | D.以上结论都不正确 |
(2)若改用漂白粉与浓盐酸反应制备氯气,装置如图所示,同时验证氯气性质(其中夹持装置已省略)。

②从反应条件看,MnO2和Ca(ClO)2的氧化能力不同,氧化能力较强的是
③装置B除了用于除去挥发的HCl,也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象
④装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(3)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①其中氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
③常温常压下,ClO2的消毒能力是等体积Cl2的
您最近半年使用:0次
名校
解题方法
8 . 下列叙述正确的是
| A.CO2和SiO2都是酸性氧化物,所以两者物理性质相似 |
| B.CO2和SiO2都能与碳反应,且都作氧化剂 |
C.因为 ,所以硅酸的酸性比碳酸的酸性强 ,所以硅酸的酸性比碳酸的酸性强 |
| D.SiO2既能与NaOH溶液反应,又能与氢氟酸反应,所以二氧化硅属于两性氧化物 |
您最近半年使用:0次
名校
解题方法
9 . 下列指定反应的离子方程式书写正确的是
A.过量SO2与“84”消毒液反应:ClO-+H2O+SO2= +HClO +HClO |
| B.将SO2通入Ba(NO3)2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+ |
C.向稀硝酸中加入过量铁粉:Fe+ +4H+=Fe3++NO↑+2H2O +4H+=Fe3++NO↑+2H2O |
D.用氨水吸收少量SO2:2NH3·H2O+SO2=2 + + +H2O +H2O |
您最近半年使用:0次
10 . 纯净物状态下的标准电极电势可用来比较对应氧化剂的氧化性强弱。现有六组标准电极电势数据如表所示:
下列分析正确的是
氧化还原电对(氧化型/还原型) | 电极反应式 | 标准电极电势 |
|
| 0.77 |
|
| 0.54 |
|
| 1.50 |
|
| 1.07 |
|
| 1.36 |
|
| 0.15 |
A.氧化性: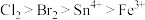 |
B.往含有 的 的 溶液中滴加少量氯水,溶液变红 溶液中滴加少量氯水,溶液变红 |
C.往淀粉- 溶液中加入过量 溶液中加入过量 溶液,溶液变蓝 溶液,溶液变蓝 |
D. 溶液与足量酸性 溶液与足量酸性 溶液反应的离子方程式: 溶液反应的离子方程式: |
您最近半年使用:0次