解题方法
1 . 已知蓝色环保颜料 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是A.简单离子半径: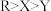 | B.最简单氢化物的稳定性: |
| C.Y的最高价氧化物对应的水化物为强酸 | D.W、Z形成的二元化合物为离子化合物 |
您最近半年使用:0次
解题方法
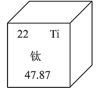
2 . 元素周期表中钛的数据如图所示,47.87的含义是___________ ;Ti在元素周期表中的位置是___________ ;基态钛原子的价电子排布式为___________ (填选项)。
您最近半年使用:0次
3 . 关于LiBF4及所含元素的说法正确的是
| A.熔点:LiBF4<H3BO3 | B.原子半径:Li<B<F |
| C.第一电离能:Li<B<F | D.电负性:Li<B<F |
您最近半年使用:0次
4 . Q、W、X、Y、Z是原子序数依次增大的短周期元素,其最高正化合价与原子半径如图所示,硫磺易溶于WZ2,Q、W原子序数之和等于X原子序数。
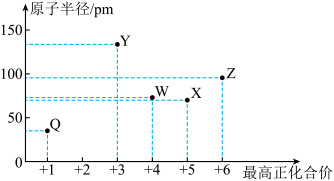
A.简单氢化物的沸点: | B.最高价含氧酸的酸性: |
C. 位于元素周期表第二周期第Ⅲ 位于元素周期表第二周期第Ⅲ 族 族 | D. 和 和 形成的18电子的微粒只有1种 形成的18电子的微粒只有1种 |
您最近半年使用:0次
7日内更新
|
58次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题
名校
5 . 已知A、B、C、D、E、F、G、H是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和G分别为同一主族元素,B原子的最外层电子数比次外层多3,F的最高价氧化物的水化物既可以和强酸反应也可以和强碱溶液反应,G的单质常出现在火山口。
(1)C在元素周期表中的位置是_______ 。
(2)C、D分别形成的简单离子中,半径较大的是______ (填离子符号)。
(3)G和H的最高价氧化物的水化物酸性较强的是______ (填化学式)。
(4)由A、C、D形成的化合物中化学键的类型为_______ ,C、D形成摩尔质量为 的化合物的电子式为
的化合物的电子式为______ ,由A、B形成 化合物的结构式为
化合物的结构式为______ 。
(5)甲烷可与 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式_______ 。
(6)D、F的最高价氧化物的水化物相互反应的离子方程式为_______ 。
(7)可用湿润的______ 试纸检验H对应单质,涉及反应的离子方程式为_______ 。
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:________ 。
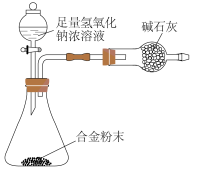
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是______ (用含m、a、b的式子表示)。
(1)C在元素周期表中的位置是
(2)C、D分别形成的简单离子中,半径较大的是
(3)G和H的最高价氧化物的水化物酸性较强的是
(4)由A、C、D形成的化合物中化学键的类型为
 的化合物的电子式为
的化合物的电子式为 化合物的结构式为
化合物的结构式为(5)甲烷可与
 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式(6)D、F的最高价氧化物的水化物相互反应的离子方程式为
(7)可用湿润的
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是
您最近半年使用:0次
6 . 催化剂(XYZ6ME5)的组成元素均为主族元素且在每个短周期均有分布,X的基态原子p轨道电子总数比s轨道电子总数多1个;仅Y、M、E处于同一周期,原子序数依次增大且相邻;E在地壳中含量最多。下列说法不正确的是
| A.第一电离能:M>E>X | B.简单氢化物的稳定性:E>M |
| C.氧化物的熔点:X>Y>Z | D.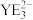 和 和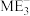 的空间结构相同 的空间结构相同 |
您最近半年使用:0次
解题方法
7 . 某阴离子由原子序数依次增大的同周期元素 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是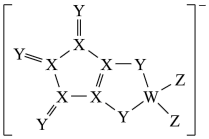
A.最高价含氧酸酸性: |
B. 、 、 的简单氢化物中 的简单氢化物中 的沸点高 的沸点高 |
C.原子半径: |
D.仅由 与 与 形成的化合物中可能含有非极性键 形成的化合物中可能含有非极性键 |
您最近半年使用:0次
解题方法
8 . 短周期主族元素W、X、Y、Z、Q的原子序数依次增大,且占据三个不同的周期。X的一种简单氢化物常用作制冷剂,Y在地壳中的含量最高,Z的基态原子价层电子排布式为ns1,Q的基态原子轨道中有2个未成对电子。下列说法正确的是
| A.原子半径:Q>Z>Y |
| B.第一电离能:Y>X>W |
| C.Q的最高价氧化物对应的水化物可能是强酸 |
D.XW3、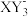 的空间结构名称均为三角锥形 的空间结构名称均为三角锥形 |
您最近半年使用:0次
9 . 某化合物的结构如图所示,其中X、Y、Z、Q为原子序数依次增大的四种短周期元素,X是元素周期表中原子半径最小的元素,Q的最外层电子数是其内层电子数的3倍。下列说法错误的是

| A.Y、Z、Q三种元素的非金属性逐渐增强 |
B.最外层电子数由大到小的顺序为 |
| C.该化合物中Z、Y、Q均满足8电子稳定结构 |
| D.仅由X、Z、Q三种元素形成的化合物不可能含有离子键 |
您最近半年使用:0次
7日内更新
|
149次组卷
|
2卷引用:2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学
名校
解题方法
10 . 某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)反应最剧烈的烧杯中金属是_______(填字母序号);
(2)实验中发现其中两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法_______ (填字母序号)。
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
(3)甲同学想从下列药品中选择最佳组合,比较Na、Mg、Al的金属性强弱。可供选择的药品有:①NH3·H2O、②NaOH溶液、③Al2(SO4)3溶液、④MgCl2溶液、⑤Na2CO3溶液、⑥NaCl溶液。你认为他所选的药品是_______ (填序号)﹔写出实验过程中Al3+与碱溶液的反应涉及的离子方程式:_______ 、_______ 。
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题,实验装置如图:(已知酸性强弱:亚硫酸>碳酸)_______ ﹔装置E中酸性高锰酸钾溶液的作用是_______ 。
(5)试管F中装有_______ 溶液;其中发生反应的离子方程式为:_______ 。
(6)能否由此得出硫、碳、硅三种元素非金属性的强弱,并说明理由:_______ 。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)反应最剧烈的烧杯中金属是_______(填字母序号);
| A.钠 | B.镁 | C.铝 | D.钾 |
(2)实验中发现其中两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择下列合适的方法
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
(3)甲同学想从下列药品中选择最佳组合,比较Na、Mg、Al的金属性强弱。可供选择的药品有:①NH3·H2O、②NaOH溶液、③Al2(SO4)3溶液、④MgCl2溶液、⑤Na2CO3溶液、⑥NaCl溶液。你认为他所选的药品是
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题,实验装置如图:(已知酸性强弱:亚硫酸>碳酸)
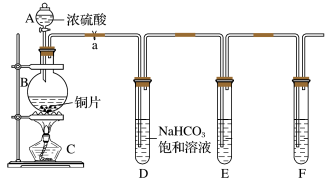
(5)试管F中装有
(6)能否由此得出硫、碳、硅三种元素非金属性的强弱,并说明理由:
您最近半年使用:0次



