1 . 第五届硒博会主题为“健康中国·硒引天下”。硒(Se)是第四周期第VI A族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g) 2Se(s)+2H2O(l) △H =a kJ·mol-1
2Se(s)+2H2O(l) △H =a kJ·mol-1
②2H2(g)+O2(g) 2H2O(l) △H=b kJ·mol-1
2H2O(l) △H=b kJ·mol-1
反应H2(g)+Se(s) H2Se(g)的反应热△H=
H2Se(g)的反应热△H=___________ kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1 mol Se,发生反应H2(g)+Se(s) H2Se(g),
H2Se(g),
①下列情况可判断反应达到平衡状态的是___________ (填字母代号)。
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
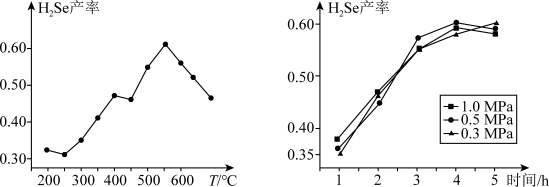
②以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图所示:___________ 。
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈___________ (填“酸性”或“碱性”),该溶液中的物料守恒关系式为___________ 。
(4)工业上从含硒废料中提取硒的方法是用硫酸和硝酸钠的混合溶液处理后获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸,硒酸与盐酸反应的化学方程式为___________ ,最后通入SO2析出硒单质。
(5)H2 Se在一定条件下可以制备出CuSe,已知常温时CuSe的Ksp=7.9×10-49,CuS的Ksp=1.3×10-36,则反应CuS(s)+Se2-(aq) CuSe(s)+S2-(aq)的化学平衡常数K=
CuSe(s)+S2-(aq)的化学平衡常数K=___________ (保留2位有效数字)。
(1)已知:①2H2Se(g)+O2(g)
 2Se(s)+2H2O(l) △H =a kJ·mol-1
2Se(s)+2H2O(l) △H =a kJ·mol-1②2H2(g)+O2(g)
 2H2O(l) △H=b kJ·mol-1
2H2O(l) △H=b kJ·mol-1反应H2(g)+Se(s)
 H2Se(g)的反应热△H=
H2Se(g)的反应热△H=(2)T℃时,向一恒容密闭容器中加入3molH2和1 mol Se,发生反应H2(g)+Se(s)
 H2Se(g),
H2Se(g),①下列情况可判断反应达到平衡状态的是
a.气体的密度不变 b.v(H2)=v(H2Se)
c.气体的压强不变 d.气体的平均摩尔质量不变
②以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图所示:
(3)已知常温下H2Se的电离平衡常数K1=1.3×10-4、K2=5.0×10-11,则NaHSe溶液呈
(4)工业上从含硒废料中提取硒的方法是用硫酸和硝酸钠的混合溶液处理后获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸,硒酸与盐酸反应的化学方程式为
(5)H2 Se在一定条件下可以制备出CuSe,已知常温时CuSe的Ksp=7.9×10-49,CuS的Ksp=1.3×10-36,则反应CuS(s)+Se2-(aq)
 CuSe(s)+S2-(aq)的化学平衡常数K=
CuSe(s)+S2-(aq)的化学平衡常数K=
您最近半年使用:0次
解题方法
2 . 化学与生活生产密切相关。下列说法正确的是
| A.“84”消毒液与洁厕灵(主要成分HCl)混合增强消毒效果 |
| B.利用高纯度单质硅可以制成太阳能光伏电池 |
| C.泡沫灭火器可用于一般的起火,也适用于电器起火 |
| D.盐碱地(含较多Na2CO3)不利于作物生长,可施加生石灰进行改良 |
您最近半年使用:0次
解题方法
3 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近半年使用:0次
解题方法
4 .  时,相同物质的量浓度的下列溶液中,
时,相同物质的量浓度的下列溶液中, 最大的是
最大的是
 时,相同物质的量浓度的下列溶液中,
时,相同物质的量浓度的下列溶液中, 最大的是
最大的是| A.NH4Cl | B.CH3COONH4 | C.NH4HSO4 | D.NH4Al(SO4)2 |
您最近半年使用:0次
名校
解题方法
5 . 室温下,用FeSO4溶液制备FeCO3的过程如图所示。
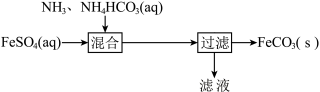
A.广泛 试纸测得 试纸测得 溶液的 溶液的 值应为7 值应为7 |
B.混合过程中,会发生反应: |
C.滤液中存在大量的: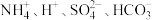 |
D. 溶液中: 溶液中: |
您最近半年使用:0次
名校
6 . 某温度下, 与不同pH的
与不同pH的 体系反应可生成不同的沉淀。下面图1表示
体系反应可生成不同的沉淀。下面图1表示 体系中各含碳粒子的物质的量分数与pH的关系。图2表示
体系中各含碳粒子的物质的量分数与pH的关系。图2表示 与不同pH的
与不同pH的 体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合
体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合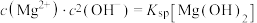 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合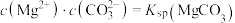 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。
 与不同pH的
与不同pH的 体系反应可生成不同的沉淀。下面图1表示
体系反应可生成不同的沉淀。下面图1表示 体系中各含碳粒子的物质的量分数与pH的关系。图2表示
体系中各含碳粒子的物质的量分数与pH的关系。图2表示 与不同pH的
与不同pH的 体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合
体系反应生成沉淀的情况,其中曲线Ⅰ的离子浓度关系符合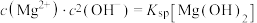 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合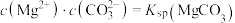 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。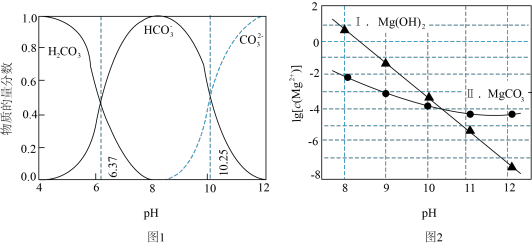
A.上述 体系呈中性时, 体系呈中性时,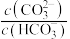 一定是 一定是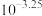 |
B.符合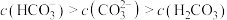 的pH范围: 的pH范围: |
C. , ,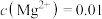 mol⋅L mol⋅L 时,溶液中存在 时,溶液中存在 和 和 两种沉淀 两种沉淀 |
D. , ,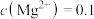 mol⋅L mol⋅L 时可发生反应: 时可发生反应: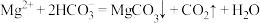 |
您最近半年使用:0次
7 . 草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX[X表示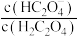 或
或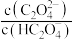 ]随pH的变化关系如图所示。下列说法不正确的是
]随pH的变化关系如图所示。下列说法不正确的是

A.Ⅰ中X表示的是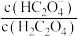 |
B.当溶液pH=4.19时,c(Na+)>3c( ) ) |
C.已知:25℃时,NH3∙H2O的电离常数为 ,则(NH4)2C2O4溶液呈酸性 ,则(NH4)2C2O4溶液呈酸性 |
D.0.1mol∙L-1NaHC2O4溶液中:c(Na+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近半年使用:0次
解题方法
8 . 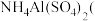 俗名铵明矾
俗名铵明矾 是食品加工中最为快捷的食品添加剂,常用于焙烤食品中;
是食品加工中最为快捷的食品添加剂,常用于焙烤食品中;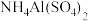 在分析试剂、医药、电子工业中用途广泛。下列有关叙述正确的是
在分析试剂、医药、电子工业中用途广泛。下列有关叙述正确的是
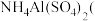 俗名铵明矾
俗名铵明矾 是食品加工中最为快捷的食品添加剂,常用于焙烤食品中;
是食品加工中最为快捷的食品添加剂,常用于焙烤食品中;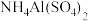 在分析试剂、医药、电子工业中用途广泛。下列有关叙述正确的是
在分析试剂、医药、电子工业中用途广泛。下列有关叙述正确的是A.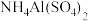 可做净水剂,其理由是水解产物可以杀菌消毒 可做净水剂,其理由是水解产物可以杀菌消毒 |
B.相同条件下,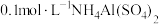 中 中 大于 大于 中 中 |
C.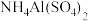 溶液中加入盐酸抑制水解,酸性减弱 溶液中加入盐酸抑制水解,酸性减弱 |
D. 时 时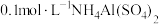 溶液的 溶液的 为 为 ,则溶液中 ,则溶液中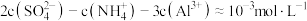 |
您最近半年使用:0次
9 . 下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中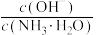 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近半年使用:0次
名校
解题方法
10 . 已知25℃时,几种弱酸的电离常数如下:
25℃时,下列说法正确的是
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数 |  |  | 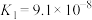 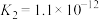 |
| A.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol/L |
| B.用0.1 mol/L的NaOH溶液滴定pH相等的CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液体积更大 |
C.NaHS和Na2S的混合溶液中,一定存在 |
| D.常温下,pH=4的CH3COOH和pH=10的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
您最近半年使用:0次



