1 . 黄铵铁矾 和
和 常用作净水剂。
常用作净水剂。
已知: 热分解过程发生的反应如下:
热分解过程发生的反应如下:
①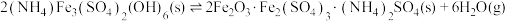
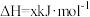
②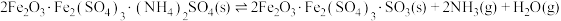
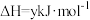
③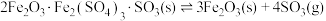
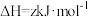
回答下列问题:
(1)基态 的M层电子排布式为
的M层电子排布式为_______ , 中N原子的
中N原子的_______ 轨道与H原子的s轨道重叠形成σ键。
(2) 的
的
_______  。
。
(3)一定温度下,在恒容密闭容器中加入一定量的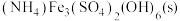 ,只发生反应:
,只发生反应: ,下列可判断该反应达到平衡状态的是_______(填序号)。
,下列可判断该反应达到平衡状态的是_______(填序号)。
(4)500℃时,在体积可变的密闭容器中加入一定量的 固体,只发生反应:
固体,只发生反应: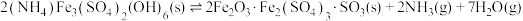 ,达到平衡时测得
,达到平衡时测得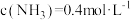 。保持温度不变,将容器体积变为原来的一半,达到新平衡时
。保持温度不变,将容器体积变为原来的一半,达到新平衡时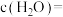
_______  。
。
(5)一定温度下,总压强恒定时,向体积可变的密闭容器中加入一定量的 和
和 氩气,仅发生反应②。测得平衡状态下
氩气,仅发生反应②。测得平衡状态下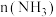 与
与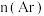 的关系如下图所示。随着通入的
的关系如下图所示。随着通入的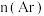 增大,
增大,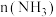 也增大的原因是
也增大的原因是_______ 。 的分解过程会发生下列反应:
的分解过程会发生下列反应:
主反应:

副反应:

两个反应的平衡常数比值 随反应温度升高而
随反应温度升高而_______ (填“增大”“减小”或“不变”);若平衡时总压为25kPa, 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
_______ 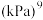 。
。
 和
和 常用作净水剂。
常用作净水剂。已知:
 热分解过程发生的反应如下:
热分解过程发生的反应如下:①
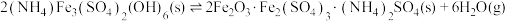
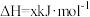
②
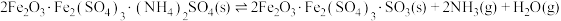
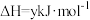
③
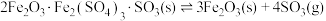
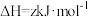
回答下列问题:
(1)基态
 的M层电子排布式为
的M层电子排布式为 中N原子的
中N原子的(2)
 的
的
 。
。(3)一定温度下,在恒容密闭容器中加入一定量的
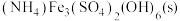 ,只发生反应:
,只发生反应: ,下列可判断该反应达到平衡状态的是_______(填序号)。
,下列可判断该反应达到平衡状态的是_______(填序号)。A. 质量不随时间变化 质量不随时间变化 | B. 体积分数不随时间变化 体积分数不随时间变化 |
| C.混合气体密度不随时间变化 | D.气体平均摩尔质量不随时间变化 |
(4)500℃时,在体积可变的密闭容器中加入一定量的
 固体,只发生反应:
固体,只发生反应: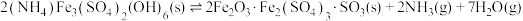 ,达到平衡时测得
,达到平衡时测得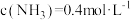 。保持温度不变,将容器体积变为原来的一半,达到新平衡时
。保持温度不变,将容器体积变为原来的一半,达到新平衡时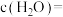
 。
。(5)一定温度下,总压强恒定时,向体积可变的密闭容器中加入一定量的
 和
和 氩气,仅发生反应②。测得平衡状态下
氩气,仅发生反应②。测得平衡状态下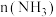 与
与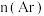 的关系如下图所示。随着通入的
的关系如下图所示。随着通入的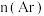 增大,
增大,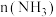 也增大的原因是
也增大的原因是
 的分解过程会发生下列反应:
的分解过程会发生下列反应:主反应:


副反应:


两个反应的平衡常数比值
 随反应温度升高而
随反应温度升高而 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
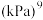 。
。
您最近半年使用:0次
7日内更新
|
16次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
2 . Ⅰ.硒(Se)是一种重要的化学元素,在医药、农业、能源和电子等领域有广泛应用。
(1)以下不能用元素周期律解释的是___________。
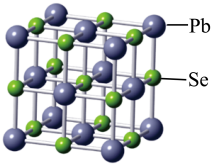
(2)硒化铅可用作玻璃和陶瓷的着色剂,其晶胞结构如图所示:___________ 。
A.离子键 B.共价键
②晶体中每个Se周围与其最近的,且距离相等的Se有___________ 个。
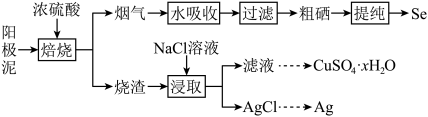
Ⅱ.工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、Ag2Se等)回收Se。
② 室温下Ksp(Ag2SO4)=10−5;Ksp(AgCl)=10−9.75。
(3)“焙烧”前,将阳极泥中大块颗粒粉碎的目的是___________ 。
(4)“烟气”中含有SO2和SeO2,被水吸收发生反应,SO2与和SeO2的物质的量之比为___________ ,SeO2体现了___________ 。
A.氧化性 B.还原性
(5)“提纯”步骤中用到真空蒸馏工艺,真空的作用是___________ 、___________ 。
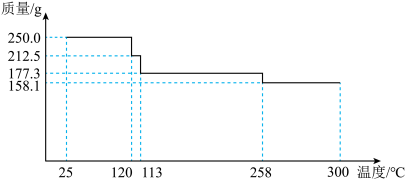
(6)小组同学测定某CuSO4∙xH2O晶体样品热分解的质量变化情况(如图所示),258℃失去全部结晶水,x=___________ 。(结果保留2位小数)___________ 。
Ⅲ.亚硒酸(H2SeO3)是主要的含硒化合物,是二元弱酸。常温下,H2SeO3溶液中某些微粒的物质的量分数与pH的关系如图所示:
(9)向滴有酚酞的H2SeO3溶液中加入氨水,当溶液由粉红色变为红色时,反应的离子方程式为___________ 。
(1)以下不能用元素周期律解释的是___________。
| A.键的极性:H−Se < H−Br | B.原子半径:Se > Br |
| C.稳定性:H2Se < HBr | D.酸性:H2SeO3 < HBrO4 |
(2)硒化铅可用作玻璃和陶瓷的着色剂,其晶胞结构如图所示:
A.离子键 B.共价键
②晶体中每个Se周围与其最近的,且距离相等的Se有
Ⅱ.工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、Ag2Se等)回收Se。
② 室温下Ksp(Ag2SO4)=10−5;Ksp(AgCl)=10−9.75。
(3)“焙烧”前,将阳极泥中大块颗粒粉碎的目的是
(4)“烟气”中含有SO2和SeO2,被水吸收发生反应,SO2与和SeO2的物质的量之比为
A.氧化性 B.还原性
(5)“提纯”步骤中用到真空蒸馏工艺,真空的作用是
(6)小组同学测定某CuSO4∙xH2O晶体样品热分解的质量变化情况(如图所示),258℃失去全部结晶水,x=
Ⅲ.亚硒酸(H2SeO3)是主要的含硒化合物,是二元弱酸。常温下,H2SeO3溶液中某些微粒的物质的量分数与pH的关系如图所示:
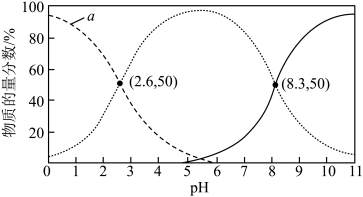
A.曲线a表示的是SeO 物质的量分数随pH变化 物质的量分数随pH变化 |
| B.Ka1=10−5.5 |
C.pH=3时, =100.4 =100.4 |
D.向H2SeO3溶液中逐滴加入NaOH溶液,pH=8.3时溶液中存在:2c(Na+)=3[c(HSeO )+ c(SeO )+ c(SeO )+ c(H2SeO3)] )+ c(H2SeO3)] |
(9)向滴有酚酞的H2SeO3溶液中加入氨水,当溶液由粉红色变为红色时,反应的离子方程式为
您最近半年使用:0次
解题方法
3 . 联氨(N2H4)又称肼,在航天、能源等领域具有广泛应用。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。___________
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
(3)酸碱质子理论提出:凡是能给出质子的分子或离子称为酸,凡是能接受质子的分子或离子称为碱。
①由N2H4+H2O N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是___________ 。
A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为___________ 。
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是___________ 。
②N2H4和N2O4作为火箭推进剂的主要原因是___________ 。
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是_______ 。
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平_______ 。
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O
当转移7.224×1024个电子数时,生成金属钴___________ 克。
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是___________ 。
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有___________ 。
Ⅰ.N2H4分子中所有原子均达到稀有气体原子的稳定结构。
(1)写出N2H4的电子式。
(2)N2H4晶体受热熔化时,破坏的作用力有___________。
| A.范德华力 | B.氢键 | C.共价键 | D.离子键 |
①由N2H4+H2O
 N2H
N2H +OH- 可知N2H4是
+OH- 可知N2H4是A.酸 B.碱
②选择足量的盐酸或NaOH溶液与N2H4充分反应,生成盐的化学式为
Ⅱ.肼具有强还原性,可作火箭推进剂燃料,反应的热化学方程式表示为:2N2H4(l)+N2O4(g)=3N2(g)+4H2O(g) ∆H<0。
(4)①结合化学反应原理分析,该反应可自发进行的原因是
②N2H4和N2O4作为火箭推进剂的主要原因是
Ⅲ.肼可还原钴离子制备纳米金属钴,纳米金属钴具有特殊的物理、化学和表面性质。
(5)下列状态的钴中,电离最外层一个电子所需能量最小的是
A.[Ar]3d74s2 B.[Ar]3d74s14p1 C.[Ar]3d74s1
(6)Co2+被N2H4还原的离子方程式如下,完成方程式并配平
 Co2++
Co2++ N2H4+
N2H4+ ___________=
___________= Co↓+
Co↓+ N2↑+
N2↑+ H2O
H2O当转移7.224×1024个电子数时,生成金属钴
(7)金属钴可以形成多种配合物。一种配合物由Co3+、NH3、Cl-、H2O组成,实验显示Co3+、NH3、Cl-、H2O的物质的量之比为1∶3∶3∶1.向该配合物的水溶液加入AgNO3溶液,只能沉淀出三分之一的Cl-。
①该配合物的化学式是
A.[Co(NH3)3ClH2O]Cl2 B.[Co(NH3)3Cl2H2O]Cl C.[Co(NH3)3H2O]Cl3
②该配合物的配体有
您最近半年使用:0次
名校
解题方法
4 . “建设生态文明是中华民族永续发展的千年大计。”控制和治理 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_______ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下:
 、
、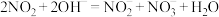
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成_______ mol 。
。
③在100mL稀 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为_______ (反应前后溶液体积变化忽略不计)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 和
和 ,其离子方程式为
,其离子方程式为_______ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是_______ 。
(4)吸收工厂烟气中的 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。
①富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除:_______ 。
②氨水吸收 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为_______ 。
已知:溶液中 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下: 、
、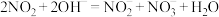
①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、
 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成 。
。③在100mL稀
 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。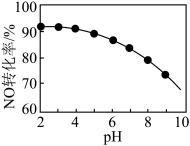
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(4)吸收工厂烟气中的
 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。①富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除: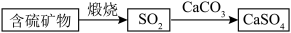
②氨水吸收
 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为已知:溶液中
 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。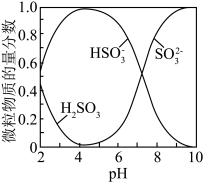
您最近半年使用:0次
名校
解题方法
5 . 已知 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:
(1)根据在 时,用蒸馏水稀释
时,用蒸馏水稀释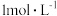 的醋酸溶液至
的醋酸溶液至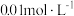 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
(2)常温下,同浓度的下列物质的水溶液 最小的是_____。(单选)
最小的是_____。(单选)
(3)常温下,下列操作(忽略过程中温度变化)可以使亚硫酸稀溶液中的 增大的是_____。(单选)
增大的是_____。(单选)
(4)下列关于 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)
(5)向 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式_____ 。
(6)含镉 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理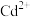 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:_____ ,此时该反应的化学平衡常数为_____ 。
 时,部分电解质的电离常数如下表所示:
时,部分电解质的电离常数如下表所示:| 电解质 |  | 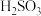 |
| 电离常数 | 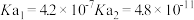 | 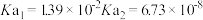 |
| 电解质 | 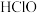 |  |
| 电离常数 |  | 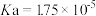 |
 时,用蒸馏水稀释
时,用蒸馏水稀释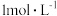 的醋酸溶液至
的醋酸溶液至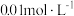 ,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)
,随着溶液的稀释,下列各项中始终保持增大趋势的是_____。(单选)A. | B.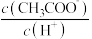 |
C.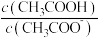 | D. |
 最小的是_____。(单选)
最小的是_____。(单选)A.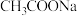 | B. | C. | D. |
 增大的是_____。(单选)
增大的是_____。(单选)A.通入 气体 气体 | B.通入 气体 气体 | C.加入 固体 固体 | D.加入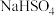 固体 固体 |
 溶液中微粒关系错误的是_____。(不定项)
溶液中微粒关系错误的是_____。(不定项)A.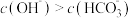 |
B.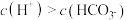 |
C. |
D.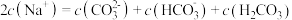 |
 溶液中通入少量
溶液中通入少量 ,写出反应的离子方程式
,写出反应的离子方程式(6)含镉
 废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下,
废水是危害严重的重金属离子废水,处理含镉废水常采用化学沉淀法。常温下, 、
、 。若用
。若用 处理
处理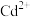 实现沉淀转化,写出反应的离子方程式:
实现沉淀转化,写出反应的离子方程式:
您最近半年使用:0次
6 . 异丁烯是一种重要的化工原料,主要用于制备甲基叔丁基醚、丁基橡胶、甲基丙烯腈等。将异丁烷脱氢制备异丁烯,可提高异丁烷的附加值,具有良好的经济与社会效益。回答下列问题。
(1)利用下列燃烧热数据,计算异丁烷直接脱氢生成异丁烯反应的∆H:
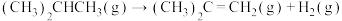 ∆H=
∆H=____________ kJ·mol-1。
(2)在恒温853K、恒压100kPa条件下,初始反应气体组成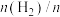 (异丁烷)或
(异丁烷)或 (异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
(异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。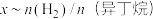 为曲线
为曲线_________ (填“M”或“N”),催化剂易被副反应产生的加聚产物__________ (填写结构简式)影响而失活。
(3)有人提出在恒温恒压条件下加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯。比较异丁烷直接脱氢制备异丁烯,从平衡产率角度分析该方法的优点是_____________ ,若生产过程中加入的空气过多,产生的主要问题是_____________ 。
(4)有人提出加入适量CO2,采用MgFe2O4催化CO2氧化异丁烷脱氢的方法制备异丁烯。催化过程中,反应物异丁烷、CO2先各自被催化剂上的不同位点吸附。催化剂中电负性较大的金属_____________ (填元素符号)是酸性位点;而电负性较小的金属是碱性位点,吸附________________ (填“异丁烷”或“CO2”)。
(1)利用下列燃烧热数据,计算异丁烷直接脱氢生成异丁烯反应的∆H:
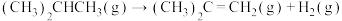 ∆H=
∆H=| 物质 | 异丁烷(g) | 异丁烯(g) | 氢气(g) |
| 燃烧热/(kJ·mol-1) | 2868 | 2700 | 286 |
(2)在恒温853K、恒压100kPa条件下,初始反应气体组成
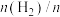 (异丁烷)或
(异丁烷)或 (异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
(异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
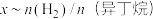 为曲线
为曲线(3)有人提出在恒温恒压条件下加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯。比较异丁烷直接脱氢制备异丁烯,从平衡产率角度分析该方法的优点是
(4)有人提出加入适量CO2,采用MgFe2O4催化CO2氧化异丁烷脱氢的方法制备异丁烯。催化过程中,反应物异丁烷、CO2先各自被催化剂上的不同位点吸附。催化剂中电负性较大的金属
您最近半年使用:0次
名校
解题方法
7 . 目前,处理烟气中 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。
I.碱液吸收法
已知常温下:
第一步:用过量的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第二步:加入石灰水,发生反应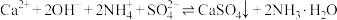 K。
K。
(1)25℃时,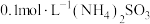 溶液的pH
溶液的pH___________ 7(填“>”“<”或“=”),并说明理由:___________ 。在该溶液中: ___________
___________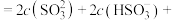 ___________。
___________。___________
(2)0.1mol/L下列溶液中,溶液中 由大到小的顺序是
由大到小的顺序是___________ 。
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为 ,该过程中溶液pH
,该过程中溶液pH___________ (填“升高”“不变”或“降低”)。
(4)计算第二步中反应的K=___________ 。
(5)测定一定浓度的 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
(6)用过量的 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:___________ 。
Ⅱ.水煤气还原法
已知:①
 ;
;
②
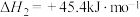 ;
;
③CO的燃烧热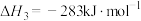 。
。
(7)表示液态硫的燃烧热的热化学方程式为___________ 。
(8)反应②中,正反应活化能
___________ (填“>”“<”或“=”) 。
。
(9)在一定压强下,发生反应①。平衡时 的转化率
的转化率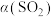 与投料比的比值
与投料比的比值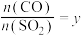 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N___________ M(填“>”“<”或“=”,下同)。逆反应速率N___________ P。 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。
①该温度下,反应②的平衡常数K为___________ 。(填数值)
②其他条件不变,在第7min时缩小容器体积,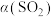
___________ (填“增大”“减小”或“不变”)。
 常采用两种方法:碱液吸收法和还原法。
常采用两种方法:碱液吸收法和还原法。I.碱液吸收法
已知常温下:
 |  |  |  |
 | 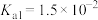  |  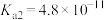 | 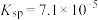 |
 ,并在空气中氧化;
,并在空气中氧化;第二步:加入石灰水,发生反应
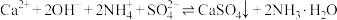 K。
K。(1)25℃时,
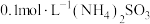 溶液的pH
溶液的pH ___________
___________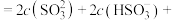 ___________。
___________。(2)0.1mol/L下列溶液中,溶液中
 由大到小的顺序是
由大到小的顺序是①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
(3)第一步氧化的目的是将硫元素全部转化为
 ,该过程中溶液pH
,该过程中溶液pH(4)计算第二步中反应的K=
(5)测定一定浓度的
 溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。
溶液pH与温度的关系曲线如图所示,下列分析错误的是___________。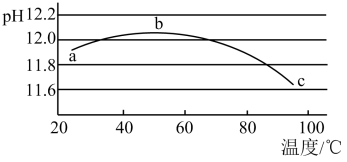
| A.c点水解程度最大 | B.水解是吸热过程 |
| C.a→b段水解平衡向右移动 | D.b点溶液中的 最大 最大 |
(6)用过量的
 溶液吸收
溶液吸收 的离子方程式:
的离子方程式:Ⅱ.水煤气还原法
已知:①

 ;
;②

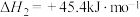 ;
;③CO的燃烧热
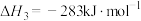 。
。(7)表示液态硫的燃烧热的热化学方程式为
(8)反应②中,正反应活化能

 。
。(9)在一定压强下,发生反应①。平衡时
 的转化率
的转化率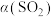 与投料比的比值
与投料比的比值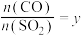 、温度T的关系如图所示。比较平衡时CO的转化率
、温度T的关系如图所示。比较平衡时CO的转化率 :N
:N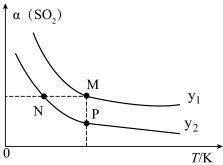
 、2molCO和
、2molCO和 发生反应①、②,第5min时达到平衡,测得混合气体中
发生反应①、②,第5min时达到平衡,测得混合气体中 、
、 的物质的量分别为1.6mol、1.8mol。
的物质的量分别为1.6mol、1.8mol。①该温度下,反应②的平衡常数K为
②其他条件不变,在第7min时缩小容器体积,
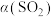
您最近半年使用:0次
名校
解题方法
8 .  是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
(1)已知:①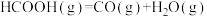
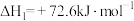
②
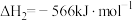
③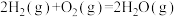
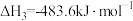
则 的
的
_______  。
。
(2)恒温恒容条件下,向密闭容器中充入1
 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。
(3)一定温度下,保持总压强为2.0 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性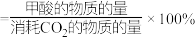 。该温度下,
。该温度下, 的平衡常数
的平衡常数
_______  。
。
(4)常温下,向 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
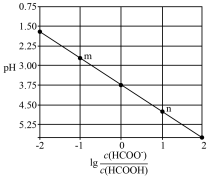
则
_______ ,n点溶液中离子浓度由大到小的排序为_______ 。
(5)常温下,已知 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中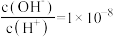 。
。
①
 的
的
_______ 。
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是_______ (填序号)
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的
C.稀释后甲酸的电离度会增大
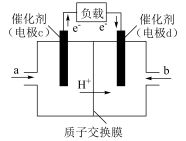
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是_______ (填“正极”或“负极”),c电极的电极反应式为_______ 。
 是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:(1)已知:①
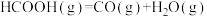
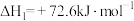
②

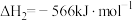
③
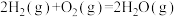
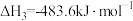
则
 的
的
 。
。(2)恒温恒容条件下,向密闭容器中充入1

 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。| A.气体压强不随时间变化时达到平衡状态 |
B.平衡时 的最大体积分数为50% 的最大体积分数为50% |
C.平衡后及时移走 ,平衡常数增大 ,平衡常数增大 |
D.平衡后再充入 , , 的平衡转化率增大 的平衡转化率增大 |
(3)一定温度下,保持总压强为2.0
 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性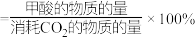 。该温度下,
。该温度下, 的平衡常数
的平衡常数
 。
。(4)常温下,向
 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
则

(5)常温下,已知
 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中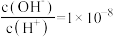 。
。①

 的
的
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的

C.稀释后甲酸的电离度会增大
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是

您最近半年使用:0次
解题方法
9 . 为防止氮的氧化物污染空气,可用甲烷或氢气还原氮氧化物。
(1)利用甲烷可将氮氧化物还原为氮气除去。已知:
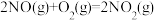
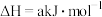

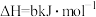
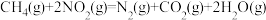

①已知反应中相关化学键的键能数据如下:
则b=___________ 。
②反应

___________  。(用a、b、c表示)
。(用a、b、c表示)
(2)消除NO污染物,在一定条件下,用 将NO还原为
将NO还原为 和
和 (g)。
(g)。
① 还原NO的总反应为
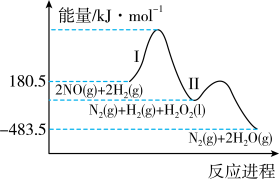
还原NO的总反应为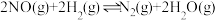 ,其能量变化如图所示。每还原1mol NO,总反应的能量变化为
,其能量变化如图所示。每还原1mol NO,总反应的能量变化为___________ 。
②研究表明上述反应历程分两步:
I. ;
;
Ⅱ.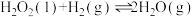 。
。
该总反应的速率由反应___________ (填“I”或“Ⅱ”)决定。
③为提高此反应的速率,下列措施可行的是___________ (填字母代号)。
A.升高温度 B.增加 浓度 C.使用适合催化剂 D.移出
浓度 C.使用适合催化剂 D.移出
(1)利用甲烷可将氮氧化物还原为氮气除去。已知:
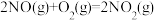
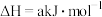

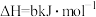
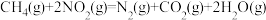

①已知反应中相关化学键的键能数据如下:
| 化学键 | C-H | O=O | C=O | O-H |
E/( ) ) | 411 | 494 | 800 | 460 |
②反应


 。(用a、b、c表示)
。(用a、b、c表示)(2)消除NO污染物,在一定条件下,用
 将NO还原为
将NO还原为 和
和 (g)。
(g)。①
 还原NO的总反应为
还原NO的总反应为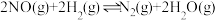 ,其能量变化如图所示。每还原1mol NO,总反应的能量变化为
,其能量变化如图所示。每还原1mol NO,总反应的能量变化为
②研究表明上述反应历程分两步:
I.
 ;
;Ⅱ.
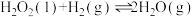 。
。该总反应的速率由反应
③为提高此反应的速率,下列措施可行的是
A.升高温度 B.增加
 浓度 C.使用适合催化剂 D.移出
浓度 C.使用适合催化剂 D.移出
您最近半年使用:0次
解题方法
10 . 科研工作者持续进行“碳达峰”“碳中和”的相关研究。根据要求回答下列问题。
Ⅰ.石灰生产工业利用开采的碳酸钙进行分解,并产生大量 ,主要反应如下:
,主要反应如下: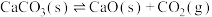
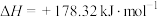
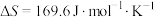 ①
①
(1)已知ΔG=0时的临界温度称为热力学分解温度,反应①的分解温度为___________ ℃。(保留整数位)
(2)恒温恒压体系内进行反应①,达到平衡后,分别进行如下操作,请填空:
操作1:加入 ,平衡
,平衡___________ (填“正向”“逆向”或“不”,下同)移动;
操作2:缓慢加入 ,平衡
,平衡___________ 移动。
Ⅱ. 和
和 占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将
占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将 和
和 这两种温室气体转化为合成气(CO和
这两种温室气体转化为合成气(CO和 )。
)。
主反应为 ②
②
副反应主要有 ③
③
 ④
④
Co基活性中心在甲烷二氧化碳重整过程有较好的反应活性,其中吸附在催化剂表面的物质用*标注。催化反应机理如下图:

(3)写出催化过程中步骤B的反应方程式:___________ ,该过程为___________ (填“放热”或“吸热”)反应。
(4)路径1和路径2同时进行,容易发生碳耦合过程最终导致积碳,使催化剂失活。根据反应机理推测可能发生的积碳反应除反应③外,还有可能的积碳反应为有___________ (填反应方程式)。
(5)相同条件下按甲烷、二氧化碳、氮气体积比为45%、45%、10%的量进行催化重整反应,若发生②③④三个反应,已知甲烷的转化率为70%, 的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=
的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=___________ [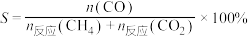 ,生成的C理论上都附着在催化剂表面]。
,生成的C理论上都附着在催化剂表面]。
Ⅰ.石灰生产工业利用开采的碳酸钙进行分解,并产生大量
 ,主要反应如下:
,主要反应如下: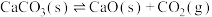
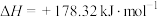
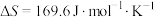 ①
①(1)已知ΔG=0时的临界温度称为热力学分解温度,反应①的分解温度为
(2)恒温恒压体系内进行反应①,达到平衡后,分别进行如下操作,请填空:
操作1:加入
 ,平衡
,平衡操作2:缓慢加入
 ,平衡
,平衡Ⅱ.
 和
和 占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将
占温室气体排放的98%以上。甲烷二氧化碳重整反应可在低温条件下将 和
和 这两种温室气体转化为合成气(CO和
这两种温室气体转化为合成气(CO和 )。
)。主反应为
 ②
②副反应主要有
 ③
③ ④
④Co基活性中心在甲烷二氧化碳重整过程有较好的反应活性,其中吸附在催化剂表面的物质用*标注。催化反应机理如下图:

(3)写出催化过程中步骤B的反应方程式:
(4)路径1和路径2同时进行,容易发生碳耦合过程最终导致积碳,使催化剂失活。根据反应机理推测可能发生的积碳反应除反应③外,还有可能的积碳反应为有
(5)相同条件下按甲烷、二氧化碳、氮气体积比为45%、45%、10%的量进行催化重整反应,若发生②③④三个反应,已知甲烷的转化率为70%,
 的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=
的转化率为80%,附着在催化剂表面的积碳占总碳元素的24%,则CO的选择性S=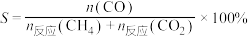 ,生成的C理论上都附着在催化剂表面]。
,生成的C理论上都附着在催化剂表面]。
您最近半年使用:0次



