2024高三下·全国·专题练习
解题方法
1 . 某研究小组用磷酸和碳酸钠制备NaH2PO4·2H2O,按如下流程开展实验。
一系列操作包括:操作A、洗涤和干燥。
(1)写出操作A的名称___________ 。
(2)洗涤时,下列洗涤剂最合适的是___________(填序号)。

一系列操作包括:操作A、洗涤和干燥。
(1)写出操作A的名称
(2)洗涤时,下列洗涤剂最合适的是___________(填序号)。
| A.冷水 | B.热水 | C.乙醇 | D.乙醇-水混合溶液 |
您最近半年使用:0次
2024高三下·全国·专题练习
2 . 学习小组利用废银催化剂制备乙炔银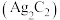 和酸性乙炔银
和酸性乙炔银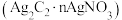 。已知乙炔银和酸性乙炔银在受热时均易发生分解。
。已知乙炔银和酸性乙炔银在受热时均易发生分解。
①制取乙炔。利用如图装置制取纯净的乙炔。 的溶液中通入乙炔可得到乙炔银沉淀。
的溶液中通入乙炔可得到乙炔银沉淀。
(1)将过滤所得滤渣置于小烧杯中,利用丙酮反复多次冲洗沉淀。检验滤渣已经洗净的实验方案是_______ 。
(2)准确称取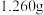 样品,用浓硝酸完全溶解后,定容得
样品,用浓硝酸完全溶解后,定容得 溶液,取
溶液,取 于锥形瓶中,以
于锥形瓶中,以 作指示剂,用
作指示剂,用 标准溶液进行滴定
标准溶液进行滴定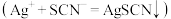 ,终点时消耗标准溶液的体积为
,终点时消耗标准溶液的体积为 。
。
滴定终点的现象为_______ 。通过计算确定n的数值_______ (写出计算过程)。
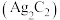 和酸性乙炔银
和酸性乙炔银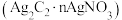 。已知乙炔银和酸性乙炔银在受热时均易发生分解。
。已知乙炔银和酸性乙炔银在受热时均易发生分解。①制取乙炔。利用如图装置制取纯净的乙炔。
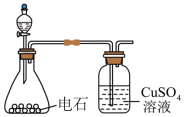
 的溶液中通入乙炔可得到乙炔银沉淀。
的溶液中通入乙炔可得到乙炔银沉淀。(1)将过滤所得滤渣置于小烧杯中,利用丙酮反复多次冲洗沉淀。检验滤渣已经洗净的实验方案是
(2)准确称取
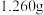 样品,用浓硝酸完全溶解后,定容得
样品,用浓硝酸完全溶解后,定容得 溶液,取
溶液,取 于锥形瓶中,以
于锥形瓶中,以 作指示剂,用
作指示剂,用 标准溶液进行滴定
标准溶液进行滴定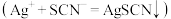 ,终点时消耗标准溶液的体积为
,终点时消耗标准溶液的体积为 。
。滴定终点的现象为
您最近半年使用:0次
2024高三下·全国·专题练习
3 .  作为绿色氧化剂应用广泛,氢醌法制备
作为绿色氧化剂应用广泛,氢醌法制备 原理及装置如下:
原理及装置如下: 、
、 等杂质易使
等杂质易使 催化剂中毒。回答下列问题:
催化剂中毒。回答下列问题:
(1)取 产品,加蒸馏水定容至
产品,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、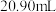 、
、 。假设其他杂质不干扰结果,产品中
。假设其他杂质不干扰结果,产品中 质量分数为
质量分数为_______ 。
 作为绿色氧化剂应用广泛,氢醌法制备
作为绿色氧化剂应用广泛,氢醌法制备 原理及装置如下:
原理及装置如下: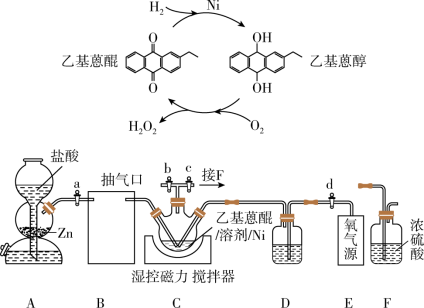
 、
、 等杂质易使
等杂质易使 催化剂中毒。回答下列问题:
催化剂中毒。回答下列问题:(1)取
 产品,加蒸馏水定容至
产品,加蒸馏水定容至 摇匀,取
摇匀,取 于锥形瓶中,用
于锥形瓶中,用 酸性
酸性 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为 、
、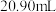 、
、 。假设其他杂质不干扰结果,产品中
。假设其他杂质不干扰结果,产品中 质量分数为
质量分数为
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
4 . CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水,稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4反应的化学方程式为:CuCl(s)+3HCl(aq) H3CuCl4(aq)。
H3CuCl4(aq)。
2Cu2++SO2+8Cl−+2H2O=2CuCl43−+SO42−+4H+
CuCl43−(aq)
 CuCl(s)+3Cl-(aq)
CuCl(s)+3Cl-(aq)
A.稀硫酸B.98%的硫酸C.65%的硫酸
(2)装置B中反应结束后,取出混合物进行如下图所示操作,得到CuCl晶体。

您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
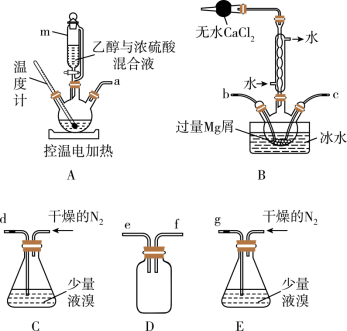
5 . 无水溴化镁常常做催化剂。选用如图所示装置(夹持装置略)采用镁屑与液溴为原料制备无水MgBr2。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是_______ 。
(2)装置A中使用仪器m的优点是_______ 。
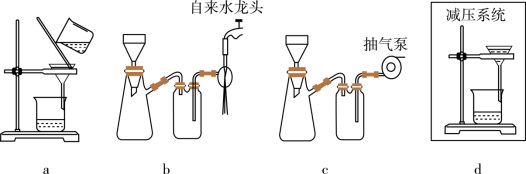
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是_______ (填序号)。_______ 。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是
(2)装置A中使用仪器m的优点是
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
6 . 某实验小组以 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
可选用试剂: 晶体、
晶体、 溶液、浓
溶液、浓 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水
步骤1. 的制备
的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。 的含量测定
的含量测定
①称取产品 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的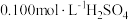 溶液,
溶液,
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为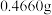 。
。
回答下列问题:
(1)在沉淀过程中,某同学在加入一定量热的 溶液后,认为沉淀已经完全,判断沉淀已完全的方法是
溶液后,认为沉淀已经完全,判断沉淀已完全的方法是_______ ;
 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:可选用试剂:
 晶体、
晶体、 溶液、浓
溶液、浓 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水步骤1.
 的制备
的制备按如图所示装置进行实验,得到
 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。
 的含量测定
的含量测定①称取产品
 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;②在不断搅拌下,向①所得溶液逐滴加入热的
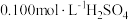 溶液,
溶液,③沉淀完全后,
 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为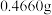 。
。回答下列问题:
(1)在沉淀过程中,某同学在加入一定量热的
 溶液后,认为沉淀已经完全,判断沉淀已完全的方法是
溶液后,认为沉淀已经完全,判断沉淀已完全的方法是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
7 .  是制备钛及其化合物的重要中间体,实验室以
是制备钛及其化合物的重要中间体,实验室以 和
和 为原料制取液态
为原料制取液态 的装置如图所示(部分夹持装置省略)。
的装置如图所示(部分夹持装置省略)。
回答下列问题:
(1)补充并分析实验步骤:①连接好装置,_______ ;②向各装置中加入药品,重新连接好装置,拧开装置A中分液漏斗活塞,缓慢加入稀硫酸,待装置G中出现白色沉淀后,关闭分液漏斗活塞;③向C中注入热水并点燃D处酒精灯……(后续步骤略)。步骤②的作用是_______ 。
(2)从E处混合物中分离出 的实验方法是_______ (填编号);
的实验方法是_______ (填编号);
 是制备钛及其化合物的重要中间体,实验室以
是制备钛及其化合物的重要中间体,实验室以 和
和 为原料制取液态
为原料制取液态 的装置如图所示(部分夹持装置省略)。
的装置如图所示(部分夹持装置省略)。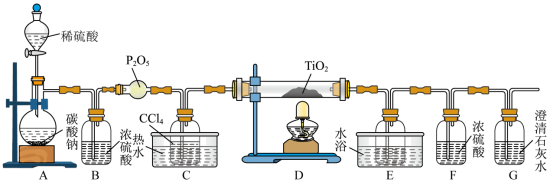
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
 | -23 | 76 | 与 互溶 互溶 |
 | -25 | 136 | 遇水极易水解,在550℃时能被氧气氧化 |
(1)补充并分析实验步骤:①连接好装置,
(2)从E处混合物中分离出
 的实验方法是_______ (填编号);
的实验方法是_______ (填编号);| A.过滤 | B.蒸发 | C.蒸馏 | D.分液 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
8 . 氯化铁是重要的化工原料。针对氯化铁的实验室制备方法,回答下列问题:
Ⅰ. 的制备
的制备
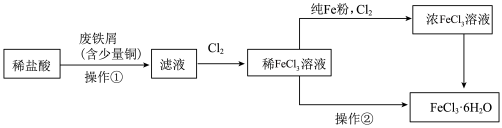
制备流程图如下: 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是_______ 。
(2)为增大 溶液的浓度,向稀
溶液的浓度,向稀 溶液中加入纯Fe粉后通入
溶液中加入纯Fe粉后通入 。此过程中发生的主要反应的离子方程式为
。此过程中发生的主要反应的离子方程式为_______ 。
(3)操作②为_______ 。
Ⅱ.由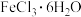 制备无水
制备无水
将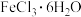 与液体
与液体 混合并加热,制得无水
混合并加热,制得无水 。已知
。已知 沸点为77℃,反应方程式为:
沸点为77℃,反应方程式为: ,装置如下图所示(夹持和加热装置略)。
,装置如下图所示(夹持和加热装置略)。 不能换成碱石灰,原因是
不能换成碱石灰,原因是_______ 。
Ⅰ.
 的制备
的制备制备流程图如下:
 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是(2)为增大
 溶液的浓度,向稀
溶液的浓度,向稀 溶液中加入纯Fe粉后通入
溶液中加入纯Fe粉后通入 。此过程中发生的主要反应的离子方程式为
。此过程中发生的主要反应的离子方程式为(3)操作②为
Ⅱ.由
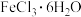 制备无水
制备无水
将
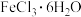 与液体
与液体 混合并加热,制得无水
混合并加热,制得无水 。已知
。已知 沸点为77℃,反应方程式为:
沸点为77℃,反应方程式为: ,装置如下图所示(夹持和加热装置略)。
,装置如下图所示(夹持和加热装置略)。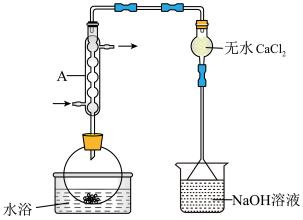
 不能换成碱石灰,原因是
不能换成碱石灰,原因是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 某研究小组以 为原料制备新型耐热材料
为原料制备新型耐热材料 。
。
步骤一: 水解制备
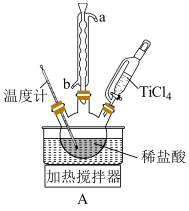
水解制备 (实验装置如图A,夹持装置省略):滴入
(实验装置如图A,夹持装置省略):滴入 ,边搅拌边加热,使混合液升温至
,边搅拌边加热,使混合液升温至 ,保温3小时。离心分离白色沉淀
,保温3小时。离心分离白色沉淀 并洗涤,煅烧制得
并洗涤,煅烧制得 。
。 水解生成的胶体主要成分为
水解生成的胶体主要成分为_______ (填化学式)。
(2)判断 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有_______ 。
步骤二:由 制备
制备 并测定产率(实验装置如下图,夹持装置省略)。
并测定产率(实验装置如下图,夹持装置省略)。_______ 。
 为原料制备新型耐热材料
为原料制备新型耐热材料 。
。步骤一:
 水解制备
水解制备 (实验装置如图A,夹持装置省略):滴入
(实验装置如图A,夹持装置省略):滴入 ,边搅拌边加热,使混合液升温至
,边搅拌边加热,使混合液升温至 ,保温3小时。离心分离白色沉淀
,保温3小时。离心分离白色沉淀 并洗涤,煅烧制得
并洗涤,煅烧制得 。
。
 水解生成的胶体主要成分为
水解生成的胶体主要成分为(2)判断
 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有步骤二:由
 制备
制备 并测定产率(实验装置如下图,夹持装置省略)。
并测定产率(实验装置如下图,夹持装置省略)。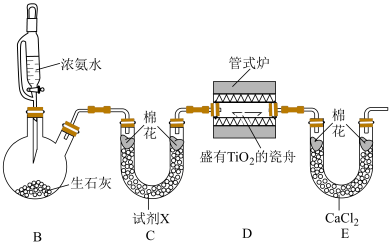
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 纯ClO2遇热易发生分解,工业上通常制成NaClO2固体以便运输和储存。制备NaClO2的实验装置如图所示(夹持装置省略),其中A装置制备ClO2,C装置用于制备NaClO2。回答下列问题:_______ 。
(2)装置A中发生反应的离子方程式为_______ 。向装置A中通入空气的目的是_______ 。
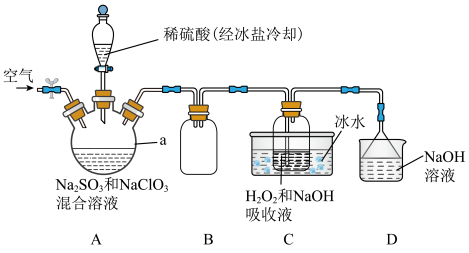
(2)装置A中发生反应的离子方程式为
您最近半年使用:0次



