解题方法
1 . M、N、P、Q、R是原子序数依次增大的前四周期主族元素,组成的化合物R4N(PM4)4Q2是某种荧光粉中的成分。M的一种单质是极性分子,N基态原子核外无未成对电子,P元素存在于航空、信息和新能源等高技术领域必需的材料中,Q是一种重要的成盐元素。下列说法错误的是
| A.N、Q、R三种元素简单离子的半径:Q>R>N |
| B.N、P、Q、R四种元素的第一电离能:Q>P>N>R |
C.M元素与氢元素形成的两种微粒的键角: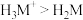 |
| D.N、P、R三种氧化物的熔点:P>R>N |
您最近半年使用:0次
名校
解题方法
2 . 下列关于微粒间的作用力说法正确的个数为
①所有金属与所有非金属之间都能形成离子键
②金属的导电性、延展性均与金属键有关
③金属晶体的熔沸点一定高于分子晶体
④晶体的熔沸点:金刚石>SiC>Si
⑤ 中的N—H键成键原理完全相同
中的N—H键成键原理完全相同
⑥分子晶体中共价键的键能越大,晶体的熔点和沸点越高
⑦离子键的强弱:NaF>NaCl>NaBr>NaI
①所有金属与所有非金属之间都能形成离子键
②金属的导电性、延展性均与金属键有关
③金属晶体的熔沸点一定高于分子晶体
④晶体的熔沸点:金刚石>SiC>Si
⑤
 中的N—H键成键原理完全相同
中的N—H键成键原理完全相同⑥分子晶体中共价键的键能越大,晶体的熔点和沸点越高
⑦离子键的强弱:NaF>NaCl>NaBr>NaI
⑧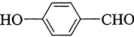 比
比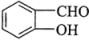 熔沸点高
熔沸点高
| A.4 | B.5 | C.6 | D.7 |
您最近半年使用:0次
名校
解题方法
3 . 硅微粒非常坚硬,比较晶体硅与碳化硅的熔点高低并解释说明___________ 。
您最近半年使用:0次
名校
解题方法
4 . 下图是MnS晶胞,其与NaCl晶胞属于同种类型。前者的熔点明显高于后者,其主要原因是___________ ;每个晶胞中平均分摊___________ 个S2-。
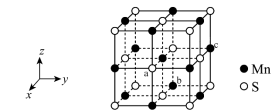
您最近半年使用:0次
解题方法
5 . 下列物质性质和原理分析相匹配的是
| 选项 | 物质性质 | 原理分析 |
| A | 冰醋酸不导电,醋酸溶液能导电 | 冰醋酸中没有能自由移动的离子 醋酸溶液中有能自由移动的离子 |
| B |  的酸性比 的酸性比 的强 的强 |  的摩尔质量小于 的摩尔质量小于 |
| C | 甲酸的沸点高于二甲醚 | 甲酸的范德华力大于二甲醚 |
| D | 油漆易溶于甲苯,不溶于水 | 甲苯是非极性溶剂,水是极性溶剂 油漆是极性大的物质 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 物质的结构决定其性质。下列实例与解释不相符的是
选项 | 实例 | 解释 |
A | NH3比PH3易液化 | NH3分子间能形成氢键 |
B | 三氟乙酸的酸性大于三氯乙酸 | 三氯乙酸分子间作用力较大 |
C | Al的硬度大于Mg | Al原子价电子数多,半径小 |
D | Br2在CCl4中的溶解度大于在H2O中的 | Br2、CCl4为非极性分子,H2O为极性分子 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 氯亚铂酸钾( )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(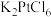 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:
Ⅰ.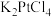 的制备
的制备
取10.00g氯铂酸钾(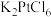 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原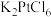 可得
可得 。
。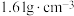 ,其物质的量浓度为
,其物质的量浓度为_____  。
。
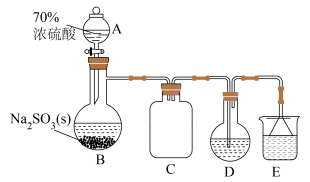
(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为_____ 。
(3)仪器B的名称为_____ ,装置C的作用是_____ 。
(4)装置D中反应的化学方程式为_____ ,装置E中的试剂可选用_____ (填序号)。
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是_____ 。
②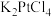 的产率为
的产率为_____ (结果保留三位有效数字)。_____ 。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是_____ 。
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(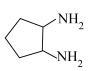 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是_____ 。
 )是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(
)是制备奥铂等抗肿瘤药物的重要中间体。某科研小组以氯铂酸钾(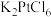 )为原料制备
)为原料制备 ,相关物质性质如下表:
,相关物质性质如下表:| 物质 | 性质 |
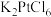 | 黄色粉末,溶于热水,微溶于冷水,几乎不溶于乙醇 |
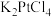 | 红色固体,溶于水,不溶于乙醇,高温易分解 |
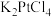 的制备
的制备取10.00g氯铂酸钾(
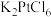 )溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原
)溶于热水,置于装置D中,按下图所示组装实验仪器(加热与夹持装置均已省略),在加热条件下还原 可得
可得 。
。
 ,其物质的量浓度为
,其物质的量浓度为 。
。(2)为使仪器A中的浓硫酸顺利滴下,需进行的操作为
(3)仪器B的名称为
(4)装置D中反应的化学方程式为
A.氨水 B.NaOH溶液 C.澄清石灰水
(5)反应结束后,拆除装置,向装置D中加入足量无水乙醇,经过滤、洗涤、干燥,得红色固体6.25g。
①加入无水乙醇的目的是
②
 的产率为
的产率为Ⅱ.奥铂(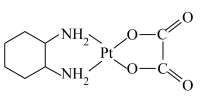 )是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺(
)是一种稳定的水溶性广谱抗肿瘤试剂,1,2-环己二胺( )是制备奥铂的原料之一。
)是制备奥铂的原料之一。
(7)奥铂中H-N-H的键角大于1,2-环已二胺中H-N-H的键角,原因是
(8)1,2-环己二胺的沸点(190℃)高于1,2-环戊二胺(
 )的沸点(170℃),其主要原因是
)的沸点(170℃),其主要原因是
您最近半年使用:0次
解题方法
8 . 下列说法正确的是
A.用电子云轮廓图表示 的 的 键形成的示意图: 键形成的示意图: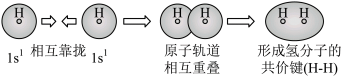 |
B. 的电子式为 的电子式为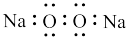 |
| C.共价键的键能越大,分子晶体的熔沸点越高 |
D.同一周期中,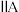 与 与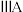 族元素原子的核电荷数都相差1 族元素原子的核电荷数都相差1 |
您最近半年使用:0次
9 . 关于LiBF4及所含元素的说法正确的是
| A.熔点:LiBF4<H3BO3 | B.原子半径:Li<B<F |
| C.第一电离能:Li<B<F | D.电负性:Li<B<F |
您最近半年使用:0次
解题方法
10 . 物质的结构决定物质的性质,下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 溶解度(25℃):S(Na2CO3)>S(NaHCO3) | 有无氢键 |
| B | pKa:一氯乙酸>二氯乙酸>三氯乙酸 | 羟基的极性 |
| C | 碱性(结合H+的能力):NH3>NF3 | 成键元素的电负性 |
| D | 熔点:金刚石>晶体硅 | 晶体类型 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



