1 . 下列有关物质的性质和用途具有对应关系的是
| A.SO2具有氧化性,可用于漂白纸浆 |
| B.CO具有还原性,可用于冶炼铁等金属 |
| C.SiO2熔点高,可用作光导纤维 |
| D.Al2O3具有两性,可用作耐高温材料 |
您最近一年使用:0次
2016-12-09更新
|
319次组卷
|
5卷引用:天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题
解题方法
2 . 合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如表:
常温下,大气固氮的倾向____ 工业固氮(填“大于”或“小于”)。
(2)N2(g)与H2(g)反应的能量变化如图所示。
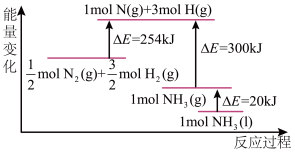
则N2(g)与H2(g)制备NH3(l)的热化学方程式为_____ 。
(3)T℃时,在2L恒容密闭容器中加入1molN2和2molH2模拟一定条件下工业固氮N2(g)+3H2(g) 2NH3(g),体系中n(NH3)随时间的变化如图。
2NH3(g),体系中n(NH3)随时间的变化如图。
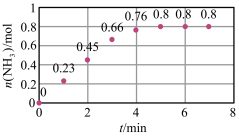
①前2分钟内的平均反应速率v(NH3)=____ mol•L-1•min-1。
②下列情况能说明该反应已达到平衡状态的是____ (选填序号)。
A.混合气体的密度不变
B.单位时间内断裂nmolN-H键的同时形成nmolH-H键
C.3v正(H2)=2v逆(NH3)
D.容器内的总压强不再变化
③有关工业固氮的说法正确的是____ (选填序号)。
A.使用催化剂可提高反应物的转化率
B.温度控制在500℃左右有利于反应向正方向进行
C.循环使用N2、H2可提高NH3的产率
D.增大压强有利于加快反应速率,所以压强越大越好
④T℃时,该反应的平衡常数为_____ 。
⑤若800℃,该反应的平衡常数为2,在该温度下,某时刻,N2、H2、NH3的浓度都2mol/L时,则v正_____ v逆(填“>”、“<”、“=”)。
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol•min-1)与催化剂的对应关系如表所示。
在不同催化剂的催化作用下,氨气分解反应中的活化能最小的催化剂是____ (填化学式)。
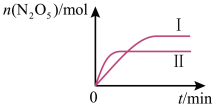
(5)在恒容密闭容器中充入2molNO2和1molO2发生反应如下:4NO2(g)(红棕色)+O2(g) 2N2O5(g)(无色)。已知在不同温度下测得N2O5的物质的量随时间的变化如图所示。该反应的△H
2N2O5(g)(无色)。已知在不同温度下测得N2O5的物质的量随时间的变化如图所示。该反应的△H____ 0,△S____ 0。
(1)固氮一直是科学家致力研究的重要课题,有关热力学数据如表:
| 反应 | 大气固氮N2(g)+O2(g) 2NO(g) 2NO(g) | 工业固氮N2(g)+3H2(g) 2NH3(g) 2NH3(g) | ||||
| 温度/℃ | 25 | 2000 | 25 | 350 | 400 | 450 |
| 平衡常数(K) | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.504 | 0.152 |
常温下,大气固氮的倾向
(2)N2(g)与H2(g)反应的能量变化如图所示。

则N2(g)与H2(g)制备NH3(l)的热化学方程式为
(3)T℃时,在2L恒容密闭容器中加入1molN2和2molH2模拟一定条件下工业固氮N2(g)+3H2(g)
 2NH3(g),体系中n(NH3)随时间的变化如图。
2NH3(g),体系中n(NH3)随时间的变化如图。 
①前2分钟内的平均反应速率v(NH3)=
②下列情况能说明该反应已达到平衡状态的是
A.混合气体的密度不变
B.单位时间内断裂nmolN-H键的同时形成nmolH-H键
C.3v正(H2)=2v逆(NH3)
D.容器内的总压强不再变化
③有关工业固氮的说法正确的是
A.使用催化剂可提高反应物的转化率
B.温度控制在500℃左右有利于反应向正方向进行
C.循环使用N2、H2可提高NH3的产率
D.增大压强有利于加快反应速率,所以压强越大越好
④T℃时,该反应的平衡常数为
⑤若800℃,该反应的平衡常数为2,在该温度下,某时刻,N2、H2、NH3的浓度都2mol/L时,则v正
(4)研究表明某些过渡金属催化剂可以加速氨气的分解,某温度下,用等质量的不同金属分别催化等浓度的氨气,测得氨气分解的初始速率(单位:mmol•min-1)与催化剂的对应关系如表所示。
| 催化剂 | Fe | Pd | Ru | Rh | Pt | Ni |
| 初始速率 | 0.5 | 1.8 | 7.9 | 4.0 | 2.2 | 3.0 |
在不同催化剂的催化作用下,氨气分解反应中的活化能最小的催化剂是
(5)在恒容密闭容器中充入2molNO2和1molO2发生反应如下:4NO2(g)(红棕色)+O2(g)
 2N2O5(g)(无色)。已知在不同温度下测得N2O5的物质的量随时间的变化如图所示。该反应的△H
2N2O5(g)(无色)。已知在不同温度下测得N2O5的物质的量随时间的变化如图所示。该反应的△H
您最近一年使用:0次
名校
解题方法
3 . 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。某同学选用适当的化学试剂和实验用品,用图中的实验装置进行实验,证明过氧化钠可作供氧剂。
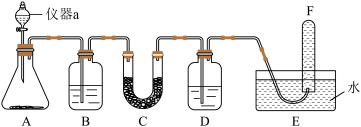
(1)A是制取 的装置,发生反应的离子方程式是
的装置,发生反应的离子方程式是________ 。
(2)B中的试剂是________ 溶液,发生反应的离子方程式是________ 。
(3)C中 的用途
的用途________ 。
(4)D中的试剂是NaOH溶液,其作用是________ 。
(5)试管F中收集满气体后,下一步实验操作是________ ,说明过氧化钠可作供氧剂。

(1)A是制取
 的装置,发生反应的离子方程式是
的装置,发生反应的离子方程式是(2)B中的试剂是
(3)C中
 的用途
的用途(4)D中的试剂是NaOH溶液,其作用是
(5)试管F中收集满气体后,下一步实验操作是
您最近一年使用:0次
4 . 下列物质的用途涉及氧化还原反应的是
A.用 做红色颜料 做红色颜料 | B.用暖宝贴(成分:铁粉、水、食盐、活性炭等)供热 |
C.用 作食品膨松剂 作食品膨松剂 | D.用可溶性的铁盐、铝盐作净水剂 |
您最近一年使用:0次
名校
解题方法
5 . FeSO4·7H2O在工业生产中有重要用途,其结构示意图如下,下列说法错误 的是
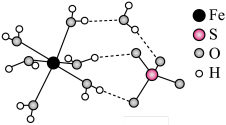
| A.电负性:O>S>H |
| B.基态Fe2+的价层电子排布式:3d6 |
| C.上述结构中含化学键:离子键、共价键、氢键、配位键 |
D.H2O中的O和 中的S均为sp3杂化,H2O的键角小于 中的S均为sp3杂化,H2O的键角小于 的键角 的键角 |
您最近一年使用:0次
2023-02-15更新
|
616次组卷
|
3卷引用:天津市滨海新区塘沽第一中学2023届高三下学期第三次模拟考化学试题
天津市滨海新区塘沽第一中学2023届高三下学期第三次模拟考化学试题广东省广州市第二中学等6校2022-2023学年高三下学期开学考试化学试题(已下线)专题卷20 《物质结构与性质》选择题分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
解题方法
6 . 元素周期表在化学中有举足轻重的地位。请根据提示回答下列问题:
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置_______ 。Fe 分别与硫单质和氯气共热,可以得到两种含铁的二元化合物。请问这两种物质中金属阳离子的未成对电子数之比为_______ 。
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式_______ 。利用铜离子作为中心原子可以形成多种具有良好特性的配合物。我们熟知的是一种深蓝色配合物,向硫酸铜溶液中通入过量氨气,可制备这种深蓝色配合物[Cu(NH3)4]2+。请用适当的化学用语描述该反应过程的实质_______ 。写出[Cu(NH3)4]2+配体的电子式_______ 。
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是_______ 。
(4)CoO 的晶胞如图所示。
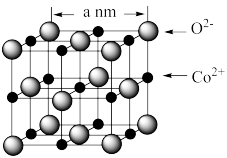
设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为_______ g﹒cm−3(列出计算式即可)
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO 的 VSEPR 模型为
的 VSEPR 模型为_______ ,其中 P 的杂化轨道类型为_______ 。
(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因_______ 。
(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因_______
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因_______ 。
(1)铁在生活生产中用途广泛,写出 Fe 在元素周期表中的位置
(2)古往今来,人类发展的脚步离不开青铜器的冶炼,锻造及使用。如今,铜元素依旧为科研人员所钟爱,请写出铜原子的价电子排布式
(3)I1表示第一电离,I1(Mg)> I1(Al)> I1(Na),原因是
(4)CoO 的晶胞如图所示。

设阿伏加德罗常数的值为 NA,则 CoO 晶体的密度为
(5)磷元素在农药的合成中有着重要作用。了解其化合物的结构有助于我们合成新型农药,提高粮食的产量。PO
 的 VSEPR 模型为
的 VSEPR 模型为(6)配位化学中,硼元素深受研究者的喜爱。其原因在于 B 容易与配体形成配位键,如BF
 、B(OH)
、B(OH) 等,从原子结构分析其原因
等,从原子结构分析其原因(7)溶解度、熔沸点、颜色等是每种物质自身特有的性质,但也存在一定的规律。
①水和 H2S 均可以溶于乙醇,但 H2O 在乙醇中的溶解度大于 H2S 的原因
a.水和乙醇均为分子晶体 b.水和乙醇分子间可以形成氢键 c.水和乙醇可以发生反应
②比较下列锗卤化物的熔点和沸点,分析其变化规律的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约 400 |
您最近一年使用:0次
7 . NO、SO2是大气污染物但又有着重要用途。
I.已知:N2(g)+O2(g) = 2NO(g) ∆H1=+180.5kJ/mol
C(s)+ O2(g) = CO2(g) ∆H2=-393.5kJ/mol
2C(s)+ O2(g) = 2CO(g) ∆H3=-221.0kJ/mol
(1)某反应的平衡常数表达式K=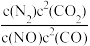 ,此反应的热化学方程式为:
,此反应的热化学方程式为:_____
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是_____ (填序号)
a.NO和N2浓度比为2:1 b.v正(CO)=2v逆(N2)
c.混合气体的密度保持不变 d.该反应平衡常数保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如图实验流程:

用离子方程式表示Na2S2O3溶液具有碱性的原因_____ ,Na2S2O3与足量氯水反应的离子方程式是____
(4)含SO2的烟气可用Na2SO3溶液吸收。
可将吸收液送至电解槽再生后循环使用。再生电解槽如图1所示。a电极上含硫微粒放电的反应式为___ (任写一个)
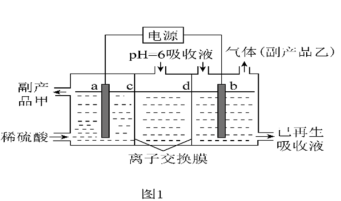
(5)2SO3(g)⇌2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图2所示。
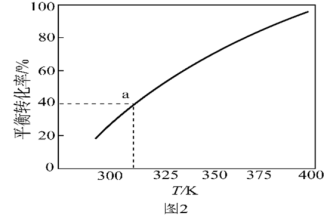
图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp=_____  用平衡分压代替平衡浓度计算,分压=
用平衡分压代替平衡浓度计算,分压= 总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将_______ (填“向正反应方向”或“向逆反应方向”“不”)移动。
I.已知:N2(g)+O2(g) = 2NO(g) ∆H1=+180.5kJ/mol
C(s)+ O2(g) = CO2(g) ∆H2=-393.5kJ/mol
2C(s)+ O2(g) = 2CO(g) ∆H3=-221.0kJ/mol
(1)某反应的平衡常数表达式K=
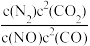 ,此反应的热化学方程式为:
,此反应的热化学方程式为:(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是
a.NO和N2浓度比为2:1 b.v正(CO)=2v逆(N2)
c.混合气体的密度保持不变 d.该反应平衡常数保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如图实验流程:

用离子方程式表示Na2S2O3溶液具有碱性的原因
(4)含SO2的烟气可用Na2SO3溶液吸收。
可将吸收液送至电解槽再生后循环使用。再生电解槽如图1所示。a电极上含硫微粒放电的反应式为

(5)2SO3(g)⇌2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图2所示。

图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp=
 用平衡分压代替平衡浓度计算,分压=
用平衡分压代替平衡浓度计算,分压= 总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
您最近一年使用:0次
解题方法
8 . 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。请回答下列问题:
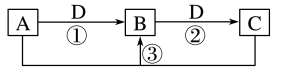
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式是___________ ;工业上制取A的离子方程式为___________ 。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为___________ 。将B、C的混合气体溶于氢氧化钠溶液中的化学方程式___________ 。
(3)若D是氯碱工业的主要产品之一,B物质具有两性,则反应②的离子方程式是___________ 。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___________ 。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:___________ 。

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式是
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
(3)若D是氯碱工业的主要产品之一,B物质具有两性,则反应②的离子方程式是
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 下列现象或用途与浓硫酸的吸水性和脱水性无关的是
| A.浓硫酸可作氯气的干燥剂 |
| B.浓硫酸滴加到蔗糖中,蔗糖变黑 |
| C.浓硫酸滴加到胆矾上,蓝色晶体变成白色粉末 |
| D.浓硫酸在加热条件下可与铜等不活泼金属反应 |
您最近一年使用:0次
2021-01-19更新
|
1063次组卷
|
21卷引用:天津市滨海新区田家炳中学2023-2024学年高一下学期第一次月考化学试题
天津市滨海新区田家炳中学2023-2024学年高一下学期第一次月考化学试题人教版(2019)必修第二册第五章第一节课时2河北省石家庄二中实验学校2019-2020学年高一下学期3月月考化学试题广东省茂名市信宜中学2019-2020学年高一下学期级线上段考化学试题辽宁省实验中学东戴河校区2019-2020学年高一下学期期中考试化学试题必修第二册RJ第5章第一节 硫及其化合物 课时2 硫酸硫酸根离子的检验高一必修第一册(苏教2019版)专题4 第一单元 含硫化合物的性质 课时2 硫酸的工业制备和浓硫酸的性质广东省东莞市光明中学2020-2021学年高二上学期期初考试化学试题甘肃省武威市民勤县第一中学2019-2020学年高一下学期期中考试化学(文) 试题山东省济南市章丘市第一中学2020-2021学年高一上学期12月月考化学试题人教版2019必修第二册 第五章 第一节 第2课时 硫酸 硫酸根离子的检验河北省深州市长江中学2020-2021学年高一下学期3月底月考化学试题吉林省延边朝鲜族自治州汪清县第六中学2020-2021学年高一下学期3月月考化学试题甘肃省白银市会宁县第四中学2021-2022学年高一下学期第一次月考化学试题(已下线)专题01 硫及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)第01练 硫及其化合物-2023年【暑假分层作业】高一化学(人教版2019必修第二册)湖南省衡阳县第四中学2022-2023学年高一下学期第一次(3月)月考化学试题5.1.2硫酸随堂练习(已下线)清单01 硫及其化合物的性质(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)猜想01 硫及其化合物的性质与转化(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)四川省广安第二中学校2024-2025学年高二上学期开学考试化学试题
名校
解题方法
10 . 水解原理在生产和生活中都具有重要的用途。下列事实与盐类的水解无关的是
| A.TiCl4溶于大量水加热制备TiO2 |
| B.加热蒸干CuCl2溶液得到Cu(OH)2固体 |
| C.次氯酸常用作消毒剂 |
| D.FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
您最近一年使用:0次
2021-01-20更新
|
222次组卷
|
2卷引用:天津市滨海新区2020-2021学年高二上学期期末考试化学试题



