解题方法
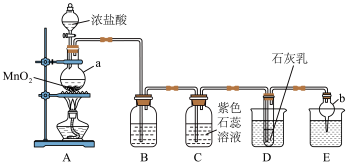
1 . Ca(ClO)2具有强氧化性,可作漂白剂。某化学兴趣小组利用如图装置制取Ca(ClO)2。已知:①氯气和碱的反应是放热反应;②Ca(ClO)2遇热水会分解生成Ca(ClO3)2。
回答下列问题:______ ,装置A中发生反应的离子方程式是______ 。
(2)装置B中盛装的试剂是______ ,其作用是______ 。
(3)装置C中的颜色变化为_______ 。
(4)为了提高Ca(ClO)2的产率,防止副反应发生,装置D需要控制一定温度,采用方式为______ (填“热水浴”或“冷水浴”),实验中除控制温度外还可采取的措施是______ 。
(5)已知氯气和Ca(OH)2溶液在一定温度下能同时发生反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。某温度下,将氯气通入Ca(OH)2溶液中,反应得到CaCl2、Ca(ClO)2和Ca(ClO3)2的混合溶液,该反应中,氧化反应的产物为______ (填化学式),经测定ClO-与ClO 的个数比为2:3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2:3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为______ 。
回答下列问题:
(2)装置B中盛装的试剂是
(3)装置C中的颜色变化为
(4)为了提高Ca(ClO)2的产率,防止副反应发生,装置D需要控制一定温度,采用方式为
(5)已知氯气和Ca(OH)2溶液在一定温度下能同时发生反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。某温度下,将氯气通入Ca(OH)2溶液中,反应得到CaCl2、Ca(ClO)2和Ca(ClO3)2的混合溶液,该反应中,氧化反应的产物为
 的个数比为2:3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
的个数比为2:3,则氯气与氢氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为
您最近一年使用:0次
解题方法
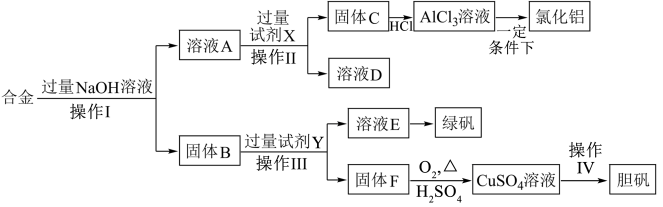
2 . 为探索工业废料的再利用,某化学兴趣小组设计了如图实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4•7H2O)和胆矾晶体(CuSO4•5H2O)。
(1)操作I的实验操作是______ 。在实验室中进行该操作时,用到的玻璃仪器有______ 。
(2)固体B是_____ ;试剂X是______ 。
(3)溶液A与过量的试剂X反应的离子方程式为______ 。
(4)试剂Y是______ ,操作Ⅳ的实验操作为_______ 。
(5)写出用固体F制备CuSO4溶液的化学方程式:______ 。
(6)若该合金的质量为147g,铝和铜占合金总质量的61.9%,则理论生成的绿矾晶体的质量为______ g(保留整数)。
(1)操作I的实验操作是
(2)固体B是
(3)溶液A与过量的试剂X反应的离子方程式为
(4)试剂Y是
(5)写出用固体F制备CuSO4溶液的化学方程式:
(6)若该合金的质量为147g,铝和铜占合金总质量的61.9%,则理论生成的绿矾晶体的质量为
您最近一年使用:0次
3 . A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素。A元素的原子是元素周期表中相对原子质量最小的;A和D、C和F分别为同一主族元素;常温下,B和C两种元素的单质都为双原子分子,且两种单质在空气中含量之和高达99%;E的最外层电子数为2。
回答下列问题:
(1)分别写出B和G的元素符号:______ 、______ 。
(2)E在元素周期表中的位置是_______ 。
(3)写出A与C以原子个数比1:1形成的化合物的电子式:______ ,该物质为_____ (填“共价”或“离子”)化合物。
(4)F、G中最高价氧化物对应的水化物酸性较弱的化合物是______ (填化学式)。
(5)由B、G形成的化合物分子中,B和G原子的最外层均达到8电子稳定结构,该化合物遇水反应生成一种具有漂白性的化合物和另一种10电子氢化物,写出反应的化学方程式:_______ 。
回答下列问题:
(1)分别写出B和G的元素符号:
(2)E在元素周期表中的位置是
(3)写出A与C以原子个数比1:1形成的化合物的电子式:
(4)F、G中最高价氧化物对应的水化物酸性较弱的化合物是
(5)由B、G形成的化合物分子中,B和G原子的最外层均达到8电子稳定结构,该化合物遇水反应生成一种具有漂白性的化合物和另一种10电子氢化物,写出反应的化学方程式:
您最近一年使用:0次
4 . 利用如下实验研究浓硫酸的性质:
实验1:取2g蔗糖放入大试管中,加2~3滴水,再加入3mL浓硫酸,搅拌,蔗糖变黑,同时将产生的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色;
实验2:将一小片铜放入试管中再加入3mL浓硫酸,加热,将产生的气体通入品红溶液中,观察到品红溶液褪色。将反应后的混合物溶于水,得到蓝色溶液。
下列说法正确的是
实验1:取2g蔗糖放入大试管中,加2~3滴水,再加入3mL浓硫酸,搅拌,蔗糖变黑,同时将产生的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色;
实验2:将一小片铜放入试管中再加入3mL浓硫酸,加热,将产生的气体通入品红溶液中,观察到品红溶液褪色。将反应后的混合物溶于水,得到蓝色溶液。
下列说法正确的是
| A.实验1现象说明浓硫酸在实验中只体现脱水性 |
| B.实验2可以说明浓硫酸具有强氧化性和酸性 |
| C.将实验1中产生的气体依次通入澄清石灰水、品红溶液可证明该混合气体中含有CO2和SO2 |
| D.由实验1和实验2得出浓硫酸有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2 |
您最近一年使用:0次
5 . 纳米级Fe3O4可用于以太阳能为热源分解水制H2,过程如图所示。下列说法正确的是
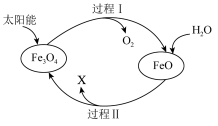
| A.过程I中O2为还原反应的产物 |
| B.过程Ⅱ的反应为3FeO+H2O=H2↑+Fe3O4 |
| C.过程I中每生成1molO2反应转移2mol电子 |
| D.FeO的稳定性强于Fe3O4 |
您最近一年使用:0次
6 . 下列离子反应方程式正确的是
| A.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe2+ |
B.碳酸氢钠溶液中加入过量氢氧化钙溶液:Ca2++2HCO +2OH-=CaCO3↓+2H2O+CO +2OH-=CaCO3↓+2H2O+CO |
| C.向CuSO4溶液中加入一小粒钠块:2Na+Cu2+=2Na++Cu |
D.向氯水中通入足量SO2气体:Cl2+SO2+2H2O=4H++2Cl-+SO |
您最近一年使用:0次
7 . 根据下列实验操作和现象所得到的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 该溶液中一定含有钠元素 |
| B | 把充满SO2、塞有橡胶塞的试管倒立在水中,打开塞子,试管内液面会缓慢上升 | SO2易溶于水 |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | Na2O2没有变质 |
| D | 向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变红褐色,停止加热,用激光笔照射,出现一条光亮通路 | 有Fe(OH)3胶体生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 硫在不同温度下的状态和分子结构不同,单质硫S8环状分子的结构如图。 时硫变为蒸气,蒸气中存在:3S8
时硫变为蒸气,蒸气中存在:3S8 4S6
4S6 6S4
6S4 12S2。下列说法错误的是
12S2。下列说法错误的是
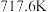 时硫变为蒸气,蒸气中存在:3S8
时硫变为蒸气,蒸气中存在:3S8 4S6
4S6 6S4
6S4 12S2。下列说法错误的是
12S2。下列说法错误的是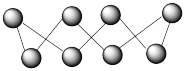
| A.S8、S6、S4、S2互为同素异形体,其相互转化为化学变化 |
B.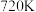 时,32gS8中共价键的数目为NA 时,32gS8中共价键的数目为NA |
| C.可用酒精洗涤试管内壁残留的硫单质 |
| D.硫在自然界中存在游离态形式 |
您最近一年使用:0次
9 . 低成本、高效率处理SO2、NO2等大气污染物一直是化学研究的重点课题。研究它们的性质在工业生产和环境保护中有着重要意义。下列有关二氧化硫的说法正确的是
| A.SO2是一种黄绿色、有刺激性气味的有毒气体 |
| B.SO2能使紫色石蕊试液先变红后褪色 |
| C.SO2能使酸性高锰酸钾溶液褪色,SO2具有漂白性 |
| D.SO2通入Na2S溶液,溶液变浑浊,SO2具有氧化性 |
您最近一年使用:0次
10 . 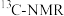 (核磁共振)、
(核磁共振)、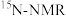 可用于测定蛋白质,核酸等生物大分子的空间结构,瑞士科学家库尔特、维特里希等人为此获得了诺贝尔化学奖。下列有关元素的说法中正确的是
可用于测定蛋白质,核酸等生物大分子的空间结构,瑞士科学家库尔特、维特里希等人为此获得了诺贝尔化学奖。下列有关元素的说法中正确的是
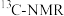 (核磁共振)、
(核磁共振)、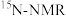 可用于测定蛋白质,核酸等生物大分子的空间结构,瑞士科学家库尔特、维特里希等人为此获得了诺贝尔化学奖。下列有关元素的说法中正确的是
可用于测定蛋白质,核酸等生物大分子的空间结构,瑞士科学家库尔特、维特里希等人为此获得了诺贝尔化学奖。下列有关元素的说法中正确的是A.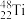 和第 和第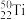 互为同位素 互为同位素 |
| B.12C与金刚石互为同素异形体 。 |
C. 为同一种核素 为同一种核素 |
D. 的质量数为核外电子数与原子序数之和 的质量数为核外电子数与原子序数之和 |
您最近一年使用:0次
2024-09-18更新
|
31次组卷
|
10卷引用:辽宁省朝阳市2023-2024学年高一下学期开学化学试题
辽宁省朝阳市2023-2024学年高一下学期开学化学试题河南省叶县高级中学2022-2023学年高一上学期1月期末考试化学试题河北省保定市泽龙实验中学2022-2023学年高一下学期开学检测化学试题四川省成都市第七中学2022-2023学年高一上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高一下学期第一次考试化学试题第2课时 元素周期表 核素河北省郑口中学2023-2024学年高一上学期第四次质量检测化学试卷河南省新未来联考2023-2024学年高一下学期4月期中考试化学试题广东省湛江第一中学2022-2023学年高一上学期期末考试化学试卷 安徽省马鞍山市第二中学2022-2023学年高一下学期选科分班摸底测试化学试卷



