名校
解题方法
1 . 下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A. | B. | C. | D. |
您最近一年使用:0次
昨日更新
|
85次组卷
|
18卷引用:吉林省通化市职教中心高中部2020-2021学年高一12月月考化学试题
吉林省通化市职教中心高中部2020-2021学年高一12月月考化学试题北京四中2017-2018学年高一上学期期末考试化学试题步步为赢 高一化学寒假作业:作业十三 富集在海水中的元素——氯(已下线)3.1.2 氯气的性质与应用练习(1)——《高中新教材同步备课》(苏教版 必修第一册)湖南省长沙市雅礼中学2020-2021学年高一上学期期中考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高一上学期期中考试化学试题甘肃省民勤县第一中学2022-2023学年高一上学期开学考试化学试题吉林省长春北师大附属学校2021-2022学年高一上学期期中考试化学试题湖北省沙市中学2022-2023学年高一上学期第二次月考化学试题重庆市育才中学校2022-2023学年高一上学期期中考试化学试题 吉林省长春市农安县2022-2023学年高一上学期11月质量监测化学试题重庆市南开中学校2022-2023学年高一上学期12月月考化学试题安徽工业大学附属中学2022-2023学年高一上学期11月期中考试化学试题宁夏回族自治区银川一中2023-2024学年高一上学期期中考试化学试题新疆乌鲁木齐市第六十八中学2023-2024学年高一上学期期中考试化学试卷 安徽省池州市贵池区2023-2024学年高一上学期期中考试化学试卷甘肃省武威市民勤县等2地2024-2025学年高一上学期开学考试 化学试题湖北省大冶市第一中学2024-2025学年高一上学期入学考试化学试题
名校
2 . 人工合成某维生素(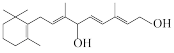 )的路线如下所示。
)的路线如下所示。
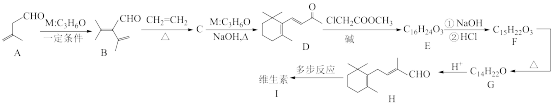
已知:①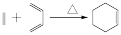 ;
;
②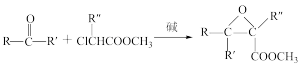 (R、R′、R″为H原子或烃基)。
(R、R′、R″为H原子或烃基)。
(1)有机物A与足量
 反应生成产物的名称为
反应生成产物的名称为(2)B→C的反应类型为
(3)D→E的化学方程式为
(4)F中含有
(5)G的同系物K分子式为
 ,其同分异构体中符合下列条件的有
,其同分异构体中符合下列条件的有①苯环上含有两个取代基 ②能与金属钠反应 ③存在两个甲基 ④水溶液呈中性
(6)参照上述合成路线,写出以氯乙酸甲酯(
 )和
)和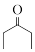 为主要原料合成
为主要原料合成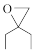 的路线。
的路线。
您最近一年使用:0次
2024-09-15更新
|
204次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期9月月考化学试题
3 .  还原
还原 实现“双减”目标,涉及反应如下:
实现“双减”目标,涉及反应如下:
Ⅰ.

 ;
;
Ⅱ.
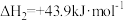
 。
。
回答下列问题:
(1)升高温度时, 将
将_______ (填“增大”“减少”或“不变”)。
(2)物质的标准摩尔生成焓是指在标准压力(100kPa)和某温度下,由元素最稳定的单质生成1mol该纯净物时的焓变。一些物质在298K时的标准摩尔生成焓( )如表所示。
)如表所示。

_______ 。
(3)阿伦尼乌斯公式为 (其中k为反应速率常数,A为比例系数,R为理想气体常数,
(其中k为反应速率常数,A为比例系数,R为理想气体常数, 为反应的活化能,e为自然对数的底,T为温度),反应Ⅰ的速率方程为
为反应的活化能,e为自然对数的底,T为温度),反应Ⅰ的速率方程为 ,
, ,增大体系的压强,
,增大体系的压强,
___ (填“增大”“减小”或“不变”)。
(4)一定条件下,向恒压密闭容器中以一定流速通入 和
和 混合气体,
混合气体, 平衡转化率和
平衡转化率和 选择性[
选择性[ ]随温度、投料比的变化曲线如图所示。
]随温度、投料比的变化曲线如图所示。 选择性的曲线是
选择性的曲线是_______ (填“ ”或“
”或“ ”);
”); 平衡转化率随温度升高发生如图变化的原因是
平衡转化率随温度升高发生如图变化的原因是_______ 。
②生成 的最佳条件是
的最佳条件是_______ (填序号)。
a.220℃, b.220℃,
b.220℃,
c.320℃, d.320℃,
d.320℃,
(5)一定温度下,向恒压密闭容器中通入 和
和 ,充分反应后,测得
,充分反应后,测得 平衡转化率为a,
平衡转化率为a, 选择性为b,该温度下反应Ⅰ的平衡常数
选择性为b,该温度下反应Ⅰ的平衡常数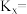
_______ ( 为以物质的量分数表示的平衡常数)。
为以物质的量分数表示的平衡常数)。
 还原
还原 实现“双减”目标,涉及反应如下:
实现“双减”目标,涉及反应如下:Ⅰ.


 ;
;Ⅱ.

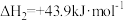
 。
。回答下列问题:
(1)升高温度时,
 将
将(2)物质的标准摩尔生成焓是指在标准压力(100kPa)和某温度下,由元素最稳定的单质生成1mol该纯净物时的焓变。一些物质在298K时的标准摩尔生成焓(
 )如表所示。
)如表所示。| 物质 |  |  |  |  |
 ( ( ) ) |  |  | 0 | 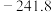 |

(3)阿伦尼乌斯公式为
 (其中k为反应速率常数,A为比例系数,R为理想气体常数,
(其中k为反应速率常数,A为比例系数,R为理想气体常数, 为反应的活化能,e为自然对数的底,T为温度),反应Ⅰ的速率方程为
为反应的活化能,e为自然对数的底,T为温度),反应Ⅰ的速率方程为 ,
, ,增大体系的压强,
,增大体系的压强,
(4)一定条件下,向恒压密闭容器中以一定流速通入
 和
和 混合气体,
混合气体, 平衡转化率和
平衡转化率和 选择性[
选择性[ ]随温度、投料比的变化曲线如图所示。
]随温度、投料比的变化曲线如图所示。
 选择性的曲线是
选择性的曲线是 ”或“
”或“ ”);
”); 平衡转化率随温度升高发生如图变化的原因是
平衡转化率随温度升高发生如图变化的原因是②生成
 的最佳条件是
的最佳条件是a.220℃,
 b.220℃,
b.220℃,
c.320℃,
 d.320℃,
d.320℃,
(5)一定温度下,向恒压密闭容器中通入
 和
和 ,充分反应后,测得
,充分反应后,测得 平衡转化率为a,
平衡转化率为a, 选择性为b,该温度下反应Ⅰ的平衡常数
选择性为b,该温度下反应Ⅰ的平衡常数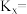
 为以物质的量分数表示的平衡常数)。
为以物质的量分数表示的平衡常数)。
您最近一年使用:0次
2024-09-15更新
|
208次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期9月月考化学试题
名校
4 . 由钛铁矿(主要成分是钛酸亚铁: ,还含有少量
,还含有少量 、
、 等杂质),制备海绵钛的一种工艺流程示意如下:
等杂质),制备海绵钛的一种工艺流程示意如下: ;
; 易水解,只能存于强酸性溶液中。
易水解,只能存于强酸性溶液中。
回答下列问题:
(1)浸渣为______ 。
(2)试剂X为______ (填化学式),X的作用是______ 。
(3)“操作Ⅱ”为______ 。
(4)“氯化”过程在高温条件下进行,发生反应的化学方程式为______ 。
(5)制备海绵钛中Ar的作用是______ 。
(6) 有三种类型晶体结构,其中一种晶胞结构如图所示。
有三种类型晶体结构,其中一种晶胞结构如图所示。______ 。
②晶胞中白球代表______ (填“钛”或“氧”),该晶体的密度为______  (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ,还含有少量
,还含有少量 、
、 等杂质),制备海绵钛的一种工艺流程示意如下:
等杂质),制备海绵钛的一种工艺流程示意如下: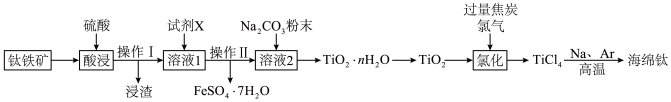
 ;
; 易水解,只能存于强酸性溶液中。
易水解,只能存于强酸性溶液中。回答下列问题:
(1)浸渣为
(2)试剂X为
(3)“操作Ⅱ”为
(4)“氯化”过程在高温条件下进行,发生反应的化学方程式为
(5)制备海绵钛中Ar的作用是
(6)
 有三种类型晶体结构,其中一种晶胞结构如图所示。
有三种类型晶体结构,其中一种晶胞结构如图所示。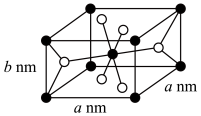
②晶胞中白球代表
 (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2024-09-15更新
|
144次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期9月月考化学试题
名校
5 .  分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
 分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)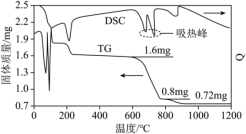
| A.0~400℃范围内,发生了化学变化 | B.600~800℃范围内,没有氧化还原反应发生 |
C.1000℃时,剩余固体的成分为 | D. 分解生成的气体可以用于制硫酸 分解生成的气体可以用于制硫酸 |
您最近一年使用:0次
2024-09-15更新
|
134次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期9月月考化学试题
名校
6 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.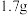 羟基和 羟基和 中含有的质子数均为 中含有的质子数均为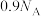 |
B. 含有的中子数为 含有的中子数为 |
C. 乙烷和丙烯的混合气体中所含碳氢键数为 乙烷和丙烯的混合气体中所含碳氢键数为 |
D.常温下,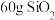 中含有Si—O极性键的数目为 中含有Si—O极性键的数目为 |
您最近一年使用:0次
2024-09-15更新
|
144次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期9月月考化学试题
名校
7 . 抗坏血酸(即维生素C)有较强的还原性,是常用的食品抗氧化剂。下列有关抗坏血酸的说法不正确 的是
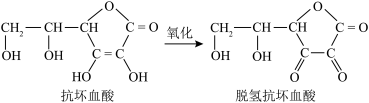
A.分子式是  |
| B.分子中有羟基、酯基和碳碳双键 |
| C.能使酸性 KMnO4溶液褪色 |
| D.抗坏血酸与脱氢抗坏血酸互为同分异构体 |
您最近一年使用:0次
2024-08-21更新
|
113次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2024-2025学年高二上学期开学考试化学试题
名校
8 . 己二酸主要用作工程塑料的原料。实验室可用 氧化环己醇制备己二酸,其反应原理及实验过程如下:
氧化环己醇制备己二酸,其反应原理及实验过程如下: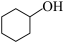
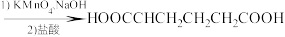 。
。
环己醇、高锰酸钾、10% NaOH溶液、
 和浓盐酸。
和浓盐酸。【步骤】
①在烧杯中加入5mL 10% NaOH溶液和50mL蒸馏水,在搅拌下加入6g高锰酸钾,待高锰酸钾溶解后,用滴管慢慢加入3mL环己醇,控制滴加速度;维持反应温度在45℃左右。滴加完毕后,维持反应5min左右,使氧化反应完全并使二氧化锰沉淀凝结。
②检验反应物。用玻璃棒蘸取一滴反应混合物点到滤纸上做点滴试验,如果有高锰酸盐存在,则在二氧化锰点的周围出现“紫色环”,可加入
 固体直到呈无色为止。
固体直到呈无色为止。③分离提纯产品。趁热过滤混合物,用少量热水洗涤滤渣X 3次,合并滤液与洗涤液,用约4mL浓盐酸酸化,使溶液呈强酸性。在石棉网上加热浓缩使溶液体积减少至10mL左右,加入少量活性炭脱色后趁热过滤,结晶,得到白色己二酸晶体。
请回答下列问题:
(1)步骤①中,烧杯的规格宜选择
A.50mL B.250mL C.500mL
(2)步骤①中,加热方式宜选择
(3)步骤②中,加入
 的目的是
的目的是(4)步骤③中,第一次趁热过滤(装置如图所示)的目的是
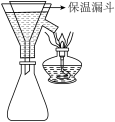
| A.还原性 | B.氧化性 | C.吸附性 | D.稳定性 |
(6)已知:己二酸在水中的溶解度与温度的关系如图所示:

您最近一年使用:0次
2024-08-21更新
|
72次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期开学考试化学试题
名校
解题方法
9 . “宏观辨识与微观探析是化学学科核心素养之一”。一种异黄酮类化合物Z的部分合成路线如下:
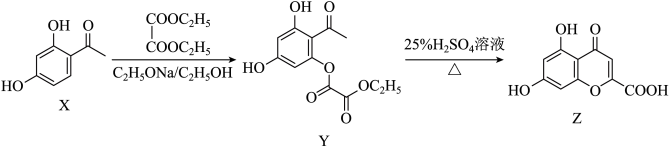
A.X可与 溶液反应显示特殊颜色 溶液反应显示特殊颜色 |
| B.等物质的量的X、Y分别与足量溴水反应,消耗单质溴的物质的量相等 |
| C.1molY最多能与4molNaOH完全反应 |
| D.向过量碳酸钠溶液中逐滴加入1molZ,消耗3mol碳酸钠 |
您最近一年使用:0次
2024-08-21更新
|
115次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2024-2025学年高三上学期开学考试化学试题
10-11高二下·福建莆田·阶段练习
名校
解题方法
10 . 在体积都为1L,c(H+)都为0.01 mol·L-1的盐酸和醋酸溶液中,投入0.65 g锌粒,则下列图示符合客观事实的是
A.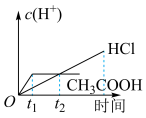 | B.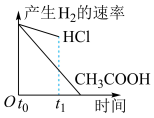 | C.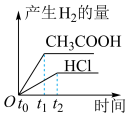 | D.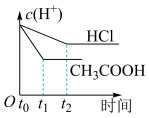 |
您最近一年使用:0次
2024-08-20更新
|
710次组卷
|
53卷引用:吉林省通化市梅河口市博文学校2019-2020学年高二上学期期末考试化学试题
吉林省通化市梅河口市博文学校2019-2020学年高二上学期期末考试化学试题(已下线)2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷(已下线)2011-2012学年河北省魏县一中高二上学期期中考试化学试卷(已下线)2011-2012学年黑龙江省大庆铁人中学高二上学期第二阶段测试化学试卷(已下线)2011-2012学年黑龙江省牡丹江一中高二上学期期末考试化学试卷(已下线)2012届四川省乐山市高三上学期期末教学质量检测化学试卷(已下线)2014届甘肃省天水市秦安县高三上学期期末检测化学试卷(已下线)2014-2015学年辽宁沈阳铁路实验中学高二上学期第一次月考化学试卷2014-2015广东省汕头市金山中学高二上学期月考化学(理)试卷2014-2015湖南省浏阳市高二上学期理科化学试卷2015-2016学年河北省冀州中学高二上第二次月考化学试卷2015-2016学年江西省南昌二中高二上第三次考试化学试卷2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷2015-2016学年天津市和平区高二上学期期末考试化学试卷2015-2016学年福建省泉州市四校高二上学期期末化学试卷2016-2017学年重庆市巴蜀中学高二上第一次月考化学卷2016-2017学年陕西西安中学高二实验班上期中化学卷2016-2017学年江西省上高二中高二上月考三化学试卷2016-2017学年黑龙江省牡丹江市第一高级中学高二上学期开学检测化学试卷江西省南昌市第二中学2017-2018学年高二上学期期中考试化学试题江西省南昌二中2017-2018学年高二上学期期中考试化学试卷福建省三明市第一中学2017-2018学年高二上学期第二次月考化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题四川省什邡中学2017-2018学年高二春秋招班第三次月考化学试题(已下线)2018年10月6日 《每日一题》一轮复习—周末培优【全国百强校】河北省辛集中学2018-2019学年高二上学期期中考试化学试题安徽省合肥市一六八中学2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第三章 第二节 水的电离和溶液的酸碱性【全国百强校】山东省博兴县第一中学2019届高三上学期第三次月考化学试题(已下线)2019年10月1日《每日一题》2020年高考一轮复习 —— 弱电解质的电离平衡山东省济宁市第一中学2017—2018学年高二上学期期中模块检测化学试题(已下线)【南昌新东方】江西省南昌市第三中学2019-2020学年度高二上学期期中化学试题2020届高三化学二轮冲刺新题专练——弱电解质的电离平衡安徽省涡阳县第一中学2019-2020学年高二3月月考化学试题(已下线)上海市嘉定区2010届高三上学期期末考试化学试题甘肃省西北师范大学附属中学2019-2020学年高二上学期期中考试化学试题湖南省衡阳市第二十六中学2021届高三上学期9月月考化学试题选择性必修1 专题3 第一单元 弱电解质的电离平衡湖北省黄冈市浠水县实验高级中学2021-2022学年高二上学期九月月考化学试题(已下线)专题3.1 电离平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)高中化学《新教材变化解读与考法剖析》第三章 水溶液中的离子反应与平衡(人教版2019选择性必修1)(已下线)3.1.1 电离平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)必考点04 弱电解质的电离-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版) (已下线)第1讲 弱电解质的电离平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)3.1.1 强电解质和弱电解质-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)甘肃省兰州第一中学2022-2023学年高二上学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)(已下线)3.2.1 弱电解质的电离平衡-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)3.1.1强电解质和弱电解质 弱电解质的电离平衡 课后江西省永修县第一中学2023-2024学年高二上学期10月月考化学试题山西省大同市浑源七中2022-2023学年高二下学期第一次月考化学试题 3.1.1强电解质和弱电解质课后作业—巩固篇3.1.2 弱电解质的电离平衡随堂检测



