1 . 下列实验操作、现象与结论均正确的是
| 实验操作或方法 | 实验现象 | 结论 | |
| A | 为鉴别久置 溶液是否存在有 溶液是否存在有 ,向溶液中滴加酸性 ,向溶液中滴加酸性 溶液。 溶液。 |  溶液后紫红色褪去。 溶液后紫红色褪去。 | 久置溶液中有部分 残留。 残留。 |
| B | 向某溶液中加入稀盐酸酸化的氯化钡溶液。 | 溶液中出现白色沉淀 | 溶液中一定存在 。 。 |
| C | 取少量溶液于试管中,加入 后,在试管口放置一块红色石蕊试纸。 后,在试管口放置一块红色石蕊试纸。 | 红色石蕊试纸变蓝 | 溶液中一定存在 |
| D | 向 溶液中加入 溶液中加入 溶液至不再生成白色沉淀,再滴加 溶液至不再生成白色沉淀,再滴加 溶液。 溶液。 | 生成黄色沉淀 | 说明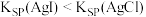 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-09-07更新
|
372次组卷
|
2卷引用:湖南省邵阳市第六中学2024届高三下学期高考考前化学冲刺卷(二)
2 . 已知钼(Mo)的晶胞如图所示,晶胞边长为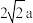 pm,相对原子质量为M,以NA表示阿伏加 德罗常数的值。
pm,相对原子质量为M,以NA表示阿伏加 德罗常数的值。_______ ,晶体中粒子的配位数为_______ 。
(2)构成钼晶体的粒子是_______ ,晶胞中所含的粒子数为_______ 。
(3)金属钼的密度为_______ g·cm-3。
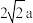 pm,相对原子质量为M,以NA表示阿伏加 德罗常数的值。
pm,相对原子质量为M,以NA表示阿伏加 德罗常数的值。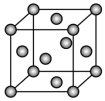
(2)构成钼晶体的粒子是
(3)金属钼的密度为
您最近一年使用:0次
名校
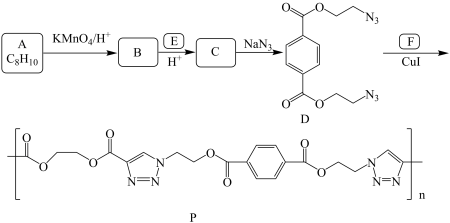
3 . 某课题组研制了一种具有较高玻璃化转变温度的聚合物P,合成路线如下:
(1)化合物B的名称是_____ ;化合物E的结构简式是_____ 。
(2)B生成C的反应类型为_____ 。
(3)下列说法不正确的是_____。
(4)化合物C生成D的化学方程式是_____ 。
(5)同时满足下列条件的化合物B的同分异构体(不考虑立体异构体)有_____ 种。
①能发生银镜反应
②能和 溶液反应生成
溶液反应生成
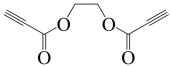
(6)以乙醇和丙炔酸为原料,设计如下化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)_____ 。
已知: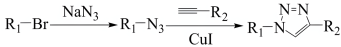
(1)化合物B的名称是
(2)B生成C的反应类型为
(3)下列说法不正确的是_____。
| A.化合物A分子中所有的碳原子一定共平面 |
B.化合物D中O原子的杂化方式均是 |
| C.化合物A的一氯代物仅有2种 |
| D.聚合物P中含氧官能团只有1种 |
(4)化合物C生成D的化学方程式是
(5)同时满足下列条件的化合物B的同分异构体(不考虑立体异构体)有
①能发生银镜反应
②能和
 溶液反应生成
溶液反应生成
(6)以乙醇和丙炔酸为原料,设计如下化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)
您最近一年使用:0次
4 .  可用于催化剂载体及功能材料的制备。天然独居石中,铈
可用于催化剂载体及功能材料的制备。天然独居石中,铈 主要以
主要以 形式存在,还含有
形式存在,还含有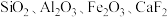 等物质。以独居石为原料制备
等物质。以独居石为原料制备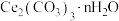 的工艺流程如下,下列说法不正确的是
的工艺流程如下,下列说法不正确的是
 可用于催化剂载体及功能材料的制备。天然独居石中,铈
可用于催化剂载体及功能材料的制备。天然独居石中,铈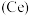 主要以
主要以 形式存在,还含有
形式存在,还含有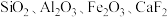 等物质。以独居石为原料制备
等物质。以独居石为原料制备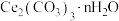 的工艺流程如下,下列说法不正确的是
的工艺流程如下,下列说法不正确的是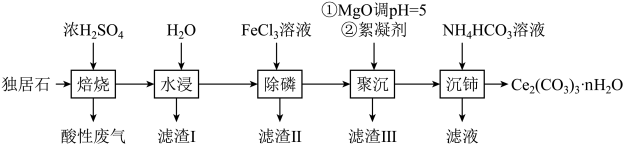
A.滤渣I的主要成分是 和 和 |
B.酸性废气的主要成分为 |
C.加入絮凝剂的目的是促进 和 和 沉淀析出 沉淀析出 |
D.沉铈的方程式为: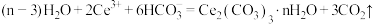 |
您最近一年使用:0次
名校
解题方法
5 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
在一定温度下,利用催化剂将 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:
(1)反应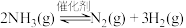

_____  ;
;
(2)已知该反应的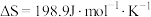 ,在下列哪些温度下反应能自发进行?_____(填标号);
,在下列哪些温度下反应能自发进行?_____(填标号);
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将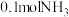 通入
通入 的密闭容器中进行反应(此时容器内总压为
的密闭容器中进行反应(此时容器内总压为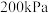 ),各物质的分压随时间的变化曲线如图所示。
),各物质的分压随时间的变化曲线如图所示。 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示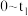 时间内的反应速率
时间内的反应速率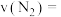
_____  (用含
(用含 的代数式表示);
的代数式表示);
② 时提高反应温度并保持不变,图中能正确表示压缩后
时提高反应温度并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是_____ (用图中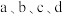 表示)。
表示)。
③在该温度下,反应的标准平衡常数
_____ 。
(已知:分压=总压×该组分物质的量分数,对于反应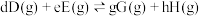 ,
,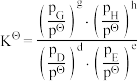 ,其中
,其中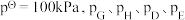 为各组分的平衡分压)。
为各组分的平衡分压)。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氮转化为高纯氢气,其装置如图所示。_____ (填从“A往B”或“从B往A”);
(5)阴极的电极反应式为_____ 。
方法I:氨热分解法制氢气
相关化学键的键能数据
| 化学键 |  |  |  |
键能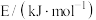 | 946.0 | 436.0 | 390.8 |
 分解为
分解为 和
和 。回答下列问题:
。回答下列问题:(1)反应
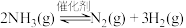

 ;
;(2)已知该反应的
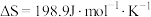 ,在下列哪些温度下反应能自发进行?_____(填标号);
,在下列哪些温度下反应能自发进行?_____(填标号);A. | B.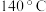 | C.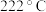 | D.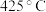 |
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将
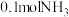 通入
通入 的密闭容器中进行反应(此时容器内总压为
的密闭容器中进行反应(此时容器内总压为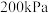 ),各物质的分压随时间的变化曲线如图所示。
),各物质的分压随时间的变化曲线如图所示。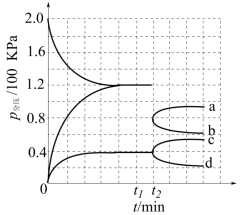
 时反应达到平衡,用
时反应达到平衡,用 的浓度变化表示
的浓度变化表示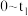 时间内的反应速率
时间内的反应速率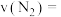
 (用含
(用含 的代数式表示);
的代数式表示);②
 时提高反应温度并保持不变,图中能正确表示压缩后
时提高反应温度并保持不变,图中能正确表示压缩后 分压变化趋势的曲线是
分压变化趋势的曲线是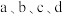 表示)。
表示)。③在该温度下,反应的标准平衡常数

(已知:分压=总压×该组分物质的量分数,对于反应
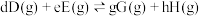 ,
,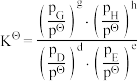 ,其中
,其中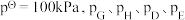 为各组分的平衡分压)。
为各组分的平衡分压)。方法Ⅱ:氨电解法制氢气
利用电解原理,将氮转化为高纯氢气,其装置如图所示。
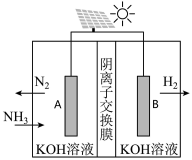
(5)阴极的电极反应式为
您最近一年使用:0次
名校
解题方法
6 . 工业上以铬铁矿( ,含
,含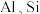 氧化物等杂质)为主要原料制备红矾钠
氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题: 原子的价电子排布图为
原子的价电子排布图为_____
(2)焙烧的目的是将 转化为
转化为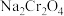 并将
并将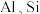 氧化物转化为可溶性钠盐。焙烧时主要发生的化学方程式为
氧化物转化为可溶性钠盐。焙烧时主要发生的化学方程式为_____ 。
(3)浸取时的滤渣主要为_____ ,中和时的滤渣主要为_____ 。
(4)矿物中相关元素可溶性组分物质的量浓度c与 的关系如图所示。当溶液中可溶组分浓度
的关系如图所示。当溶液中可溶组分浓度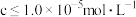 时,可认为已除尽。
时,可认为已除尽。 的理论范围为
的理论范围为_____ ;酸化的目的是_____ 。
(5)奥氏体是碳溶解在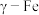 中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示。若该晶胞的棱长为
中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示。若该晶胞的棱长为 ,则晶胞的密度
,则晶胞的密度
_____ (列出含 的计算式),每个
的计算式),每个 原子附近有
原子附近有_____ 个最近且距离相等的C原子。
 ,含
,含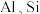 氧化物等杂质)为主要原料制备红矾钠
氧化物等杂质)为主要原料制备红矾钠 的工艺流程如图。回答下列问题:
的工艺流程如图。回答下列问题: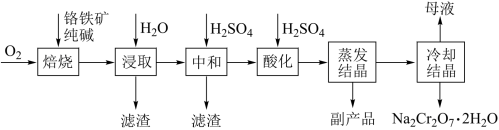
 原子的价电子排布图为
原子的价电子排布图为(2)焙烧的目的是将
 转化为
转化为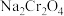 并将
并将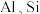 氧化物转化为可溶性钠盐。焙烧时主要发生的化学方程式为
氧化物转化为可溶性钠盐。焙烧时主要发生的化学方程式为(3)浸取时的滤渣主要为
(4)矿物中相关元素可溶性组分物质的量浓度c与
 的关系如图所示。当溶液中可溶组分浓度
的关系如图所示。当溶液中可溶组分浓度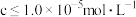 时,可认为已除尽。
时,可认为已除尽。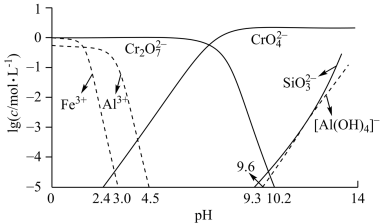
 的理论范围为
的理论范围为(5)奥氏体是碳溶解在
 中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示。若该晶胞的棱长为
中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示。若该晶胞的棱长为 ,则晶胞的密度
,则晶胞的密度
 的计算式),每个
的计算式),每个 原子附近有
原子附近有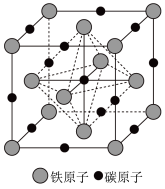
您最近一年使用:0次
名校
解题方法
7 . 某实验小组以 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
可选用试剂: 晶体、
晶体、 溶液、浓
溶液、浓 、稀
、稀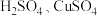 溶液、蒸馏水步骤1:
溶液、蒸馏水步骤1: 的制备
的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。 的含量测定
的含量测定
①称取产品 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的 溶液;
溶液;
③沉淀完全后, 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为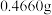 。
。
回答下列问题:
(1)试剂a是_____ (填名称),在试剂a过量并微热时,发生主要反应的化学方程式为_____ 。
(2)Ⅱ中仪器b的名称是_____ ,选取并组装仪器b的作用是_____ 。
(3)加入一定量热的 溶液后,如何判定
溶液后,如何判定 已沉淀完全的方法是
已沉淀完全的方法是_____ 。
(4)在溶液的配置实验中,下列仪器不需要用到的是_____ (填名称)。 的质量分数为
的质量分数为_____ (保留2位小数)。
 溶液为原料制备
溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:可选用试剂:
 晶体、
晶体、 溶液、浓
溶液、浓 、稀
、稀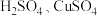 溶液、蒸馏水步骤1:
溶液、蒸馏水步骤1: 的制备
的制备按如图所示装置进行实验,得到
 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。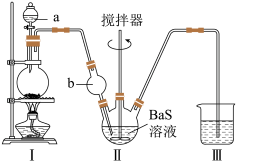
 的含量测定
的含量测定①称取产品
 ,用
,用 水溶解,酸化,加热至近沸;
水溶解,酸化,加热至近沸;②在不断搅拌下,向①所得溶液逐滴加入热的
 溶液;
溶液;③沉淀完全后,
 水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为
水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为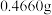 。
。回答下列问题:
(1)试剂a是
(2)Ⅱ中仪器b的名称是
(3)加入一定量热的
 溶液后,如何判定
溶液后,如何判定 已沉淀完全的方法是
已沉淀完全的方法是(4)在溶液的配置实验中,下列仪器不需要用到的是

 的质量分数为
的质量分数为
您最近一年使用:0次
名校
8 . 赖氨酸 ,用
,用 表示]是人体必需氨基酸,其盐酸盐
表示]是人体必需氨基酸,其盐酸盐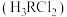 在水溶液中存在如下平衡:
在水溶液中存在如下平衡: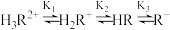 向一定浓度的
向一定浓度的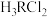 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中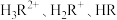 和
和 的分布系数
的分布系数 随
随 变化如图所示。已知
变化如图所示。已知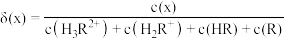 ,下列表述正确的是
,下列表述正确的是
 ,用
,用 表示]是人体必需氨基酸,其盐酸盐
表示]是人体必需氨基酸,其盐酸盐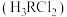 在水溶液中存在如下平衡:
在水溶液中存在如下平衡: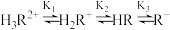 向一定浓度的
向一定浓度的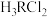 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中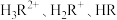 和
和 的分布系数
的分布系数 随
随 变化如图所示。已知
变化如图所示。已知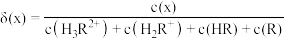 ,下列表述正确的是
,下列表述正确的是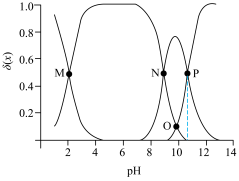
A. 的数量级为 的数量级为 |
B.M点,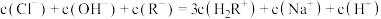 |
C.O点, |
D.N点,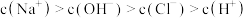 |
您最近一年使用:0次
2024-08-24更新
|
92次组卷
|
2卷引用:湖南省邵阳市第六中学2024届高三下学期高考考前化学冲刺卷(二)
名校
9 . 钒液流电池是一种新型的绿色环保储能系统,工作原理如下图,电池总方程式是:
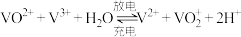 ,下列说法正确的是:
,下列说法正确的是:
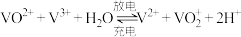 ,下列说法正确的是:
,下列说法正确的是: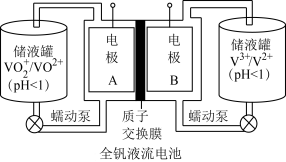
| A.放电时,电极B是负极 |
B.放电时,正极的电极方程式为: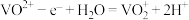 |
C.充电时, 的移动方向是电极 的移动方向是电极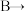 电极A 电极A |
D.充电时,生成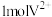 理论上外电路需要转移 理论上外电路需要转移 |
您最近一年使用:0次
10 .  晶胞如下图所示,晶胞棱长为
晶胞如下图所示,晶胞棱长为 ,则下列说法不正确的是
,则下列说法不正确的是
 晶胞如下图所示,晶胞棱长为
晶胞如下图所示,晶胞棱长为 ,则下列说法不正确的是
,则下列说法不正确的是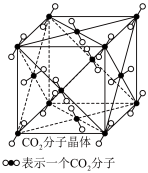
A.一个 晶胞含有4个 晶胞含有4个 分子 分子 |
B. 晶胞中, 晶胞中, 分子的配位数为12 分子的配位数为12 |
C. 晶胞中,两个 晶胞中,两个 分子最近距离为 分子最近距离为 |
D. 晶胞的密度 晶胞的密度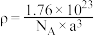 |
您最近一年使用:0次



