1 .  常作有机反应的催化剂。某实验小组拟制备
常作有机反应的催化剂。某实验小组拟制备 并探究其性质。
并探究其性质。
实验(一)制备 。
。
装置如图1所示。已知: 沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。_______ (填“溴水”或“液溴”)。用铁粉替代铁片的目的是_______ 。
(2)装置中利用到的四氯化碳的性质是_______ 。实验完毕后,将烧瓶中混合物经_______ (填实验操作名称)得到 固体。
固体。
实验(二)探究性质。
为了探究的稳定性,进行如图2实验。_______ (填实验现象)时,可以确认 发生分解反应,生成了
发生分解反应,生成了 。
。
(4)实验过程中,先通入一会儿 ,再点燃酒精灯,这样操作的目的是
,再点燃酒精灯,这样操作的目的是_______ 。
(5)为确认玻璃管中残留物有 ,宜选择试剂
,宜选择试剂_______ (填标号)。
a. 溶液 b.酸性
溶液 b.酸性 溶液
溶液
c.KSCN溶液,氯水 d. 溶液
溶液
(6)为了探究浓度对 氧化性的影响,实验操作及现象如下:
氧化性的影响,实验操作及现象如下:
已知: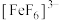 呈无色。
呈无色。
写出实验ⅰ中离子反应方程式:_______ 。
实验ⅱ“不变蓝色”的原因是_______ (结合必要化学用语和文字解释)。
 常作有机反应的催化剂。某实验小组拟制备
常作有机反应的催化剂。某实验小组拟制备 并探究其性质。
并探究其性质。实验(一)制备
 。
。装置如图1所示。已知:
 沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
沸点为58.8℃。实验中,观察到烧瓶中产生红棕色气体。
(2)装置中利用到的四氯化碳的性质是
 固体。
固体。实验(二)探究性质。
为了探究的稳定性,进行如图2实验。
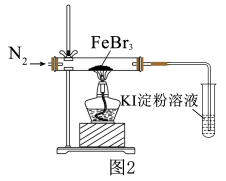
 发生分解反应,生成了
发生分解反应,生成了 。
。(4)实验过程中,先通入一会儿
 ,再点燃酒精灯,这样操作的目的是
,再点燃酒精灯,这样操作的目的是(5)为确认玻璃管中残留物有
 ,宜选择试剂
,宜选择试剂a.
 溶液 b.酸性
溶液 b.酸性 溶液
溶液c.KSCN溶液,氯水 d.
 溶液
溶液(6)为了探究浓度对
 氧化性的影响,实验操作及现象如下:
氧化性的影响,实验操作及现象如下:实验 | 操作 | 现象 |
ⅰ | 向2mL0.1mol 溶液中滴加KI淀粉溶液 溶液中滴加KI淀粉溶液 | 溶液变蓝色 |
ⅱ | 向2mL0.1mol 溶液中先加入适量NaF固体,后滴加KI淀粉溶液 溶液中先加入适量NaF固体,后滴加KI淀粉溶液 | 溶液不变蓝色 |
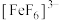 呈无色。
呈无色。写出实验ⅰ中离子反应方程式:
实验ⅱ“不变蓝色”的原因是
您最近一年使用:0次
2024-09-11更新
|
238次组卷
|
2卷引用:湖南省名校联考联合体2025届高三上学期第一次联考(暨入学检测)化学试题
2 . 在水溶液中,EDTA的结构简式为: 。EDTA分子常用
。EDTA分子常用 表示,当溶液中的酸度很高时,
表示,当溶液中的酸度很高时, 分子中的俩个羧酸根可以各在接受一个
分子中的俩个羧酸根可以各在接受一个 而形成
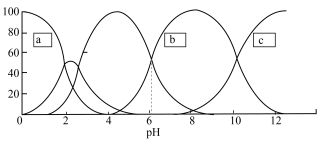
而形成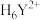 ,这种完全质子化的EDTA相当于一个六元酸,EDTA水溶液中含Y的物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与
,这种完全质子化的EDTA相当于一个六元酸,EDTA水溶液中含Y的物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与 的关系如图所示(pH=2附近
的关系如图所示(pH=2附近 未画出来),已知以
未画出来),已知以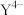 与金属离子形成的配合物最为稳定,下列说法正确的是
与金属离子形成的配合物最为稳定,下列说法正确的是
A.EDTA的分子式为 |
| B.EDTA溶液在pH为1左右时与金属离子形成的配合物最为稳定 |
C.a曲线表示的是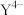 |
D. 的数量级为 的数量级为 |
您最近一年使用:0次
3 . 黄铜矿是一种铜铁硫化物矿物,是炼铜的最主要矿物原料,中国商代或更早就已由黄铜矿等铜矿物炼铜,其最常见的四方晶系晶胞结构如图所示,下列说法错误的是

A.该晶体的化学组成可表示为 |
B.若a原子的分数坐标为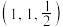 ,则b原子的分数坐标为 ,则b原子的分数坐标为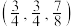 |
| C.基态Cu原子价层电子排布式为3d104s1 |
D.若该晶胞体积为 ,则单位体积含Cu质量的计算式为: ,则单位体积含Cu质量的计算式为: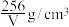 |
您最近一年使用:0次
4 . 我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。CO2的综合利用成为研究的重点。
(1)目前 和
和 已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ: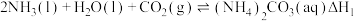
反应Ⅱ: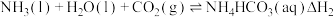
反应Ⅲ:
请问 与
与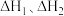 之间的关系是:
之间的关系是:
_______ 。
(2)下列物质中也可能作为CO2捕获剂的是_______。
(3)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比
_______ 。
(4)理论计算表明,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。 变化的曲线分别是
变化的曲线分别是_______ 、_______ 。
(5)根据图中点 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
_______  (列出计算式。以分压表示,分压=总压×物质的量分数)
(列出计算式。以分压表示,分压=总压×物质的量分数)
(1)目前
 和
和 已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:反应Ⅰ:
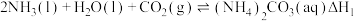
反应Ⅱ:
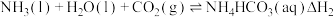
反应Ⅲ:

请问
 与
与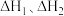 之间的关系是:
之间的关系是:
(2)下列物质中也可能作为CO2捕获剂的是_______。
A. | B. | C. | D. |
(3)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比

(4)理论计算表明,原料初始组成
 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。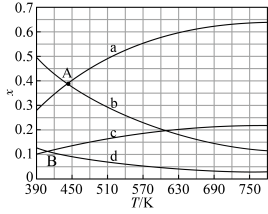
 变化的曲线分别是
变化的曲线分别是(5)根据图中点
 ,计算该温度时反应的平衡常数
,计算该温度时反应的平衡常数
 (列出计算式。以分压表示,分压=总压×物质的量分数)
(列出计算式。以分压表示,分压=总压×物质的量分数)
您最近一年使用:0次
名校
解题方法
5 . 研究含碳和含氮物质的反应对生产、生活、科研等方面具有重要的意义。
回答下列问题:
(1)已知:
i.
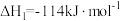
ii.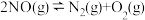

iii.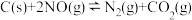
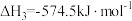
则 与
与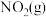 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(2)在保持 、
、 条件下,向反应器中充入
条件下,向反应器中充入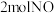 和
和 发生反应i,平衡时
发生反应i,平衡时 的转化率为
的转化率为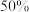 ,欲将平衡转化率降低至
,欲将平衡转化率降低至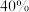 ,需要向反应器中充入
,需要向反应器中充入___________  作为稀释气(计算时不考虑其他反应)。
作为稀释气(计算时不考虑其他反应)。
(3)一定条件下,向起始压强为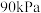 的
的 恒容密闭容器中通入
恒容密闭容器中通入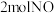 和
和 的混合气体,加入足量焦炭发生上述反应,
的混合气体,加入足量焦炭发生上述反应, 时反应达到平衡,测得体系总压强为
时反应达到平衡,测得体系总压强为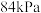 ,
,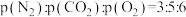 (p为气体分压,单位为
(p为气体分压,单位为 )。
)。
① 的平均反应速率
的平均反应速率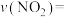
___________  。
。
②下列说法正确的是___________ (填标号)。
A.加入炭块可加快反应速率
B.平衡时充入 ,反应i正向移动
,反应i正向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡状态
③反应i的相对压力平衡常数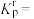
___________ (用分数表示)「已知:将浓度平衡常数表达式中的浓度用相对分压所代替,即为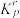 的表达式。气体的相对分压等于其分压除以
的表达式。气体的相对分压等于其分压除以 ]。
]。
(4)某科研小组以耐高温催化剂催化 转化为
转化为 ,测得
,测得 转化为
转化为 的转化率随温度变化情况如图所示。请用平衡移动原理解释加入
的转化率随温度变化情况如图所示。请用平衡移动原理解释加入 后,
后, 转化为
转化为 的转化率增大的原因是
的转化率增大的原因是___________ 。 )为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池如图所示。该固体氧化物电解质的工作温度高达
)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池如图所示。该固体氧化物电解质的工作温度高达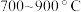 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:___________ 。
回答下列问题:
(1)已知:
i.

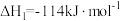
ii.
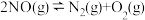

iii.
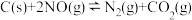
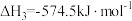
则
 与
与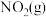 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)在保持
 、
、 条件下,向反应器中充入
条件下,向反应器中充入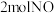 和
和 发生反应i,平衡时
发生反应i,平衡时 的转化率为
的转化率为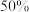 ,欲将平衡转化率降低至
,欲将平衡转化率降低至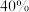 ,需要向反应器中充入
,需要向反应器中充入 作为稀释气(计算时不考虑其他反应)。
作为稀释气(计算时不考虑其他反应)。(3)一定条件下,向起始压强为
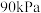 的
的 恒容密闭容器中通入
恒容密闭容器中通入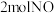 和
和 的混合气体,加入足量焦炭发生上述反应,
的混合气体,加入足量焦炭发生上述反应, 时反应达到平衡,测得体系总压强为
时反应达到平衡,测得体系总压强为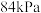 ,
,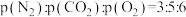 (p为气体分压,单位为
(p为气体分压,单位为 )。
)。①
 的平均反应速率
的平均反应速率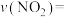
 。
。②下列说法正确的是
A.加入炭块可加快反应速率
B.平衡时充入
 ,反应i正向移动
,反应i正向移动C.混合气体的密度保持不变时,说明反应体系已达到平衡状态
③反应i的相对压力平衡常数
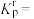
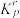 的表达式。气体的相对分压等于其分压除以
的表达式。气体的相对分压等于其分压除以 ]。
]。(4)某科研小组以耐高温催化剂催化
 转化为
转化为 ,测得
,测得 转化为
转化为 的转化率随温度变化情况如图所示。请用平衡移动原理解释加入
的转化率随温度变化情况如图所示。请用平衡移动原理解释加入 后,
后, 转化为
转化为 的转化率增大的原因是
的转化率增大的原因是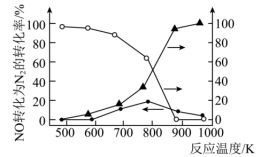
 无
无 时
时 转化为
转化为 的转化率
的转化率

 剩余的百分率
剩余的百分率

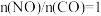 条件下,
条件下, 生成
生成 的转化率
的转化率
 )为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池如图所示。该固体氧化物电解质的工作温度高达
)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池如图所示。该固体氧化物电解质的工作温度高达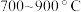 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式:
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。请写出负极电极反应式: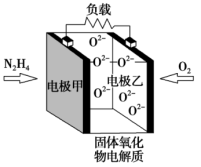
您最近一年使用:0次
6 . 室温下,用 的标准
的标准 溶液滴定
溶液滴定 某浓度的
某浓度的 溶液,滴定过程中溶液pH、分布系数
溶液,滴定过程中溶液pH、分布系数 随滴定分数的变化如图所示。
随滴定分数的变化如图所示。 ;
;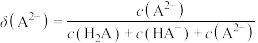 ]
]
下列有关滴定过程说法不正确的是
 的标准
的标准 溶液滴定
溶液滴定 某浓度的
某浓度的 溶液,滴定过程中溶液pH、分布系数
溶液,滴定过程中溶液pH、分布系数 随滴定分数的变化如图所示。
随滴定分数的变化如图所示。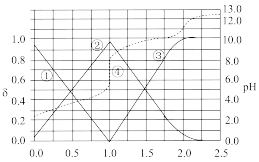
 ;
;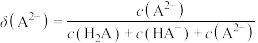 ]
]下列有关滴定过程说法不正确的是
A. 溶液的浓度为 溶液的浓度为 |
B.曲线①代表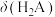 ,曲线③代表 ,曲线③代表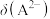 |
C. 的数量级为 的数量级为 |
D.滴定分数为1.5时,溶液中离子浓度大小为: |
您最近一年使用:0次
2024-09-03更新
|
75次组卷
|
2卷引用:2024届湖南省永州市高三第二次模拟考试化学试卷
7 . 室温下,向 和
和 的混合液中滴加
的混合液中滴加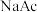 溶液,溶液中
溶液,溶液中 [
[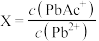 、
、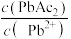 或
或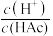 ]与
]与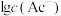 的关系如图所示。
的关系如图所示。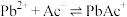
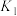 ,
,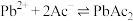
 ,
, 表示醋酸根离子。
表示醋酸根离子。
下列叙述错误的是
 和
和 的混合液中滴加
的混合液中滴加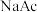 溶液,溶液中
溶液,溶液中 [
[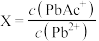 、
、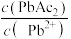 或
或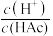 ]与
]与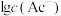 的关系如图所示。
的关系如图所示。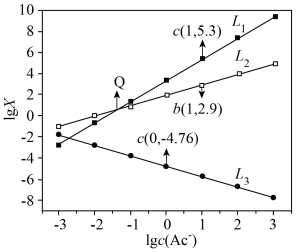
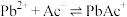
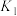 ,
,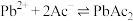
 ,
, 表示醋酸根离子。
表示醋酸根离子。下列叙述错误的是
A.线 代表 代表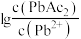 与 与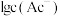 的关系 的关系 |
B.常温下, 的 的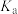 为 为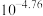 |
C.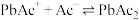 的 的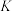 为 为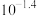 |
D.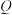 点对应体系中 点对应体系中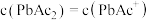 |
您最近一年使用:0次
名校
8 . 某课题组研制了一种具有较高玻璃化转变温度的聚合物P,合成路线如下:
(1)化合物B的名称是_____ ;化合物E的结构简式是_____ 。
(2)B生成C的反应类型为_____ 。
(3)下列说法不正确的是_____。
(4)化合物C生成D的化学方程式是_____ 。
(5)同时满足下列条件的化合物B的同分异构体(不考虑立体异构体)有_____ 种。
①能发生银镜反应
②能和 溶液反应生成
溶液反应生成
(6)以乙醇和丙炔酸为原料,设计如下化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)_____ 。
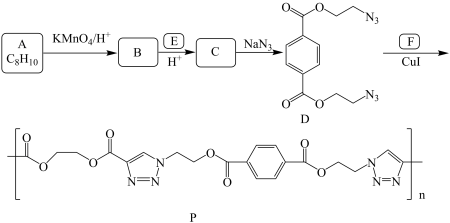
已知: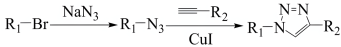
(1)化合物B的名称是
(2)B生成C的反应类型为
(3)下列说法不正确的是_____。
| A.化合物A分子中所有的碳原子一定共平面 |
B.化合物D中O原子的杂化方式均是 |
| C.化合物A的一氯代物仅有2种 |
| D.聚合物P中含氧官能团只有1种 |
(4)化合物C生成D的化学方程式是
(5)同时满足下列条件的化合物B的同分异构体(不考虑立体异构体)有
①能发生银镜反应
②能和
 溶液反应生成
溶液反应生成
(6)以乙醇和丙炔酸为原料,设计如下化合物的合成路线(用流程图表示,无机试剂、有机溶剂任选)
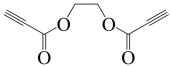
您最近一年使用:0次
名校
解题方法
9 . 一定温度下, 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中
溶液中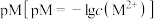 随pH的变化如图1,
随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。
 均为难溶物;②初始
均为难溶物;②初始 。
。
下列说法错误的是
 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中
溶液中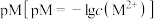 随pH的变化如图1,
随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。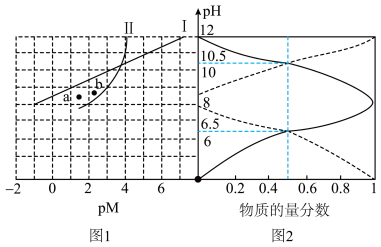
 均为难溶物;②初始
均为难溶物;②初始 。
。下列说法错误的是
A.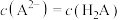 时, 时, |
B.初始状态a点发生反应: |
C.Ⅰ曲线上的点满足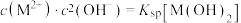 |
D.初始状态的b点,平衡后溶液中存在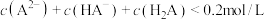 |
您最近一年使用:0次
2024-08-08更新
|
275次组卷
|
4卷引用:湖南省长沙市雅礼中学2024-2025学年高三上学期入学考试化学试题
10 . 常温下,向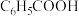 、
、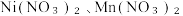 的混合溶液中滴加NaOH溶液,溶液中pX
的混合溶液中滴加NaOH溶液,溶液中pX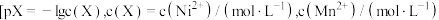 与pH的关系如图所示,下列叙述正确的是
与pH的关系如图所示,下列叙述正确的是
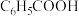 、
、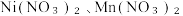 的混合溶液中滴加NaOH溶液,溶液中pX
的混合溶液中滴加NaOH溶液,溶液中pX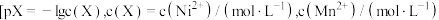 与pH的关系如图所示,下列叙述正确的是
与pH的关系如图所示,下列叙述正确的是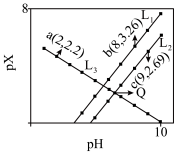
A.L1代表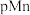 和pH的关系 和pH的关系 |
B.苯甲酸的 为 为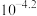 |
C.反应 的化学平衡常数K为 的化学平衡常数K为 |
| D.Q点坐标为(5.65,-1.45) |
您最近一年使用:0次
2024-07-26更新
|
243次组卷
|
4卷引用:湖南省衡阳县第一中学2025届高三上学期开学考试化学试卷



