1 . 由于温室效应和资源短缺等问题,如何降低大气中的 含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用
含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应:

 ,如图表示该反应进行过程中能量(单位为
,如图表示该反应进行过程中能量(单位为 )的变化。
)的变化。
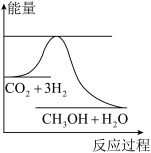
(1)该反应平衡常数K的表达式为_______________ 。
(2)温度降低,平衡常数K__________ (填“增大”、“不变”或“减小”)。
(3)在体积为1L的恒容密闭容器中,充入1mol 和3mol
和3mol ,测得
,测得 和
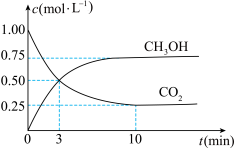
和 的浓度随时间变化如图所示。从反应开始到平衡,用
的浓度随时间变化如图所示。从反应开始到平衡,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率 为
为__________  ,
, 的转化率为
的转化率为__________ ,平衡常数
__________ 。
(4)下列措施中能使(3)题中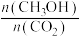 增大的有__________。(填字母)
增大的有__________。(填字母)
 含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用
含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应:
 ,如图表示该反应进行过程中能量(单位为
,如图表示该反应进行过程中能量(单位为 )的变化。
)的变化。
(1)该反应平衡常数K的表达式为
(2)温度降低,平衡常数K
(3)在体积为1L的恒容密闭容器中,充入1mol
 和3mol
和3mol ,测得
,测得 和
和 的浓度随时间变化如图所示。从反应开始到平衡,用
的浓度随时间变化如图所示。从反应开始到平衡,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率 为
为 ,
, 的转化率为
的转化率为

(4)下列措施中能使(3)题中
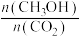 增大的有__________。(填字母)
增大的有__________。(填字母)| A.降低温度 | B.加入催化剂 |
C.将 从体系中分离 从体系中分离 | D.充入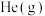 ,使体系总压强增大 ,使体系总压强增大 |
您最近一年使用:0次
2022-11-27更新
|
239次组卷
|
2卷引用:贵州省部分学校2022-2023学年高二上学期10月联考化学试题
解题方法
2 . 回答下列问题:
(1)在密闭容器中发生如下反应: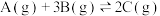
 ,根据下列速率-时间图像,回答下列问题:
,根据下列速率-时间图像,回答下列问题:
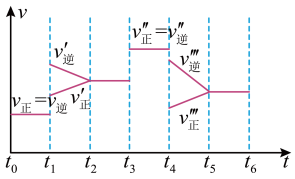
(1)下列时刻所改变的外界条件是:
__________ ;
__________ ;
__________ 。
(2)产物C的体积分数最大的时间段是__________ 。
(3)上述图像中C的体积分数相等的两个时间段是_______________ 。
(4)反应速率最快的时间段是__________ 。
(2)在 的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)
的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)
①在溶液中加入少量的 固体,平衡
固体,平衡__________ 移动。
②在溶液中加入少量的 固体,平衡
固体,平衡__________ 移动。
③在溶液中加入少量的 固体,平衡
固体,平衡__________ 移动,理由是:_____________ 。
(1)在密闭容器中发生如下反应:
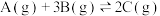
 ,根据下列速率-时间图像,回答下列问题:
,根据下列速率-时间图像,回答下列问题:
(1)下列时刻所改变的外界条件是:



(2)产物C的体积分数最大的时间段是
(3)上述图像中C的体积分数相等的两个时间段是
(4)反应速率最快的时间段是
(2)在
 的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)
的平衡体系中,回答下列问题:(填“正向”、“逆向”、“不”)①在溶液中加入少量的
 固体,平衡
固体,平衡②在溶液中加入少量的
 固体,平衡
固体,平衡③在溶液中加入少量的
 固体,平衡
固体,平衡
您最近一年使用:0次
2022-11-27更新
|
174次组卷
|
2卷引用:贵州省部分学校2022-2023学年高二上学期10月联考化学试题
解题方法
3 . 根据所给信息,回答下列问题。
(1)11.2L(标准状况) 在足量
在足量 中燃烧生成
中燃烧生成 气体,放出91.5kJ热量,其热化学方程式为
气体,放出91.5kJ热量,其热化学方程式为_____________ 。
(2)甲烷的燃烧热为 ,则甲烷燃烧热的热化学方程式可表示为
,则甲烷燃烧热的热化学方程式可表示为_____________________________ 。
(3)25℃时,1L0.5mol/L的 溶液和足量稀硫酸反应,放出28.65kJ的热量,则该反应的热化学方程式为
溶液和足量稀硫酸反应,放出28.65kJ的热量,则该反应的热化学方程式为__________________ 。
(4)以 、
、 为原料生产尿素
为原料生产尿素 的反应历程与能量变化示意图如下。
的反应历程与能量变化示意图如下。
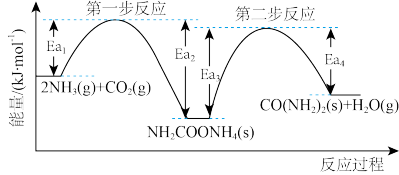
①第一步反应的热化学方程式为_____________________________ 。
②第二步反应的
__________ 0(填“>”、“<”或“=”)。
③从图象分析决定生产尿素的总反应的反应速率的步骤的是第__________ 步反应。被还原为S。
(5)在化工生产过程中,少量 的存在会引起催化剂中毒。为了防止催化剂中毒,用
的存在会引起催化剂中毒。为了防止催化剂中毒,用 将
将 氧化,
氧化, 被还原为S。
被还原为S。
已知:①
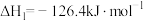
②
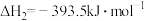
③
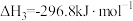
则 氧化
氧化 的热化学方程式为
的热化学方程式为__________________________ 。
(1)11.2L(标准状况)
 在足量
在足量 中燃烧生成
中燃烧生成 气体,放出91.5kJ热量,其热化学方程式为
气体,放出91.5kJ热量,其热化学方程式为(2)甲烷的燃烧热为
 ,则甲烷燃烧热的热化学方程式可表示为
,则甲烷燃烧热的热化学方程式可表示为(3)25℃时,1L0.5mol/L的
 溶液和足量稀硫酸反应,放出28.65kJ的热量,则该反应的热化学方程式为
溶液和足量稀硫酸反应,放出28.65kJ的热量,则该反应的热化学方程式为(4)以
 、
、 为原料生产尿素
为原料生产尿素 的反应历程与能量变化示意图如下。
的反应历程与能量变化示意图如下。
①第一步反应的热化学方程式为
②第二步反应的

③从图象分析决定生产尿素的总反应的反应速率的步骤的是第
(5)在化工生产过程中,少量
 的存在会引起催化剂中毒。为了防止催化剂中毒,用
的存在会引起催化剂中毒。为了防止催化剂中毒,用 将
将 氧化,
氧化, 被还原为S。
被还原为S。已知:①

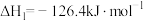
②

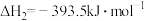
③

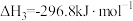
则
 氧化
氧化 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
2022-11-27更新
|
305次组卷
|
2卷引用:贵州省部分学校2022-2023学年高二上学期10月联考化学试题
4 . 回答下列问题
(1)在400℃时,将一定量的AB2和14molB2压入一个盛有催化剂的10L密闭容器中进行反应:2AB2+B2 2AB3,已知2min后,容器中剩余2molAB2和12molB2,则:
2AB3,已知2min后,容器中剩余2molAB2和12molB2,则:
①反应中消耗了_______ molAB2,2min后AB3的物质的量浓度是_______ 。
②2min内平均反应速率:v(B2)=_______ 。
③发生反应前容器内压强与发生反应后容器中压强比值为:_______ 。
(2)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。_______ 。
②由图中所给数据进行分析,该反应的化学方程式为_______ 。
③若三种物质都是气体,则平衡时X所占体积的百分比为_______ 。
(1)在400℃时,将一定量的AB2和14molB2压入一个盛有催化剂的10L密闭容器中进行反应:2AB2+B2
 2AB3,已知2min后,容器中剩余2molAB2和12molB2,则:
2AB3,已知2min后,容器中剩余2molAB2和12molB2,则:①反应中消耗了
②2min内平均反应速率:v(B2)=
③发生反应前容器内压强与发生反应后容器中压强比值为:
(2)某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
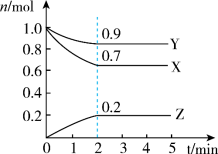
②由图中所给数据进行分析,该反应的化学方程式为
③若三种物质都是气体,则平衡时X所占体积的百分比为
您最近一年使用:0次
2022-10-25更新
|
443次组卷
|
3卷引用:贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题
贵州省黔西南州金成实验学校2022-2023学年高二上学期9月月考化学试题湖南省长沙市芙蓉高级中学2022-2023学年高二上学期期中考试化学试题(已下线)专题突破卷09 化学反应速率与化学平衡(一)-2025年高考化学一轮复习考点通关卷(新高考通用)
名校
解题方法
5 . 已知: 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
(1)若镁条在 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为_______ 。
(2)若常温下, 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为_______ 。
(3)若向酸性 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为_______ ;向烧碱溶液中通入过量 的离子方程式为
的离子方程式为_______ 。
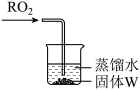
(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为_______ ,向某密闭容器中充入 和
和 ,则产物的分子数
,则产物的分子数_______ (填“大于”、“小于”或“等于”)2NA。
(5)若 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有_______ 性而能杀菌消毒;工业上,常用+5价R的含氧酸的钠盐和HR的浓溶液在常温下反应制备气态 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为_______ 。
 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:(1)若镁条在
 中燃烧生成黑色粉末(单质)和白色粉末,则
中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为
的化学式为(2)若常温下,
 能与氢氟酸反应生成一种气体和一种液态化合物。
能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生成R的含氧酸盐,
和纯碱混合在铁坩埚中熔融生成R的含氧酸盐, 和纯碱反应的化学方程式为
和纯碱反应的化学方程式为(3)若向酸性
 溶液、含酚酞的烧碱溶液中分别通入无色气体
溶液、含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
,两溶液颜色均逐渐褪去。酸性 溶液吸收
溶液吸收 的离子方程式为
的离子方程式为 的离子方程式为
的离子方程式为(4)设NA为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入
 ,固体W逐渐溶解(如图所示),则
,固体W逐渐溶解(如图所示),则 的化学式为
的化学式为 和
和 ,则产物的分子数
,则产物的分子数
(5)若
 是一种绿色饮用水消毒剂,则
是一种绿色饮用水消毒剂,则 具有
具有 ,同时还有R单质和水生成,该反应的离子方程式为
,同时还有R单质和水生成,该反应的离子方程式为
您最近一年使用:0次
2022-10-10更新
|
258次组卷
|
5卷引用:贵州省毕节市金沙县2022-2023学年高三上学期期中教学质量检测化学试题
名校
6 . 现有下列物质:①生石灰 ② 固体 ③浓
固体 ③浓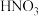 ④单质铁 ⑤
④单质铁 ⑤ ⑥熔融
⑥熔融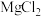 ⑦石墨 ⑧蔗糖晶体 ⑨
⑦石墨 ⑧蔗糖晶体 ⑨ 固体 ⑩
固体 ⑩ 固体。请填空:
固体。请填空:
(1)上述状态下可导电的物质是_______ (填标号,下同),属于电解质的是_______ 。
(2)上述物质中属于碱性氧化物的是_______ (填化学式),原因为_______ (请用化学方程式说明)。
(3)⑥的电离方程式为_______ ,⑩溶于水时的电离方程式为_______ 。
(4)②的水溶液与④反应的离子方程式为_______ ,②与⑨的水溶液混合后,溶液恰好呈中性,发生反应的离子方程式为_______ 。
 固体 ③浓
固体 ③浓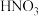 ④单质铁 ⑤
④单质铁 ⑤ ⑥熔融
⑥熔融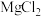 ⑦石墨 ⑧蔗糖晶体 ⑨
⑦石墨 ⑧蔗糖晶体 ⑨ 固体 ⑩
固体 ⑩ 固体。请填空:
固体。请填空:(1)上述状态下可导电的物质是
(2)上述物质中属于碱性氧化物的是
(3)⑥的电离方程式为
(4)②的水溶液与④反应的离子方程式为
您最近一年使用:0次
2022-10-10更新
|
459次组卷
|
4卷引用:贵州省部分学校2022-2023学年高一上学期期中联合考试化学试题
7 . 根据题意解答
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_______ 。
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______ 。
(3)Cu与稀硝酸反应制备NO的离子方程式_______ 。
(4)实验室常用铵盐和碱的混合物制取氨气,写出化学方程式_______
(5)设计实验检验铵盐溶液中的阳离子,写出实验操作、现象和结论。_______ 。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:
(3)Cu与稀硝酸反应制备NO的离子方程式
(4)实验室常用铵盐和碱的混合物制取氨气,写出化学方程式
(5)设计实验检验铵盐溶液中的阳离子,写出实验操作、现象和结论。
您最近一年使用:0次
8 . 完成下列问题。
(1)现有下列4种物质:①NH3;②浓硝酸;③浓硫酸;④NO。其中,遇空气迅速变成红棕色的气体是_______ (填序号,下同),能使湿润的红色石蕊试纸变蓝的气体是_______ ,加入蔗糖产生“黑面包”现象的溶液是_______ ,常温下,能用铁制容器盛放的溶液是_______ 。
(2)将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
①用稀硝酸制取一氧化氮_______ 。
②常温下用铁制或铝制容器贮存、运输浓HNO3_______ 。
③久置的浓硝酸变黄色_______ 。
(1)现有下列4种物质:①NH3;②浓硝酸;③浓硫酸;④NO。其中,遇空气迅速变成红棕色的气体是
(2)将硝酸表现出的性质填在下列各反应操作或现象后:
A.氧化性 B.酸性 C.还原性 D.不稳定性
①用稀硝酸制取一氧化氮
②常温下用铁制或铝制容器贮存、运输浓HNO3
③久置的浓硝酸变黄色
您最近一年使用:0次
9 . 如图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合的。
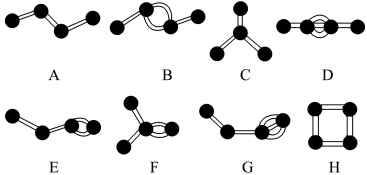
(1)图中属于链状烷烃的是_______ (填字母)。
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成_______ 和_______ ;不仅可以形成_______ ,还可以形成碳环。
(3)上图中互为同分异构体的是A与_______ ;D与_______ 。(填字母)

(1)图中属于链状烷烃的是
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成
(3)上图中互为同分异构体的是A与
您最近一年使用:0次
10 . 分析下列烃分子,按要求作答。
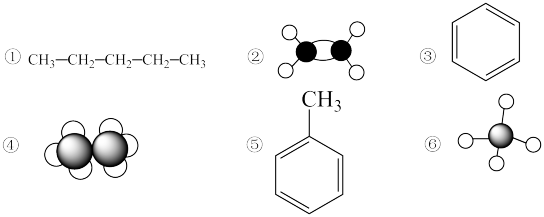
(1)互为同系物且为链烃的是_______ ;(填序号)
(2)②在一定条件下与水反应的化学方程式为:_______ ;
(3)②在一定条件下与溴的CCl4反应的化学方程式为:_______ ;
(4)④的二氯代物有_______ 种。写出②的结构式:_______ ;
(5)写出的⑤分子式:_______ ;写出①的同分异构体的结构简式:_______ ;

(1)互为同系物且为链烃的是
(2)②在一定条件下与水反应的化学方程式为:
(3)②在一定条件下与溴的CCl4反应的化学方程式为:
(4)④的二氯代物有
(5)写出的⑤分子式:
您最近一年使用:0次



