名校
解题方法
1 . I.化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是___________ (填序号)。写出d的化学方程式___________ 。
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合
d氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸和镁的反应
(2)下列图像分别表示有关反应的反应过程与能量变化的关系。___________ (填序号)。
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
c. 和
和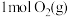 具有的总能量小于
具有的总能量小于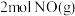 具有的总能量
具有的总能量
Ⅱ.如下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
(3)当电解质溶液为稀硫酸时,a上有气泡产生,说明a为___________ 极,金属性a___________ b(填“<”或“>”)
(4)当电极a为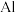 ,电极b为
,电极b为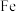 ,电解质溶液为
,电解质溶液为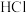 溶液时,该电池的负极反应式为
溶液时,该电池的负极反应式为___________ 。当反应中收集到标准状况下 气体时,消耗负极的物质的量为
气体时,消耗负极的物质的量为___________ 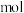 。
。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合
d氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸和镁的反应
(2)下列图像分别表示有关反应的反应过程与能量变化的关系。
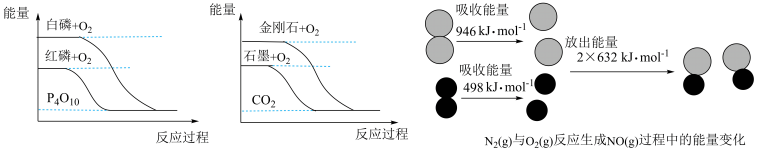
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
c.
 和
和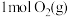 具有的总能量小于
具有的总能量小于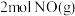 具有的总能量
具有的总能量Ⅱ.如下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
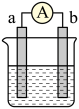
(3)当电解质溶液为稀硫酸时,a上有气泡产生,说明a为
(4)当电极a为
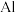 ,电极b为
,电极b为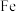 ,电解质溶液为
,电解质溶液为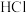 溶液时,该电池的负极反应式为
溶液时,该电池的负极反应式为 气体时,消耗负极的物质的量为
气体时,消耗负极的物质的量为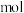 。
。
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分,请参照元素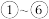 的位置回答下列问题:
的位置回答下列问题:_______ 。
(2)元素②和③组成的化合物有_______ 、_______ (填化学式)。
(3)上述元素中,原子半径最大的是_______ (填元素符号)。
(4)下列说法正确的是_______ (填字母标号)。
a.④的最高价氧化物为两性氧化物
b.非金属性: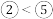
c.⑥在化合物中呈现的最高化合价为 价
价
(5)34号元素硒 和元素⑤位于同一主族,是生命必需元素,硒酸
和元素⑤位于同一主族,是生命必需元素,硒酸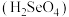 的酸性比硫酸
的酸性比硫酸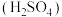
_______ (填“强”或“弱”),请从“位—构—性”角度分析原因_______ 。
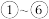 的位置回答下列问题:
的位置回答下列问题: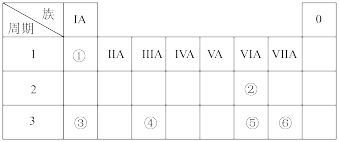
(2)元素②和③组成的化合物有
(3)上述元素中,原子半径最大的是
(4)下列说法正确的是
a.④的最高价氧化物为两性氧化物
b.非金属性:
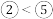
c.⑥在化合物中呈现的最高化合价为
 价
价(5)34号元素硒
 和元素⑤位于同一主族,是生命必需元素,硒酸
和元素⑤位于同一主族,是生命必需元素,硒酸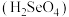 的酸性比硫酸
的酸性比硫酸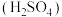
您最近一年使用:0次
名校
解题方法
3 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题: 的化学方程式是
的化学方程式是_______ 。
(2) 的电离方程式是
的电离方程式是_______ 。
(3)样液中加入 后产生氧气,说明
后产生氧气,说明 与水反应的过程中还生成了
与水反应的过程中还生成了_______ (化学式)。
(4)用该方法制备的 中含有碳酸钠。生成白色沉淀的离子方程式是
中含有碳酸钠。生成白色沉淀的离子方程式是_______ 。
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
 的化学方程式是
的化学方程式是(2)
 的电离方程式是
的电离方程式是(3)样液中加入
 后产生氧气,说明
后产生氧气,说明 与水反应的过程中还生成了
与水反应的过程中还生成了(4)用该方法制备的
 中含有碳酸钠。生成白色沉淀的离子方程式是
中含有碳酸钠。生成白色沉淀的离子方程式是
您最近一年使用:0次
名校
解题方法
4 . 合成氨N2(g)+3H2(g) 2NH3(g)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
2NH3(g)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氢原子中,核外电子的电子云轮廓图形状为___________ 。
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ 。
②N2、H2、NH3三个物质的沸点由高到低的顺序为:___________
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ (填元素符号)。
②Al2O3有晶体和非晶体形态,区分这两种形态最可靠的科学方法为:___________
(4)下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
请从原子结构的角度解释Mg的第一电离能大于Al:___________
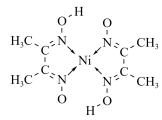
(5)在稀氨水介质中丁二酮肟常用于检验Ni2+,丁二酮肟与Ni2+反应可生成鲜红色沉淀,该沉淀结构如图所示___________ 。
 2NH3(g)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
2NH3(g)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②N2、H2、NH3三个物质的沸点由高到低的顺序为:
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、CaO、MgO、
、CaO、MgO、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②Al2O3有晶体和非晶体形态,区分这两种形态最可靠的科学方法为:
(4)下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
电离能 | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(5)在稀氨水介质中丁二酮肟常用于检验Ni2+,丁二酮肟与Ni2+反应可生成鲜红色沉淀,该沉淀结构如图所示
您最近一年使用:0次
名校
解题方法
5 . 按要求回答下列问题:
(1)为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。_______ ,产生此现象的化学方程式为_______ 。
②轻轻摇动烧瓶,观察到烧瓶中的现象为____ 、___ 。产生此现象的化学方程式为____ 。
(2)某学生课外活动小组利用图所示装置分别做如下实验:___ 溶液;加热时溶液由红色逐渐变浅的原因是:_______ 。
②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是_______ 溶液;加热时溶液由无色变为红色的原因是:_______ 。
(1)为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
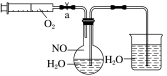
②轻轻摇动烧瓶,观察到烧瓶中的现象为
(2)某学生课外活动小组利用图所示装置分别做如下实验:
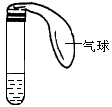
②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是
您最近一年使用:0次
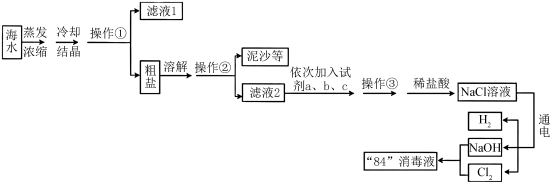
6 . “84”消毒液是一种主要用于物体表面和环境的消毒剂。用海水模拟制备“84”消毒液的流程如图。请回答下列问题: 、
、 、
、 、
、 ;
;
②除杂试剂均过量。
(1)操作①为_______ ,该操作需要的玻璃仪器有玻璃棒、_______ ;向滤液2中依次加入的试剂a、b、c可以是_______ (填标号)。
A.NaOH溶液、 溶液、
溶液、 溶液
溶液
B. 溶液、
溶液、 溶液、NaOH溶液
溶液、NaOH溶液
C. 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液
溶液
(2)操作③结束后往滤液中加入稀盐酸的目的是_______ ;NaCl溶液通电后生成 、
、 、NaOH的化学方程式为
、NaOH的化学方程式为_______ 。
(3) 与NaOH溶液反应制备“84”消毒液的化学方程式为
与NaOH溶液反应制备“84”消毒液的化学方程式为_______ ;每转移1mol电子,生成的氧化产物的质量为_______ g。
 、
、 、
、 、
、 ;
;②除杂试剂均过量。
(1)操作①为
A.NaOH溶液、
 溶液、
溶液、 溶液
溶液B.
 溶液、
溶液、 溶液、NaOH溶液
溶液、NaOH溶液C.
 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液
溶液(2)操作③结束后往滤液中加入稀盐酸的目的是
 、
、 、NaOH的化学方程式为
、NaOH的化学方程式为(3)
 与NaOH溶液反应制备“84”消毒液的化学方程式为
与NaOH溶液反应制备“84”消毒液的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 某同学用如图所示的装置进行二氧化硫的制备与性质探究。回答下列问题: 的化学方程式为
的化学方程式为_______ 。
(2)可抽动铜丝的优点为_______ 。
(3)实验过程中,观察到品红溶液褪色,说明 具有
具有_______ 性。
(4)欲探究 是否具有还原性,可选用
是否具有还原性,可选用_______ (填标号)。
a. 溶液 b.浓硫酸 c.
溶液 b.浓硫酸 c. 溶液 d.酸性高锰酸钾溶液
溶液 d.酸性高锰酸钾溶液
(5)反应结束后取D中溶液进行如下图所示实验。产生淡黄色沉淀的原因为_______ (用离子方程式表示),说明 具有
具有_______ 性。_______ 。
②能证明亚硫酸酸性强于碳酸的实验现象是_______ 。
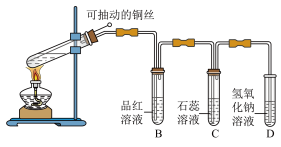
 的化学方程式为
的化学方程式为(2)可抽动铜丝的优点为
(3)实验过程中,观察到品红溶液褪色,说明
 具有
具有(4)欲探究
 是否具有还原性,可选用
是否具有还原性,可选用a.
 溶液 b.浓硫酸 c.
溶液 b.浓硫酸 c. 溶液 d.酸性高锰酸钾溶液
溶液 d.酸性高锰酸钾溶液(5)反应结束后取D中溶液进行如下图所示实验。产生淡黄色沉淀的原因为
 具有
具有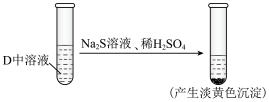
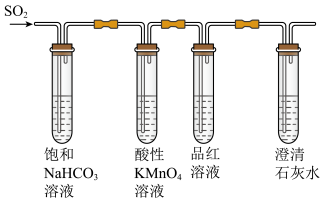
②能证明亚硫酸酸性强于碳酸的实验现象是
您最近一年使用:0次
名校
解题方法
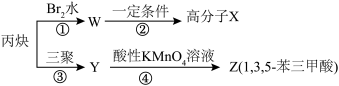
8 . 丙炔可以发生下列物质转化,结合已知信息,回答下列问题:
(2)写出 的顺式结构:
的顺式结构:______ 。①的反应类型:______ 。
(3)物质 是丙炔的同系物且同时满足以下三个条件,写出
是丙炔的同系物且同时满足以下三个条件,写出 的系统命名
的系统命名______ 。
①质谱图中最大质荷比为82;②主链4个碳;③分子中存在三个甲基。
(4)物质 的一氯代物有
的一氯代物有______ 种,物质 完全氢化后的产物核磁共振氢谱的峰面积比为
完全氢化后的产物核磁共振氢谱的峰面积比为______ 。
(5)分子式为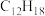 与物质
与物质 互为同系物,且只有一个侧链,写出所有不能被酸性
互为同系物,且只有一个侧链,写出所有不能被酸性 溶液氧化成苯甲酸的结构简式:
溶液氧化成苯甲酸的结构简式:______ 。(已知:若苯的同系物侧链的烷基中,直接与苯环连接的碳原子上没有 ,则该物质一般不能被酸性
,则该物质一般不能被酸性 溶液氧化成苯甲酸。)
溶液氧化成苯甲酸。)
已知:①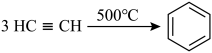
②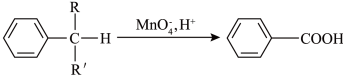 (
( 、
、  表示烷基或氢原子)
表示烷基或氢原子)
A.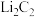 | B. | C. | D.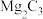 |
(2)写出
 的顺式结构:
的顺式结构:(3)物质
 是丙炔的同系物且同时满足以下三个条件,写出
是丙炔的同系物且同时满足以下三个条件,写出 的系统命名
的系统命名①质谱图中最大质荷比为82;②主链4个碳;③分子中存在三个甲基。
(4)物质
 的一氯代物有
的一氯代物有 完全氢化后的产物核磁共振氢谱的峰面积比为
完全氢化后的产物核磁共振氢谱的峰面积比为(5)分子式为
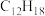 与物质
与物质 互为同系物,且只有一个侧链,写出所有不能被酸性
互为同系物,且只有一个侧链,写出所有不能被酸性 溶液氧化成苯甲酸的结构简式:
溶液氧化成苯甲酸的结构简式: ,则该物质一般不能被酸性
,则该物质一般不能被酸性 溶液氧化成苯甲酸。)
溶液氧化成苯甲酸。)
您最近一年使用:0次
名校
9 . 氮及其化合物在农业、医药、国防等领域应用广泛。请回答下列问题
(1)实验室加热 和
和 固体混合物制取
固体混合物制取 ,反应的化学方程式是
,反应的化学方程式是___________ 。
(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。 ,说明
,说明 具有
具有___________ (填“氧化性”或“还原性”)。
②氧化炉中 转化为NO,发生反应的化学方程式是
转化为NO,发生反应的化学方程式是___________ 。
③吸收塔中NO最终可转化为 。通入空气是为了提供
。通入空气是为了提供___________ (填字母)。
A. B.
B. C.
C.
④尾气处理装置中,可用 将尾气中
将尾气中 还原为
还原为 。反应的化学方程式是
。反应的化学方程式是___________ 。
(1)实验室加热
 和
和 固体混合物制取
固体混合物制取 ,反应的化学方程式是
,反应的化学方程式是(2)工业合成氨及氨氧化制取硝酸的流程示意图如下。
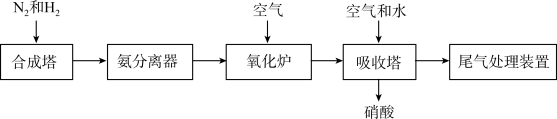
 ,说明
,说明 具有
具有②氧化炉中
 转化为NO,发生反应的化学方程式是
转化为NO,发生反应的化学方程式是③吸收塔中NO最终可转化为
 。通入空气是为了提供
。通入空气是为了提供A.
 B.
B. C.
C.
④尾气处理装置中,可用
 将尾气中
将尾气中 还原为
还原为 。反应的化学方程式是
。反应的化学方程式是
您最近一年使用:0次
名校
解题方法
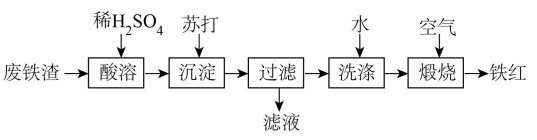
10 . 铁红可用于油漆、油墨、橡胶等工业中,可作为玻璃、宝石、金属的抛光剂等。某课外活动小组用废铁渣(含Fe和少量Fe2O3)制取铁红,所设计的流程如下:
(1)苏打中的化学键类型为___________ ;沉淀的化学式为___________ ;“滤液”中主要溶质的化学式为___________ 。
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是___________ (名称);若溶液中检测不到Fe3+的原因是___________ 。
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为___________ 。
(4)实验室过滤所需的玻璃仪器(填名称)有___________ 。
(5)煅烧的化学方程式为___________ 。
(1)苏打中的化学键类型为
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为
(4)实验室过滤所需的玻璃仪器(填名称)有
(5)煅烧的化学方程式为
您最近一年使用:0次



