2024高三·全国·专题练习
1 . 设NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2022·全国卷) 溶液中,
溶液中, 的数目为
的数目为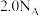
B.(2022·全国卷)电解熔融 ,阴极增重
,阴极增重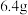 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷) 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)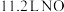 与
与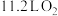 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
A.(2022·全国卷)
 溶液中,
溶液中, 的数目为
的数目为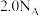
B.(2022·全国卷)电解熔融
 ,阴极增重
,阴极增重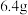 ,外电路中通过电子的数目为
,外电路中通过电子的数目为
C.(2022·浙江卷)
 和
和 于密闭容器中充分反应后,
于密闭容器中充分反应后, 分子总数为
分子总数为
D.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
E.(2021·河北卷)电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为NA
F.(2021·广东卷)
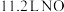 与
与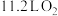 混合后的分子数目为
混合后的分子数目为
G.(2021·浙江卷)0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
您最近一年使用:0次
2024高三·全国·专题练习
2 . 用 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是_______ 。
A.(2023·广东卷) 和
和 的混合物中含
的混合物中含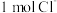 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷) 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷) 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
 表示阿伏加德罗常数的值,下列叙述错误的是
表示阿伏加德罗常数的值,下列叙述错误的是A.(2023·广东卷)
 和
和 的混合物中含
的混合物中含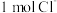 ,则混合物中质子数为
,则混合物中质子数为
B.(2022·浙江卷)
 乙烷和丙烯的混合气体中所含碳氢键数为
乙烷和丙烯的混合气体中所含碳氢键数为
C.(2021·河北卷)1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NA
D.(2021·湖南卷)
 与
与 在密闭容器中充分反应后的分子数为
在密闭容器中充分反应后的分子数为
E.(2021·浙江卷)CH4和C2H4混合气体2.24L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA
您最近一年使用:0次
2024高三·全国·专题练习
3 . NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g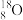 中含有的中子数为NA
中含有的中子数为NA
D.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g
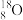 中含有的中子数为NA
中含有的中子数为NAD.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
您最近一年使用:0次
2024高三·全国·专题练习
4 . NA为阿伏加德罗常数的值。下列说法错误的是_______ 。
A.(2023·全国甲卷) 的
的 溶液中
溶液中 的数目为
的数目为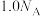
B.(2023·海南卷)5.6g铁粉与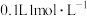 的HCl的溶液充分反应,产生的气体分子数目为
的HCl的溶液充分反应,产生的气体分子数目为
C.(2023·浙江6月)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.(2023·广东卷)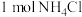 含有的共价键数目为
含有的共价键数目为
E.(2023·辽宁卷)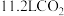 含
含 键数目为
键数目为
F.(2022·全国甲卷)25℃、101kPa下,28L氢气中质子的数目为2.5NA
G.(2021·天津卷)1L1mol/LHCl溶液中,HCl分子的数目为NA
H.(2023·全国甲卷)标准状况下, 中电子的数目为
中电子的数目为
I.(2022·辽宁卷)pH=12的Na2CO3溶液中OH-数目为0.01NA
J.(2021·福建卷)1.12L C2H4所含极性共价键的数目为0.2NA
K.0.1mol·L-1 HClO4溶液中含有的H+数为0.1NA
L.(2021·广东卷)11.2LNO与11.2LO2混合后的分子数目为NA
M.(2022·浙江6月)11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
A.(2023·全国甲卷)
 的
的 溶液中
溶液中 的数目为
的数目为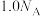
B.(2023·海南卷)5.6g铁粉与
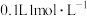 的HCl的溶液充分反应,产生的气体分子数目为
的HCl的溶液充分反应,产生的气体分子数目为
C.(2023·浙江6月)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
D.(2023·广东卷)
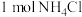 含有的共价键数目为
含有的共价键数目为
E.(2023·辽宁卷)
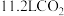 含
含 键数目为
键数目为
F.(2022·全国甲卷)25℃、101kPa下,28L氢气中质子的数目为2.5NA
G.(2021·天津卷)1L1mol/LHCl溶液中,HCl分子的数目为NA
H.(2023·全国甲卷)标准状况下,
 中电子的数目为
中电子的数目为
I.(2022·辽宁卷)pH=12的Na2CO3溶液中OH-数目为0.01NA
J.(2021·福建卷)1.12L C2H4所含极性共价键的数目为0.2NA
K.0.1mol·L-1 HClO4溶液中含有的H+数为0.1NA
L.(2021·广东卷)11.2LNO与11.2LO2混合后的分子数目为NA
M.(2022·浙江6月)11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
您最近一年使用:0次
名校
解题方法
5 . 乙酰苯胺俗称退热冰,是常用的化工原料和重要的化学试剂。某实验小组拟用一定量的乙酸和苯胺制备一定量的乙酰苯胺,具体实验步骤如下:
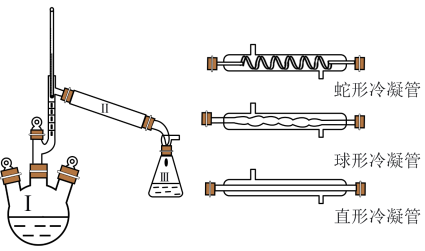
步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
回答下列问题
(1)Ⅱ处空白位置应选择的仪器为___________ (填“蛇形冷凝管”“球形冷凝管”或“直形冷凝管”);反应开始后发现忘加沸石,正确的操作为___________ 。
(2)步骤1中,发生反应的化学方程式是___________ ;温度计控温在105℃的原因是___________ 。
(3)步骤2中,用冷水进行洗涤的原因是___________ 。
(4)步骤3中,趁热抽滤的目的是___________ 。
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为___________ (结果保留2位有效数字)。

步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g/mL) | 溶解性 | |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能溶于水、乙醇、乙醚 |
| 苯胺 | 93 | -6 | 184 | 1.022 | 微溶于水,易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 114 | 304 | 1.12 | 微溶于冷水,能溶于热水 |
(1)Ⅱ处空白位置应选择的仪器为
(2)步骤1中,发生反应的化学方程式是
(3)步骤2中,用冷水进行洗涤的原因是
(4)步骤3中,趁热抽滤的目的是
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为
您最近一年使用:0次
名校
解题方法
6 . 已知 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是
 是阿伏加德罗常数的值。下列说法正确的是
是阿伏加德罗常数的值。下列说法正确的是A.22 g CO2中含有 个碳氧双键 个碳氧双键 |
B.标准状况下,22.4 L HF含有的氟原子数大于 |
C.32 g Cu完全反应一定会失去 个电子 个电子 |
D. 的Na2CO3溶液中,含有的C原子个数为 的Na2CO3溶液中,含有的C原子个数为 |
您最近一年使用:0次
名校
解题方法
7 . 聚合硫酸铁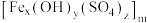 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁,配成 溶液。
溶液。
②准确量取①中溶液 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。
③准确量取①中溶液 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。
该聚合硫酸铁组成中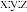 为
为
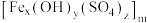 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁,配成
 溶液。
溶液。②准确量取①中溶液
 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。③准确量取①中溶液
 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。该聚合硫酸铁组成中
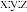 为
为A. | B. | C.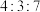 | D. |
您最近一年使用:0次
2023-12-30更新
|
198次组卷
|
3卷引用:选择题11-14
名校
解题方法
8 . 工业上利用碳热还原 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应
ⅰ.
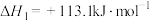
ⅱ.
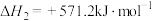
ⅲ.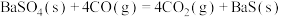
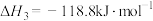

关于碳热还原 的过程,下列说法正确的是
的过程,下列说法正确的是
 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应ⅰ.

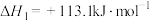
ⅱ.

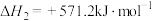
ⅲ.
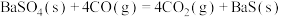
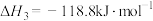

关于碳热还原
 的过程,下列说法正确的是
的过程,下列说法正确的是A.制 的最佳温度应控制在1000℃ 的最佳温度应控制在1000℃ |
| B.400℃之前一定不会发生反应ⅱ |
C.400℃后,反应后组分的变化可能与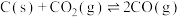 有关 有关 |
D.反应过程中,生成的 和CO的物质的量之和始终等于投入C的物质的量 和CO的物质的量之和始终等于投入C的物质的量 |
您最近一年使用:0次
2023高三·全国·专题练习
9 . 设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是A.室温下, 的 的 溶液中含 溶液中含 的数目为 的数目为 |
B. 铁粉与足量的水蒸气完全反应,转移电子数为 铁粉与足量的水蒸气完全反应,转移电子数为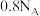 |
C.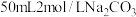 溶液中,阴离子的数目大于 溶液中,阴离子的数目大于 |
D. 由乙烯和环丙烷 由乙烯和环丙烷 组成的混合气体中所含氢原子总数为 组成的混合气体中所含氢原子总数为 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
10 . 氮化硼(BN)是白色难溶于水的粉末状固体,高温下易被氧化。实验室以硼粉(黑色)为原料,用下图装置模拟制备氮化硼。
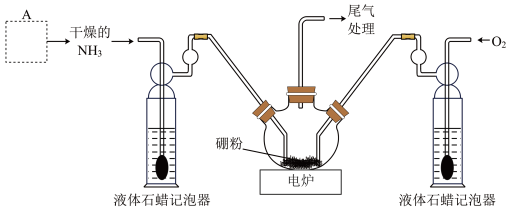
(1)写出制备BN的化学方程式___________ 。
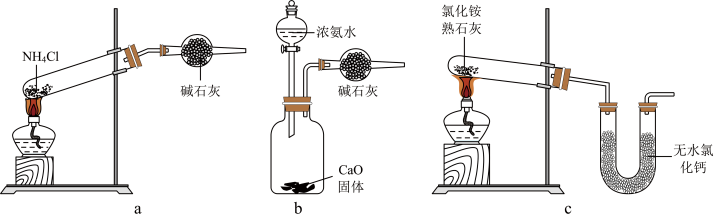
(2)下列装置可填入A框中的是___________ (填标号)。
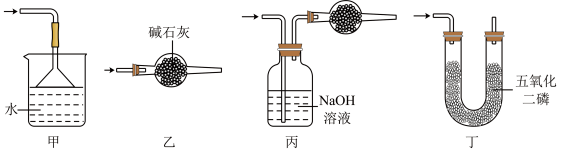
(3)下列装置可用做尾气处理的是___________ (填标号)。
(4)实验所得的氮化硼样品可用“铵盐蒸馏法”测定纯度,具体步骤如下:
①称取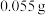 氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
②向铵盐中加入足量 溶液并加热,蒸出的氨全部被
溶液并加热,蒸出的氨全部被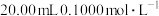 的稀硫酸溶液完全吸收;
的稀硫酸溶液完全吸收;
③向稀硫酸中加入指示剂,用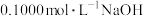 溶液滴定剩余硫酸,消耗
溶液滴定剩余硫酸,消耗 溶液平均体积为
溶液平均体积为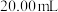 。
。
氮化硼样品的纯度为___________ %(保留1位小数)。

(1)写出制备BN的化学方程式
(2)下列装置可填入A框中的是

(3)下列装置可用做尾气处理的是

(4)实验所得的氮化硼样品可用“铵盐蒸馏法”测定纯度,具体步骤如下:
①称取
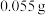 氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;②向铵盐中加入足量
 溶液并加热,蒸出的氨全部被
溶液并加热,蒸出的氨全部被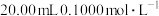 的稀硫酸溶液完全吸收;
的稀硫酸溶液完全吸收;③向稀硫酸中加入指示剂,用
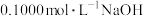 溶液滴定剩余硫酸,消耗
溶液滴定剩余硫酸,消耗 溶液平均体积为
溶液平均体积为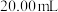 。
。氮化硼样品的纯度为
您最近一年使用:0次



