名校
解题方法
1 . 工业上通常用来吸收燃煤烟气中的SO2的方法有两种:
(1)方法一:在燃煤过程中加入生石灰,称为“钙基固硫法”,反应可看作两步:
①:_______。
②:将①反应的产物进一步与反应生成CaSO4。
写出①反应的化学方程式_______ 。
(2)方法二:用足量的氨水吸收SO2,生成铵盐可作为氮肥加以利用,写出吸收过程的离子方程式_________ 。
(1)方法一:在燃煤过程中加入生石灰,称为“钙基固硫法”,反应可看作两步:
①:_______。
②:将①反应的产物进一步与反应生成CaSO4。
写出①反应的化学方程式
(2)方法二:用足量的氨水吸收SO2,生成铵盐可作为氮肥加以利用,写出吸收过程的离子方程式
您最近半年使用:0次
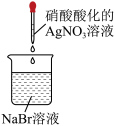
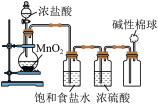
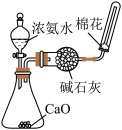
2 . 下列实验设计不能达到相应实验目的的是
A.检验 | B.制备少量纯净的 |
|
|
C.除去 中的少量HCl杂质 中的少量HCl杂质 | D.制备并收集干燥的 |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
回答下列问题:
(1)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为_______ 时, (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是_______ 。
 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。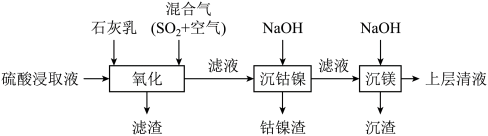
| 物质 |  | 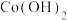 |  |  |
 |  |  |  | 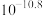 |
(1)“氧化”中保持空气通入速率不变,
 (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为 (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是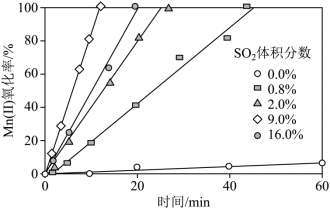
您最近半年使用:0次
4 . CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装置略去)将SO2通入新制氢氧化铜悬浊液中制备CuCl。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有 的操作方法是
的操作方法是_______ 。
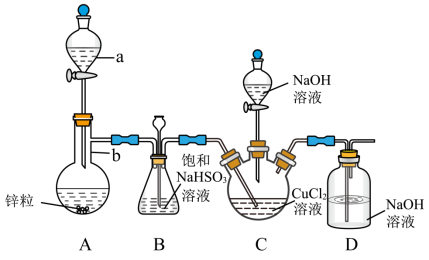
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有
 的操作方法是
的操作方法是
您最近半年使用:0次
5 . 化学和生活、科技、社会发展息息相关,下列说法正确的是
| A.推广使用煤的液化技术,可减少二氧化碳等温室气体的排放,有利于实现碳中和 |
B.华为手机mate 60使用的麒麟 芯片,其主要成分是二氧化硅 芯片,其主要成分是二氧化硅 |
C.造纸业常用 处理纸浆,利用了 处理纸浆,利用了 的漂白性 的漂白性 |
D.科技创新利用 合成脂肪酸,实现无机小分子向有机高分子的转变 合成脂肪酸,实现无机小分子向有机高分子的转变 |
您最近半年使用:0次
6 . 将Cl2分别进行下列实验,现象及结论(或解释)均正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 将过量的干燥氯气通入装有新鲜玫瑰花瓣的集气瓶中,鲜花未变色 | 干燥Cl2没有漂白性 |
| B | 向淀粉-KI溶液中通入Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去 | 还原性:SO2>I->Cl- |
| C | 向FeBr2溶液中通入Cl2,溶液变黄 | 氧化性:Cl2>Br2 |
| D | 将Cl2通入K2S溶液中,生成淡黄色沉淀 | Cl2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 下图是有关二氧化硫性质的实验装置图,下列说法不正确的是
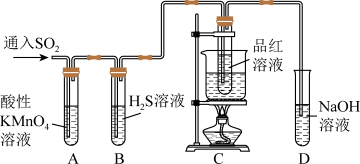
| A.装置A中酸性KMnO4溶液褪色,体现了SO2的漂白性 |
| B.装置B中生成淡黄色沉淀,体现了SO2的氧化性 |
| C.装置C中品红溶液褪色,加热后又恢复原色 |
| D.装置D的作用是吸收多余的SO2,防止污染空气 |
您最近半年使用:0次
名校
解题方法
8 . 下列指定反应的离子方程式书写正确的是
A.将氯气通入水中: |
B. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
C. 通入酸性高锰酸钾溶液:5SO2+2 通入酸性高锰酸钾溶液:5SO2+2 +2H2O = 5 +2H2O = 5 +2Mn2++4H+ +2Mn2++4H+ |
D.向硫酸酸化的 溶液中通入O2: 溶液中通入O2: |
您最近半年使用:0次
9 . 下列对实验设计的评价错误的是
| 选项 | 实验设计 | 实验评价 |
| A. | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。通过测定白色沉淀的质量,可推算二氧化硫的物质的量 | 不合理,酸性高锰酸钾中的稀硫酸会与氯化钡产生沉淀 |
| B. | 实验室用浓硫酸和乙醇制取乙烯时,若要检验所得气体含有CH2=CH2,可将混合气体干燥后,通入溴的四氯化碳溶液中。若溶液褪色,则证明有乙烯 | 合理,混合气体中,只有乙烯可使溴的四氯化碳溶液褪色 |
| C. | 常温下,用pH计分别测定等体积 CH3COONH4溶液和 CH3COONH4溶液和 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 | 合理 |
| D. | 探究浓度对反应速率的影响,向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液。通过观察现象,探究浓度对反应速率的影响 | 不合理,该实验无明显现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 下列装置可以用于相应实验的是
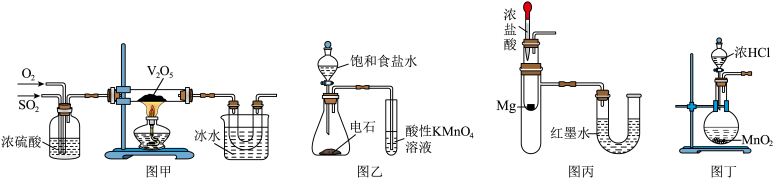
| A.图甲制取并收集SO3 | B.图乙检验乙炔具有还原性 |
| C.图丙中红墨水左高右低 | D.图丁装置制取Cl2 |
您最近半年使用:0次