1 . 下列方程式与所给事实不相符 的是
A.Al溶于NaOH溶液产生无色气体:2Al+2OH-+2H2O=2AlO +3H2↑ +3H2↑ |
| B.用CuSO4溶液除去乙炔中的H2S产生黑色沉淀:Cu2++S2-=CuS↓ |
| C.Fe(OH)2在空气中放置最终变为红褐色:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
D.乙醛与新制的Cu(OH)2在加热条件下产生砖红色沉淀:CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O CH3COONa+Cu2O↓+3H2O |
您最近半年使用:0次
名校
2 . 下列选项所示的物质间转化不能实现的是
A.Na Na2O Na2O Na2O2 Na2O2 NaOH NaOH |
B.H2S SO2 SO2 SO3 SO3 H2SO4 H2SO4 |
C.NH3 NO NO NO2 NO2 HNO3 HNO3 |
D.Si SiO2 SiO2 H2SiO3 H2SiO3 Na2SiO3 Na2SiO3 |
您最近半年使用:0次
名校
解题方法
3 . 下列表述对应的离子方程式书写正确的是
A.FeO溶解于稀硝酸中: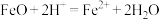 |
B.过量 气体通入氢氧化钠溶液中: 气体通入氢氧化钠溶液中: |
C. 气体通入氯水中: 气体通入氯水中: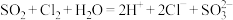 |
D.向氢硫酸( )中通入氯气: )中通入氯气: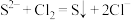 |
您最近半年使用:0次
4 . 根据下列各实验的操作和现象所得出的结论错误的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将 分别通入品红的乙醇溶液和品红的水溶液 分别通入品红的乙醇溶液和品红的水溶液 | 品红的乙醇溶液不褪色,品红的水溶液慢慢褪色 | 使品红褪色的不是 ,而是 ,而是 与水反应后的产物 与水反应后的产物 |
| B | 向 溶液中通入 溶液中通入 | 有淡黄色沉淀产生 | 氧化性: |
| C | 向某待测溶液中滴加 溶液 溶液 | 有白色沉淀产生 | 该溶液中含有 |
| D | 向蔗糖中滴入浓硫酸 | 蔗糖变黑后膨胀,同时有刺激性气味的气体产生 | 浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 回答下列问题:_______ (填化学)。利用图中的物质,写出一个化学方程式以证明还原性:_______ 。
(2)Y是形成酸雨的主要物质之一,含有Y的尾气可以用过量的NaOH溶液吸收,发生反应的化学方程式为________ 。另一类硝酸型酸雨主要由人类活动(汽车尾气)产生的NO造成的,NO2与水反应中氧化产物与还原产物的物质的量之比为_______ 。

(2)Y是形成酸雨的主要物质之一,含有Y的尾气可以用过量的NaOH溶液吸收,发生反应的化学方程式为
您最近半年使用:0次
名校
解题方法
6 . 下列物质中,既能与硫化氢反应又能使溴水褪色的是
①硫化钾溶液;②二氧化硫;③硫酸铜溶液;④硝酸银溶液;⑤小苏打溶液;⑥烧碱溶液
①硫化钾溶液;②二氧化硫;③硫酸铜溶液;④硝酸银溶液;⑤小苏打溶液;⑥烧碱溶液
| A.①②③ | B.①②④⑤⑥ | C.③④⑤⑥ | D.②④⑥ |
您最近半年使用:0次
7 . 能正确表示下列反应的离子方程式为
A.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
C.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3•H2O +OH-=NH3•H2O |
您最近半年使用:0次
名校
8 . 天然气是一种重要的化工原料和燃料,常含有少量H2S。一种在酸性介质中进行天然气脱硫的原理示意图如图所示。下列说法不正确的是
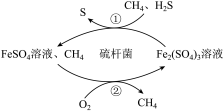

| A.脱硫过程中第①步会使溶液的酸性增强 |
| B.CH4是天然气脱硫过程的催化剂 |
| C.脱硫过程总反应方程式为:2H2S+O2=2S↓+2H2O |
| D.整个脱硫过程中参加反应的n(H2S)∶n(O2)=2∶1 |
您最近半年使用:0次
解题方法
9 . 下列反应的离子方程式正确的是
| A.向CuSO4溶液中通入H2S产生沉淀:Cu2++S2-=CuS↓ |
| B.向H2O2溶液中滴入FeCl3溶液:H2O2+2Fe3+=2Fe2++O2↑+2H+ |
| C.向AgCl沉淀中滴加浓氨水:2NH3·H2O+AgCl=[Ag(NH3)2]++Cl-+2H2O |
| D.向FeI2溶液中通入少量Cl2:Cl2+2Fe2+=2Fe3++2Cl- |
您最近半年使用:0次
名校
10 . 硫脲 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:① ;
;
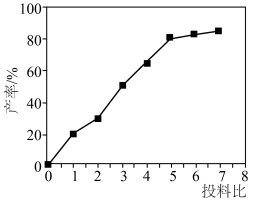
②25℃时硫脲溶解度为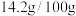 水;
水;
③实验室常用FeS与稀 在常温下制
在常温下制 。
。
(1)盛放石灰乳的仪器的名称是_______ ,B的加热方式宜选择_______ (填标号)。
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现_______ (填实验现象)时表明B中生成了 。
。
(3)实验发现,硫脲产率与投料比 的关系如图所示。
的关系如图所示。
最佳投料比为_______ 。
实验(二):探究硫脲的性质。
资料显示:①150℃时 转化成
转化成 。
。
②酸性 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。
(4)取少量 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加_______ ,可检验是否有 生成。
生成。
(5)取少量 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成_______ (填离子符号)。
(6)甲同学取少量 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。
①乙同学认为甲同学的实验不能证明生成了 ,理由是
,理由是_______ 。
②乙同学设计如图装置验证氧化产物中含有 。
。
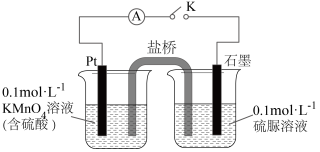
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为_______ ,经检验石墨电极附近还有 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为_______ 。
 是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。
是一种杀菌剂。某小组设计实验制备硫脲并探究其性质。实验(一):制备硫脲。装置如图所示(加热装置已省略)。

已知:①
 ;
;②25℃时硫脲溶解度为
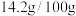 水;
水;③实验室常用FeS与稀
 在常温下制
在常温下制 。
。(1)盛放石灰乳的仪器的名称是
a.直接用酒精灯加热 b.油浴加热(100~250℃) c.热水浴加热
(2)当C装置中出现
 。
。(3)实验发现,硫脲产率与投料比
 的关系如图所示。
的关系如图所示。
最佳投料比为
实验(二):探究硫脲的性质。
资料显示:①150℃时
 转化成
转化成 。
。②酸性
 溶液和硫脲反应,还原产物为
溶液和硫脲反应,还原产物为 ,氧化产物为
,氧化产物为 和
和 。
。(4)取少量
 溶于水,加热至150℃,一段时间后再冷却至室温时,滴加
溶于水,加热至150℃,一段时间后再冷却至室温时,滴加 生成。
生成。(5)取少量
 溶于NaOH溶液,加入
溶于NaOH溶液,加入 溶液,过滤、洗涤,得到黑色固体,由此推知,
溶液,过滤、洗涤,得到黑色固体,由此推知, 在碱性条件下会生成
在碱性条件下会生成(6)甲同学取少量
 溶于水,滴加几滴酸性
溶于水,滴加几滴酸性 溶液,振荡,溶液褪色;再滴加
溶液,振荡,溶液褪色;再滴加 和盐酸溶液,产生白色沉淀。
和盐酸溶液,产生白色沉淀。①乙同学认为甲同学的实验不能证明生成了
 ,理由是
,理由是②乙同学设计如图装置验证氧化产物中含有
 。
。
关闭K,发现电流计指针偏转。一段时间后,左烧杯中酸性高锰酸钾溶液褪色。铂电极上的反应式为
 和
和 生成,总反应的离子方程式为
生成,总反应的离子方程式为
您最近半年使用:0次
2024-04-01更新
|
170次组卷
|
2卷引用:四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学



