名校
1 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行如下实验。
I.实验探究
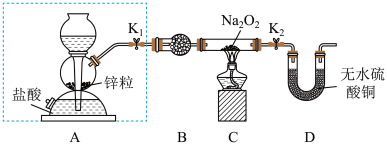
步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:________ 。
(2)B装置中所盛放的试剂是_____ ,其作用是_______ 。
(3)步骤3中的必要操作为打开K1、K2,_______ (请按正确的顺序填入下列步骤的字母)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为__________ 。
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和____ 。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数_____ (填“偏大”“偏小”或“不变”)
I.实验探究

步骤1:按如图所示的装置组装仪器(图中夹持仪器已省略)并检查装置的气密性,然后装入药品。
步骤2:打开K1、K2,在产生的氢气流经装有Na2O2的硬质玻璃管的过程中,未观察到明显现象。
步骤3:进行必要的实验操作,淡黄色的粉末慢慢变成白色固体,无水硫酸铜未变蓝色。
(1)组装好仪器后,要检查装置的气密性。简述检查虚线框内装置气密性的方法:
(2)B装置中所盛放的试剂是
(3)步骤3中的必要操作为打开K1、K2,
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.关闭K1
D.停止加热,充分冷却
(4)由上述实验可推出Na2O2与H2反应的化学方程式为
II.数据处理
(5)实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。
其操作流程如下:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
2017-10-30更新
|
1168次组卷
|
9卷引用:河北省承德市各县第一中学2018届高三上学期期末考试化学试题
河北省承德市各县第一中学2018届高三上学期期末考试化学试题河北省廊坊市2018-2019学年高二下学期期末考试化学试题江西省百所名校2018届高三第一次联合考试化学试题湖南省衡阳市第八中学2017-2018学年高一(理科实验班)上学期第一次月考理综化学试题山西省大同市2020届高三第一次联合考试(县区)化学试题(已下线)第三章 能力提升检测卷(测)——2021年高考化学一轮复习讲练测甘肃省天水市第一中学2021届高三上学期第一学段考试化学试题(已下线)第06讲 钠及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第1讲 钠及其重要化合物
名校
2 . 外观与NaCl相似的亚硝酸钠(NaNO2)可用作建筑钢材缓蚀剂。某学习小组设计如图装置制备亚硝酸钠(夹持装置已省略)。
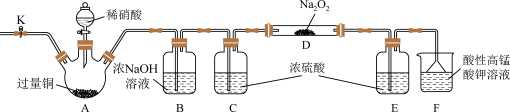
已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3。
回答下列问题:
(1)实验前应检查装置气密性,写出检查装置A气密性的操作步骤和结论:____ 。
(2)装置A中铜与稀硝酸反应的化学方程式为____ 。
(3)反应开始前先打开止水夹K,通入一段时间的氮气的目的是____ 。
(4)若想制备的亚硝酸钠更纯,装置B中浓NaOH溶液的作用是____ 。
(5)若没有装置C,则装置D中剩余固体为____ 。
(6)装置F处理尾气时,酸性高锰酸钾溶液中Mn全部转化为Mn2+,写出该反应的离子方程式:___ 。

已知:2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3。
回答下列问题:
(1)实验前应检查装置气密性,写出检查装置A气密性的操作步骤和结论:
(2)装置A中铜与稀硝酸反应的化学方程式为
(3)反应开始前先打开止水夹K,通入一段时间的氮气的目的是
(4)若想制备的亚硝酸钠更纯,装置B中浓NaOH溶液的作用是
(5)若没有装置C,则装置D中剩余固体为
(6)装置F处理尾气时,酸性高锰酸钾溶液中Mn全部转化为Mn2+,写出该反应的离子方程式:
您最近一年使用:0次
2022-05-01更新
|
178次组卷
|
2卷引用:山西长治上党区第一中学校2021-2022学年高一下学期期末考试化学试题
3 . 已知:① 可与过氧化钠粉末发生化合反应生成
可与过氧化钠粉末发生化合反应生成 ,②
,② 能被酸性
能被酸性 溶液氧化成
溶液氧化成 。某兴趣小组设计了如下图所示的装置制备
。某兴趣小组设计了如下图所示的装置制备 ,下列说法
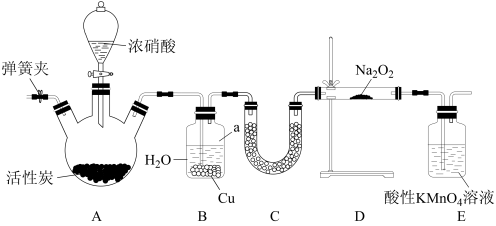
,下列说法不正确 的是
 可与过氧化钠粉末发生化合反应生成
可与过氧化钠粉末发生化合反应生成 ,②
,② 能被酸性
能被酸性 溶液氧化成
溶液氧化成 。某兴趣小组设计了如下图所示的装置制备
。某兴趣小组设计了如下图所示的装置制备 ,下列说法
,下列说法
| A.装置A无需加热,滴入浓硝酸就能发生反应 |
| B.装置B中铜的作用是提高NO的生成率 |
| C.装置C中装的药品可以是氢氧化钠固体 |
D.装置E中的酸性 溶液的主要作用是吸收多余的NO 溶液的主要作用是吸收多余的NO |
您最近一年使用:0次
2022-05-05更新
|
1268次组卷
|
6卷引用:福建省福州金山中学2021-2022学年高一下学期期末考化学试题
福建省福州金山中学2021-2022学年高一下学期期末考化学试题江苏省高邮市重点中学2022届高三第一次诊断测试化学试题(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2022年江苏卷高考真题变式题1-13山东省历城第二中学等学校2023届高三上学期10月月考联合考试化学试题 (已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)
4 . 实验室常用强氧化剂(如: 、
、 、
、 等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用
等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用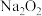 与浓盐酸制备并检验氯气。供选用的实验试剂及装置如图所示(部分导管、蒸馏水略)。
与浓盐酸制备并检验氯气。供选用的实验试剂及装置如图所示(部分导管、蒸馏水略)。
a. b.浓盐酸 c.碱石灰 d.
b.浓盐酸 c.碱石灰 d. 溶液 e.淀粉
溶液 e.淀粉 溶液 f.
溶液 f. g.石蕊溶液 h.饱和
g.石蕊溶液 h.饱和 溶液
溶液
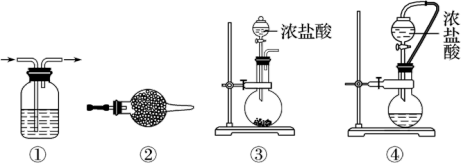
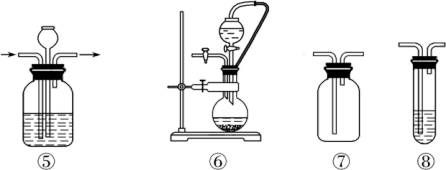
(1)写出用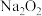 与浓盐酸制备氯气的化学方程式:
与浓盐酸制备氯气的化学方程式:_______ 。
(2)下表中的装置组合最合理的是_______ (填字母,需考虑实验结束撤除装置时残留有害气体的处理)。
(3)某小组成员认为用双氧水代替过氧化钠继续进行探究实验效果要好。请你给出合适的理由:_______ 。
(4)你是否同意将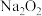 与浓盐酸的反应作为实验室制备氯气的方法之一?
与浓盐酸的反应作为实验室制备氯气的方法之一?_______ (填“是”或“否”);理由是_______ (用化学方程式表示,若填是,该问不必回答)。
 、
、 、
、 等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用
等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用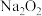 与浓盐酸制备并检验氯气。供选用的实验试剂及装置如图所示(部分导管、蒸馏水略)。
与浓盐酸制备并检验氯气。供选用的实验试剂及装置如图所示(部分导管、蒸馏水略)。a.
 b.浓盐酸 c.碱石灰 d.
b.浓盐酸 c.碱石灰 d. 溶液 e.淀粉
溶液 e.淀粉 溶液 f.
溶液 f. g.石蕊溶液 h.饱和
g.石蕊溶液 h.饱和 溶液
溶液

(1)写出用
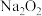 与浓盐酸制备氯气的化学方程式:
与浓盐酸制备氯气的化学方程式:(2)下表中的装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ②/c | ⑦/e | ⑤ |
| B | ③ | ①/d | ⑧/g | ① |
| C | ④ | ①/h | ⑤/e | ② |
| D | ⑥ | ⑤/h | ⑧/e | ① |
(4)你是否同意将
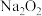 与浓盐酸的反应作为实验室制备氯气的方法之一?
与浓盐酸的反应作为实验室制备氯气的方法之一?
您最近一年使用:0次
名校
5 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是
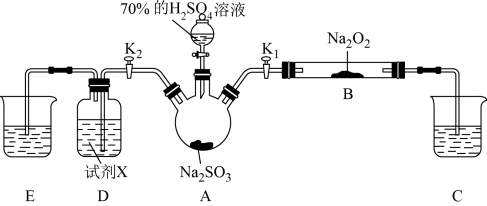

| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5molNa2O2,转移电子数为3NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
2021-11-03更新
|
338次组卷
|
5卷引用:山东省菏泽第一中学2022-2023学年高一上学期期末考试化学试题
6 . 亚硝酸钠是重要的防腐剂,某化学兴趣小组以铜和稀硝酸为起始原料,设计如下装置利用NO与Na2O2反应制备NaNO2。(夹持装置已略)
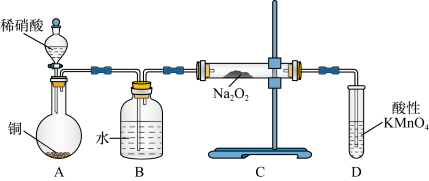
(1)A中反应的化学方程式为_____ 。
(2)B装置的作用是_____ ,装置D的作用是_____ 。
(3)为防止生成其他杂质,B、C装置间还应接入装有_____ (填试剂名称)的_____ (填仪器名称)。
(4)测定C装置中NaNO2的质量分数的过程如下:准确称取装置C中反应后的固体0.600 g于锥形瓶中,先加水溶解,再向其中滴加0.1000 mol·L-1酸性KMnO4溶液,恰好完全反应时,消耗酸性KMnO4溶液24.00 mL。计算装置C中所得固体中NaNO2的质量分数___________ (请写出计算过程)。已知测定过程中发生反应的方程式为MnO4-+NO2-+H+—Mn2++NO3-+H2O(未配平)

(1)A中反应的化学方程式为
(2)B装置的作用是
(3)为防止生成其他杂质,B、C装置间还应接入装有
(4)测定C装置中NaNO2的质量分数的过程如下:准确称取装置C中反应后的固体0.600 g于锥形瓶中,先加水溶解,再向其中滴加0.1000 mol·L-1酸性KMnO4溶液,恰好完全反应时,消耗酸性KMnO4溶液24.00 mL。计算装置C中所得固体中NaNO2的质量分数
您最近一年使用:0次



