1 . 镓是化学史上第一个先从理论预言,后在自然界中被发现验证的化学元素。镓的活动性与锌相似,比铝低。粉煤灰(主要成分为Ga2O3,含CaO、Al2O3等杂质)中提取镓的工艺流程如下图所示。
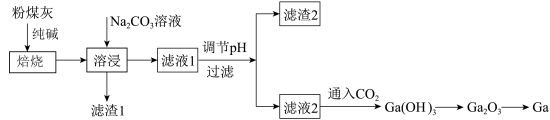
| A.粉煤灰与纯碱在“焙烧”中会产生CO2 |
| B.“溶浸”可使镓、铝化合物溶于溶液,同时将CaO转化为CaCO3而滤出 |
| C.向“滤液1”中加入酸性物质使pH减小,“滤渣2”是Al(OH)3 |
| D.工业上采用电解Ga2O3的方法制备金属Ga |
您最近半年使用:0次
2 . 世界上95%的铝业公司均使用拜耳法(原料为铝土矿,主要成分为 ,含少量
,含少量 、
、 等)生产
等)生产 ,其工艺流程如下:
,其工艺流程如下:
下列说法错误的是
 ,含少量
,含少量 、
、 等)生产
等)生产 ,其工艺流程如下:
,其工艺流程如下: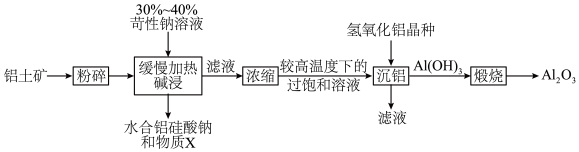
下列说法错误的是
A.物质X为 |
B.可用过量 代替氢氧化铝晶种 代替氢氧化铝晶种 |
C.“缓慢加热”可促使 转化为水合铝硅酸钠 转化为水合铝硅酸钠 |
| D.该流程中可循环利用的物质主要有氢氧化铝晶种 |
您最近半年使用:0次
3 . 以黄铁矿为原料制硫酸会产生大量的矿渣(主要成分为Fe2O3,还有Al2O3、CuO),合理利用矿渣可以减少环境污染,变废为宝。利用该矿渣生产碱式硫酸铁的流程如图所示:

| A.“碱浸”的目的是除去矿渣中的Al2O3 |
| B.“酸浸”后所得溶液中的金属阳离子主要是Fe3+、Cu2+ |
C.“去铜”过程中发生的反应之一为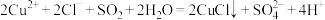 |
| D.“调pH”时,pH越高,越有利于提高碱式硫酸铁的产率 |
您最近半年使用:0次
名校
4 . 金属Co、Ni的性质相似,在电子工业以及金属材料中应用十分广泛。实验室中采用含钴、镍、铝的废渣(主要成分为Co2O3、Ni,含少量杂质Al2O3)提取钴、镍的具体流程如下:
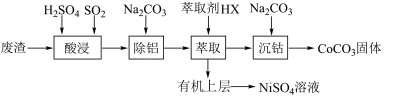
| A.酸浸时SO2的作用是加强反应液的酸性 |
| B.酸浸时Ni发生反应的离子方程式为2Ni+6H+=3H2↑+2Ni3+ |
| C.除铝过程中有白色沉淀碳酸铝产生 |
| D.Ni2+比Co2+更容易与萃取剂HX结合 |
您最近半年使用:0次
名校
解题方法
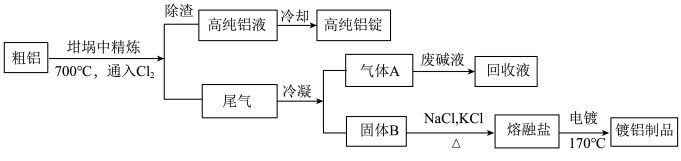
5 . 由熔盐电解法获得的粗铝含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。有关工艺流程如下: 在181℃升华】
在181℃升华】
请回答下列问题:
(1)精炼前,需清除坩埚表面的氧化铁和石英砂( ),防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为
),防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为 和
和______________________________ 。
(2)将 连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除
连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除 外还含有
外还含有__________ ,__________ (填化学式);固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在__________ (填化学式)。
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为: 和
和______________________________ 。
 在181℃升华】
在181℃升华】请回答下列问题:
(1)精炼前,需清除坩埚表面的氧化铁和石英砂(
 ),防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为
),防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为 和
和(2)将
 连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除
连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除 外还含有
外还含有(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为:
 和
和
您最近半年使用:0次
名校
6 . 下表是元素周期表前20号元素的有关信息:
已知:Li的半径为0.152nm,Be的半径为0.111nm。回答下列问题:
(1)元素c在周期表中的位置为________ ,用电子式表示a2e的形成过程:________ 。
(2)f、h、b简单离子半径由大到小的顺序为________ (用离子符号表示)。
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是________ ,发生反应的离子方程式为________ 。
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:________ 。
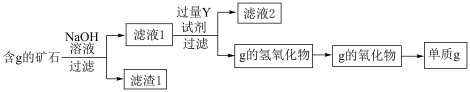
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:________ (填写化学式),滤液1中通入过量Y试剂反应的离子方程式为:________ 。
| 元素 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 | +1 | +4 | +1 | +6 | +1 | +3 | +7 | |
| 最低负化合价 | -2 | -4 | -2 | -1 |
(1)元素c在周期表中的位置为
(2)f、h、b简单离子半径由大到小的顺序为
(3)BaCl2溶液中先通入eb2,再加入h的单质,可观察到的现象是
(4)化合物A、B均由a、b、e、f四种元素组成,则A和B相互反应的离子方程式:
(5)工业上用含g元素的矿石(主要成分为g的氧化物,还含有杂质FeO、Fe2O3)提纯g的氧化物并冶炼单质g,流程如下,滤渣1的成分为:

您最近半年使用:0次
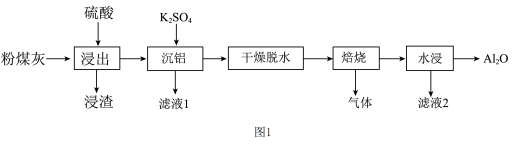
7 . 粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰(主要含SiO2、Al2O3和CaO等)为原料提铝的工艺流程如下图1。其中“沉铝”时,体系中三种物质的溶解度曲线如下图2所示。

下列说法错误的是


下列说法错误的是
| A.“浸出”时不涉及氧化还原反应 | B.“浸渣”的主要成分是SiO2 |
C.“沉铝”的滤渣为 | D.“滤液2”可返回“沉铝”循环使用 |
您最近半年使用:0次
解题方法
8 . 下表是各物质及其所含的少量杂质,以及除去这些杂质所选用的试剂或操作方法,其中错误的是
| 选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
| A | FeCl2 溶液 | FeCl3 | 加入过量铁粉,再过滤 |
| B | NaHCO3 溶液 | Na2CO3 | 通入过量的 CO2气体 |
| C | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,再过滤 |
| D | MgO 固体 | Al2O3 | 加入过量的NaOH溶液,再过滤 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
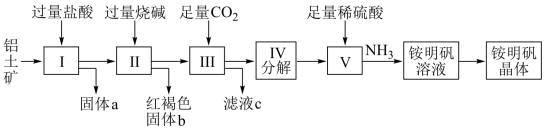
9 . 铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2•12H2O]的工艺流程如图所示:
请回答下列问题:
(1)固体a的化学式为___________ 。
(2)加快I的反应速率的措施有___________ (任写两点即可)。
(3)写出Ⅱ中加过量的烧碱涉及的反应离子方程式:___________ ,___________ 。
(4)由I中得到固体a的实验操作为___________ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)___________ 、___________ 、过滤、洗涤。
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子刚好完全沉淀的化学反应方程式为___________ 。

请回答下列问题:
(1)固体a的化学式为
(2)加快I的反应速率的措施有
(3)写出Ⅱ中加过量的烧碱涉及的反应离子方程式:
(4)由I中得到固体a的实验操作为
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子刚好完全沉淀的化学反应方程式为
您最近半年使用:0次
23-24高一下·全国·课后作业
名校
解题方法
10 . 工业上以铝土矿(主要成分是氧化铝,含氧化铁杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是
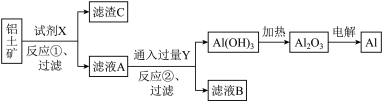

| A.反应①中试剂X是氢氧化钠溶液 |
B.试剂Y是 ,它与 ,它与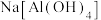 反应生成氢氧化铝 反应生成氢氧化铝 |
| C.图中所示转化反应中包含2个氧化还原反应 |
| D.将X与Y试剂进行对换,最终可以达到相同结果 |
您最近半年使用:0次



