1 . 下列物质可通过化合反应制得的是
A. | B. | C.CuS | D. |
您最近半年使用:0次
2 . “类比”是化学学习中一种常用的方法,下列“类比”结果正确的是
| A.酸性氧化物CO2与Na2O2反应生成Na2CO3,则SO2与Na2O2反应生成Na2SO3 |
| B.Cl2与水反应生成HCl和HClO,推测F2与水反应生成HF和HFO |
| C.CO2可以与Ca(ClO)2反应生成CaCO3和HClO,类比出SO2与Ca(ClO)2反应生成CaSO3和HClO |
| D.MgCl2溶液中加入过量氨水生成Mg(OH)2,则AlCl3溶液中加入过量氨水生成Al(OH)3 |
您最近半年使用:0次
名校
解题方法
3 . 下列离子方程式书写正确的是
A.硫酸铝溶液与过量氨水反应: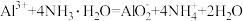 |
B.向过量的 溶液中滴加少量“84”消毒液: 溶液中滴加少量“84”消毒液: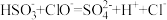 |
C.向次氯酸钠溶液中通入少量二氧化碳: |
D.向碘化亚铁溶液中通入过量氯气: |
您最近半年使用:0次
名校
4 . 下列离子方程式书写正确的是
A.向NaClO溶液中通入足量SO2气体:ClO-+SO2+H2O=Cl-+ +2H+ +2H+ |
B.NO2气体通入足量NaOH溶液中:NO2+2OH-= +H2O +H2O |
C.向氯化铝溶液中滴加过量氨水:4NH3•H2O+Al3+= +4 +4 +2H2O +2H2O |
| D.向Fe(OH)3加入氢碘酸溶液:Fe(OH)3+3H+=Fe3++3H2O |
您最近半年使用:0次
名校
解题方法
5 . 下列指定反应的离子方程式正确的是
A.向NaAlO2溶液中通入足量CO2:2 +3H2O+CO2= +3H2O+CO2= +2Al(OH)3↓ +2Al(OH)3↓ |
| B.向CuCl2溶液中加入铁粉:2Fe+3Cu2+=2Fe3++3Cu |
C.NO2气体溶于水:NO2+H2O=2H++ |
D.向AlCl3溶液中加入过量氨水: |
您最近半年使用:0次
名校
解题方法
6 . 下列离子方程式书写错误的是
| A.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
B.向AlCl3溶液中通入足量NH3:Al3+ + 4NH3 + 2H2O=AlO + 4NH + 4NH |
| C.氢氧化铜浊液中滴加氨水得到深蓝色溶液:Cu(OH)2 + 4NH3 = [Cu(NH3)4]2+ + 2OH- |
D.将铜丝插入足量浓硝酸中:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
您最近半年使用:0次
名校
解题方法
7 . 随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。下图是废旧钴酸锂电池材料(主要成分为 ,含少量铁、铝、铜等元素的化合物)回收工艺流程:
,含少量铁、铝、铜等元素的化合物)回收工艺流程:________ 。
(2)滤液1中加入 的主要目的是
的主要目的是________ 。
(3)加入 氧化
氧化 的离子方程式为
的离子方程式为________ 。
(4)滤液1经过一系列反应后,加入氨水生成氢氧化铝的离子方程式为________ 。
(5)“沉钴”过程中, 的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示: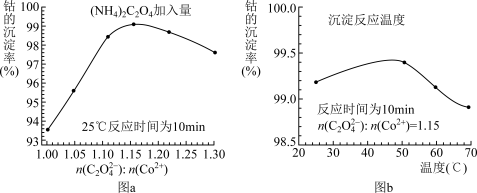
根据图分析:沉钴时应控制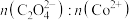 为
为________ ,温度控制在________ ℃左右。
(6)已知100kg废旧的锂电池中钴酸锂( )的含量为9.8%,若按照上述生产流程,可以生成
)的含量为9.8%,若按照上述生产流程,可以生成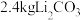 ,则其产率为
,则其产率为________ (保留一位小数)。
 ,含少量铁、铝、铜等元素的化合物)回收工艺流程:
,含少量铁、铝、铜等元素的化合物)回收工艺流程: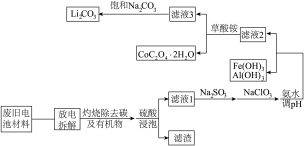
(2)滤液1中加入
 的主要目的是
的主要目的是(3)加入
 氧化
氧化 的离子方程式为
的离子方程式为(4)滤液1经过一系列反应后,加入氨水生成氢氧化铝的离子方程式为
(5)“沉钴”过程中,
 的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:
根据图分析:沉钴时应控制
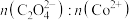 为
为(6)已知100kg废旧的锂电池中钴酸锂(
 )的含量为9.8%,若按照上述生产流程,可以生成
)的含量为9.8%,若按照上述生产流程,可以生成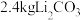 ,则其产率为
,则其产率为
您最近半年使用:0次
名校
8 . 解释下列事实的化学方程式或离子方程式正确的是
A.反萃取法中碘单质和氢氧化钠浓溶液反应: |
B.用焦炭还原二氧化硅制备粗硅: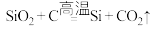 |
C.将氧化铁溶于氢碘酸的离子反应: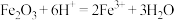 |
D.铝盐与过量氨水的离子反应: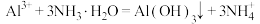 |
您最近半年使用:0次
9 . 取一定体积的下列两种试剂(浓度均为 )进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
)进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
 )进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
)进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是A. 溶液、稀盐酸 溶液、稀盐酸 | B. 溶液、氨水 溶液、氨水 |
C. 溶液、溴水 溶液、溴水 | D. 溶液、酸性 溶液、酸性 溶液 溶液 |
您最近半年使用:0次
解题方法
10 . 下列物质性质实验对应的离子方程式书写正确的是
A. 溶于水: 溶于水: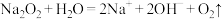 |
B.食醋去除水垢中的 : :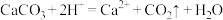 |
C.同浓度同体积 溶液与 溶液与 溶液混合: 溶液混合: |
D.硫酸铝溶液中滴入足量氨水: |
您最近半年使用:0次



