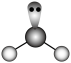
1 . 下列“事实”的“图示表达”不正确 的是
| 事实 | 图示表达 | |
| A. | SO2是极性分子 |
|
| B. | 气态氟化氢中存在(HF)2 |
|
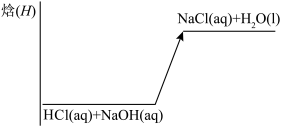
| C. | HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) < < |
|
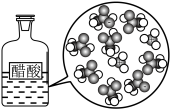
| D. | CH3COOH CH3COO-+H+ CH3COO-+H+ |
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列说法或表示正确的是
A.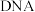 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 |
B. 要在光照和点燃条件下才反应,所以 要在光照和点燃条件下才反应,所以 , , |
C.已知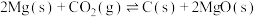 ,达平衡后,缩小容器体积, ,达平衡后,缩小容器体积, 浓度增大 浓度增大 |
D.将 的醋酸稀释为 的醋酸稀释为 的过程中, 的过程中, 减小 减小 |
您最近半年使用:0次
解题方法
3 . 25℃时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示。

| A.在该反应条件下,产物1比产物2稳定 |
| B.固体酸分子筛可通过氢键吸附乙醇 |
| C.固体酸分子筛能减小图示反应的焓变 |
D.生成产物1的决速步骤的活化能为36.7 |
您最近半年使用:0次
7日内更新
|
200次组卷
|
2卷引用:河南省新乡市2024届高三第二次模拟考试理综-化学试题
4 .  是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用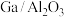 作为催化剂实现了
作为催化剂实现了 100%催化水解,其历程如下图所示。
100%催化水解,其历程如下图所示。
 是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用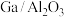 作为催化剂实现了
作为催化剂实现了 100%催化水解,其历程如下图所示。
100%催化水解,其历程如下图所示。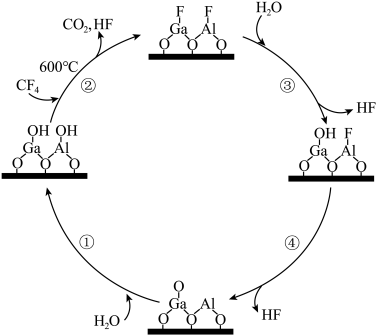
A.总反应为 |
B.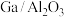 不能改变总反应的 不能改变总反应的 |
| C.反应过程中,Ga-F、C-F键既有断裂又有形成 |
| D.反应过程中涉及的小分子包含两种非极性分子 |
您最近半年使用:0次
2024-04-12更新
|
218次组卷
|
2卷引用:河南省周口市2024届高三二模理综-化学试题
名校
5 . 明朝著名科学家宋应星所著《天工开物》中记载:“凡火药以硝石,硫黄为主,草木灰为辅。”黑火药爆炸时发生的反应为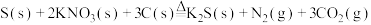
 ,设
,设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
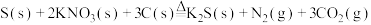
 ,设
,设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是| A.将硝石和硫黄捣碎后与草木灰混合的目的是增大反应物接触面积,加快反应速率 |
B.若上述反应在纯氧中发生,生成物中会有大量的 |
C.反应中每生成 ,放出 ,放出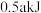 能量 能量 |
D.可以用焰色反应鉴别硝石( )和芒硝( )和芒硝( ) ) |
您最近半年使用:0次
解题方法
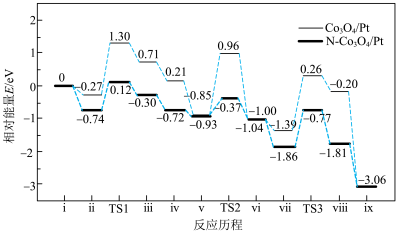
6 . 我国科学家利用两种不同的纳米催化剂(Co3O4/Pt、N- Co3O4/Pt)在室温水汽条件下实现高效CO催化氧化(C16O+ 16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
 16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
16O2=C16O2),其反应历程中相对能量的变化如下图所示(TS1、TS2、TS3分别代表过渡态1、过渡态2、过渡态3)。下列说法错误的是
| A.效果较好的催化剂是N-Co3O4/Pt |
| B.若利用H218O进行同位素标记实验,检测到以上反应中有C16O18O和C18O2生成,说明O-H键断裂 |
C.反应:C16O(g)+ 16O2(g)=C16O2 (g)的∆H<0 16O2(g)=C16O2 (g)的∆H<0 |
| D.若ⅱ表示H2O被吸附在催化剂表面,则Co3O4/Pt更容易吸附H2O |
您最近半年使用:0次
解题方法
7 . 下列说法正确的是
| A.常温下,2.0×10-4mol/L的盐酸稀释104倍,c(H+)=2.0×10-8 mol/L |
B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的 H不同 H不同 |
| C.常温下,pH=3的醋酸溶液中加入少量醋酸钠固体,溶液pH不变 |
| D.将KCl溶液从常温加热至60℃,溶液的pH变小但仍保持中性 |
您最近半年使用:0次
8 . 甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
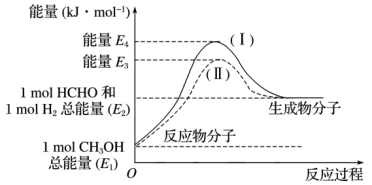
(1)甲醇催化脱氢转化为甲醛的反应是___________ (填“吸热”或“放热”)反应。
(2)过程Ⅰ与过程Ⅱ的反应热是否相同?___________ ,原因是___________ 。
(3)该反应的焓变ΔH=___________ kJ·mol-1。

(1)甲醇催化脱氢转化为甲醛的反应是
(2)过程Ⅰ与过程Ⅱ的反应热是否相同?
(3)该反应的焓变ΔH=
您最近半年使用:0次
解题方法
9 . Ⅰ.现有部分元素的性质与原子(或分子)结构如表所示:
回答下列问题:
(1)T是_______ (填元素符号)。元素X在周期表的位置_______ 。
(2)Y与Z相比,金属性较强的是_____ (填元素符号),下列表述中能证明这一事实的是_______ (填标号)。
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.Y单质与水反应比Z单质与水反应剧烈得多
(3)Z的最高价氧化物属于_______ 氧化物(“酸性”、“碱性”或“两性”),写出Y、Z最高价氧化物对应水化物反应的离子方程式____ 。
Ⅱ.2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
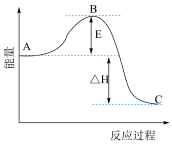
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(4)图中A、C分别表示_______ 、_______ 。
(5)图中△H=_______ kJ·mol-1。
(6)已知单质硫的燃烧热为296KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H_______ 。
元素 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,是空气的主要成分,分子比较稳定 |
| Y | M层比K层少一个电子 |
| Z | 有三个电子层,M层上有3个电子 |
(1)T是
(2)Y与Z相比,金属性较强的是
A.Y单质的熔点比Z单质的低
B.Y的化合价比Z的低
C.Y单质与水反应比Z单质与水反应剧烈得多
(3)Z的最高价氧化物属于
Ⅱ.2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(4)图中A、C分别表示
(5)图中△H=
(6)已知单质硫的燃烧热为296KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H
您最近半年使用:0次
10 . 已知化学反应A2(g)+B2(g)=2AB(g) ΔH=+100kJ·mol-1的能量变化如图所示,判断下列叙述中错误的是

| A.加入催化剂,该反应的反应热ΔH将不变 | B.每形成2molA—B键,将放出bkJ能量 |
| C.每生成2分子AB吸收(a-b)kJ热量 | D.该反应正反应的活化能大于100kJ·mol-1 |
您最近半年使用:0次