1 . 相同温度和压强下,关于反应的 ,下列判断正确的是
,下列判断正确的是
 ,下列判断正确的是
,下列判断正确的是
A. | B. |
C.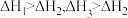 | D.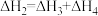 |
您最近一年使用:0次
2021-06-15更新
|
7336次组卷
|
18卷引用:2021年6月新高考浙江化学高考真题
2021年6月新高考浙江化学高考真题(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)2021年6月浙江高考化学试题变式题21-25(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点05 化学反应中的能量变化-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第15讲 化学反应的热效应 (练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点18 化学反应与能量-备战2023年高考化学考试易错题(已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第34讲 反应热的计算(已下线)专题08 化学反应中的能量变化(已下线)专题08 化学反应中的能量变化(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)第2讲 盖斯定律 反应热的计算(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第01讲 化学反应的热效应(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)第01讲 化学反应的热效应(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2 . 汽车尾气是否为导致空气质量问题的主要原因,由此引发的“汽车限行”争议,是当前备受关注的社会性科学议题。
(1)反应
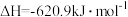 可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(
可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如图所示( 表示过渡态、
表示过渡态、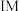 表示中间产物)。
表示中间产物)。
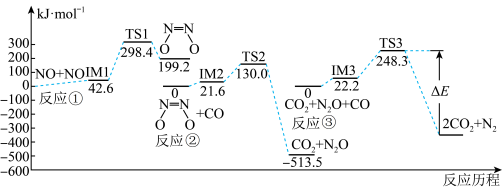
三个基元反应中,属于放热反应的是___________ (填标号);图中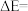
___________  。
。
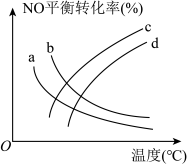
(2)探究温度、压强(2 、5
、5 )对反应
)对反应 的影响,如图所示,表示2
的影响,如图所示,表示2 的是
的是___________ (填标号)。
(3)用 可以消除
可以消除 污染:
污染: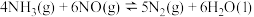

①某条件下该反应速率 ,
,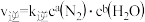 ,该反应的平衡常数
,该反应的平衡常数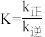 ,则
,则
___________ ,
___________ 。
②一定温度下,在体积为1L的恒容密闭容器中加入4
 和6
和6
 发生上述反应,测得
发生上述反应,测得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
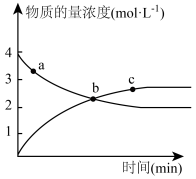
a点的正反应速率___________ c点的逆反应速率(填“大于”、“小于”或“等于”);测得平衡时体系压强为 ),则该反应温度下
),则该反应温度下
___________ 。(用含 的式子表示,只列式不用化简)。若在相同时间内测得
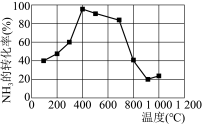
的式子表示,只列式不用化简)。若在相同时间内测得 的转化率随温度的变化曲线如下图,400℃~900℃之间
的转化率随温度的变化曲线如下图,400℃~900℃之间 的转化率下降由缓到急的原因是
的转化率下降由缓到急的原因是___________ 。
(1)反应

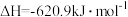 可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(
可有效降低汽车尾气污染物的排放。一定条件下该反应经历三个基元反应阶段,反应历程如图所示( 表示过渡态、
表示过渡态、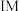 表示中间产物)。
表示中间产物)。
三个基元反应中,属于放热反应的是
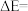
 。
。(2)探究温度、压强(2
 、5
、5 )对反应
)对反应 的影响,如图所示,表示2
的影响,如图所示,表示2 的是
的是
(3)用
 可以消除
可以消除 污染:
污染: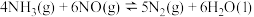

①某条件下该反应速率
 ,
,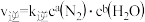 ,该反应的平衡常数
,该反应的平衡常数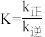 ,则
,则

②一定温度下,在体积为1L的恒容密闭容器中加入4

 和6
和6
 发生上述反应,测得
发生上述反应,测得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
a点的正反应速率
 ),则该反应温度下
),则该反应温度下
 的式子表示,只列式不用化简)。若在相同时间内测得
的式子表示,只列式不用化简)。若在相同时间内测得 的转化率随温度的变化曲线如下图,400℃~900℃之间
的转化率随温度的变化曲线如下图,400℃~900℃之间 的转化率下降由缓到急的原因是
的转化率下降由缓到急的原因是
您最近一年使用:0次
2021-05-11更新
|
777次组卷
|
4卷引用:山东省青岛市2021届高三二模化学试题
山东省青岛市2021届高三二模化学试题(已下线)专题15 化学反应原理综合-备战2022年高考化学真题及地市好题专项集训【山东专用】湖北武汉市2022届高三5月第一次模拟考试化学试题山东省青岛市即墨区第一中学2022-2023学年高三上学期10月月考化学试题
名校
解题方法
3 . 已知反应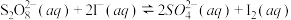 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:
①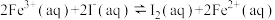
②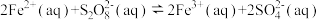
下列说法错误的是
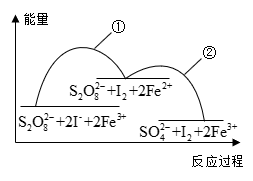
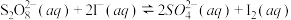 ,若往该溶液中加入含
,若往该溶液中加入含 的某溶液,反应机理:
的某溶液,反应机理:①
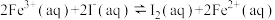
②
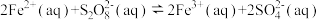
下列说法错误的是

A. 是该反应的催化剂,加入 是该反应的催化剂,加入 后降低了该反应的活化能 后降低了该反应的活化能 |
| B.往该溶液中滴加淀粉溶液,溶液变蓝,适当升温,蓝色加深 |
C.步骤①中 和 和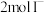 的总能量低于 的总能量低于 和 和 的总能量 的总能量 |
D.增大 浓度或 浓度或 浓度,反应①、反应②的反应速率均加快 浓度,反应①、反应②的反应速率均加快 |
您最近一年使用:0次
2020-12-18更新
|
1501次组卷
|
8卷引用:押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)
(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)北京市第五十五中学2022-2023学年高三上学期期中考试化学试题山东省菏泽市2020-2021学年高二上学期期中考试化学试题(A)山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题(已下线)2.4 化学反应的调控-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)河南省南阳市第一中学校2022-2023学年高二上学期开学考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179
20-21高三上·江西南昌·期中
解题方法
4 . (1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应化学方程式为:C2H5OH(g)+IB(g)=ETBE(g)△H。反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=___ kJ/mol。反应历程的最优途径是____ (填C1、C2或C3)。
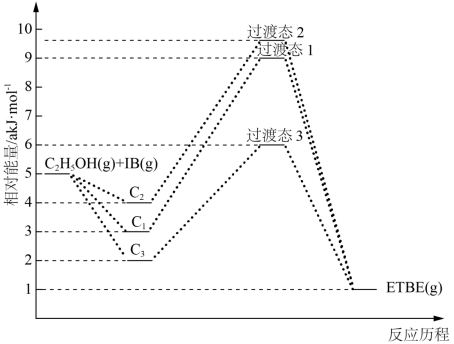
C1表示先吸附乙醇,C2表示先吸附异丁烯,C3表示乙醇和异丁烯同时吸附
(2)用NH3可消除NO污染,反应原理为:4NH3+6NO 5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。

①曲线a对应的n(NH3):n(NO)=___ 。
②曲线c中NO的起始浓度为4×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为____ 。
③由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降,可能的原因是____ (至少写两条)。
(3)已知NO2存在如下平衡:2NO2(g) N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。
N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。

一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=____ ;在上图标出点中,指出能表示反应达到平衡状态的点是___ ,理由是___ 。
(4)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g) 2SO3(g)。
2SO3(g)。
已知:标准平衡常数Kθ= ,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=____ (用含ω的最简式表示)。

C1表示先吸附乙醇,C2表示先吸附异丁烯,C3表示乙醇和异丁烯同时吸附
(2)用NH3可消除NO污染,反应原理为:4NH3+6NO
 5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
5N2+6H2O,以n(NH3):n(NO)分别为4:1、3:1、1:3投料,得到NO脱除率随温度变化的曲线如图所示。
①曲线a对应的n(NH3):n(NO)=
②曲线c中NO的起始浓度为4×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为
③由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降,可能的原因是
(3)已知NO2存在如下平衡:2NO2(g)
 N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。
N2O4(g)△H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1•p2(NO2),v(N2O4)=k2•p(N2O4),相应的速率与其分压关系如图所示。
一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(4)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g)
 2SO3(g)。
2SO3(g)。已知:标准平衡常数Kθ=
 ,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=
您最近一年使用:0次
5 . 我国科研人员研究了在Cu - ZnO – ZrO2催化剂上CO2加氢制CH3OH的机理,其反应历程如图所示:
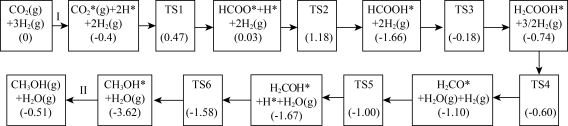
其中,TS表示过渡态、吸附在催化剂表面上的物种用*标注,括号里的数字表示微粒的相对总能量[单位:eV(1 eV= 1.60×10-19)],下列说法正确的是

其中,TS表示过渡态、吸附在催化剂表面上的物种用*标注,括号里的数字表示微粒的相对总能量[单位:eV(1 eV= 1.60×10-19)],下列说法正确的是
| A.该反应的反应热ΔH= -8.16×10-23kJ/mol |
| B.过程I有H-H键断裂,过程II表示与催化剂脱离 |
| C.等物质的量的CO2和CH3OH中共用电子对数目之比为8:5 |
D.催化剂表面发生的反应中决速步骤为HCOOH*+ H2(g)一-H2COOH* H2(g)一-H2COOH* |
您最近一年使用:0次
解题方法
6 . 目前Haber-Bosch法是工业合成氨的主要方式,其生产条件需要高温高压。为了有效降低能耗,过渡金属催化还原氮气合成氨被认为是具有巨大前景的替代方法。催化过程一般有吸附—解离—反应—脱附等过程,图示为N2和H2在固体催化剂表面合成氨反应路径的势能面图(部分数据略),其中“*”表示被催化剂吸附。
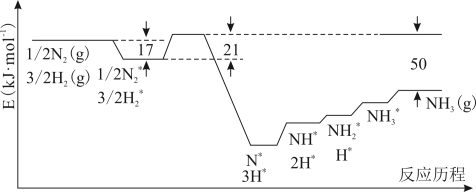
(1)氨气的脱附是____ 过程(填“吸热”或“放热”),合成氨的热化学方程式为_____
(2)合成氨的捷姆金和佩热夫速率方程式为 w= k1 p(N2) -k2
-k2 ,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2⇌2NH3的平衡常数Kp=
,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2⇌2NH3的平衡常数Kp=_________ (用k1,k2表示)(注:Kp用各物质平衡分压来表示)。
(3)若将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。

①温度T1___ T2 (填“>”、“<”或“=”下同),T1温度下恰好平衡时,曲线B上的点为b(m, n ),则m___ 12,n__ 2。
②T2 温度下,反应从开始到恰好平衡时平均速率v(N2) =_____ 。
③T2温度下,合成氨反应N2+3H2⇌2NH3的平衡常数的数值是____ ;若某时刻,容器内气体的压强为起始时的80%,则此时v(正)____ v(逆)(填“>”、“<”或“=”)。
(4)工业上通过降低反应后混合气体的温度而使氨气分离出来。这种分离物质的方法, 其原理类似于下列方法中的___ (填序号)。
A.过滤 B.蒸馏 C.渗析 D.萃取

(1)氨气的脱附是
(2)合成氨的捷姆金和佩热夫速率方程式为 w= k1 p(N2)
 -k2
-k2 ,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2⇌2NH3的平衡常数Kp=
,w为反应的瞬时总速率,为正反应和逆反应速率之差,k1、k2是正、逆反应速率常数。合成氨反应N2+3H2⇌2NH3的平衡常数Kp=(3)若将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。

①温度T1
②T2 温度下,反应从开始到恰好平衡时平均速率v(N2) =
③T2温度下,合成氨反应N2+3H2⇌2NH3的平衡常数的数值是
(4)工业上通过降低反应后混合气体的温度而使氨气分离出来。这种分离物质的方法, 其原理类似于下列方法中的
A.过滤 B.蒸馏 C.渗析 D.萃取
您最近一年使用:0次
7 . 水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用·标注。下列说法正确的是( )
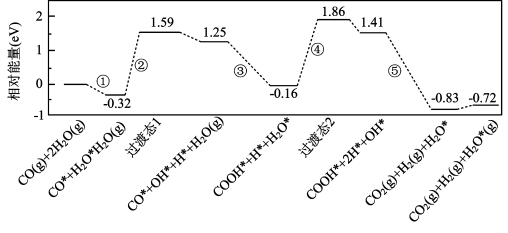

| A.水煤气变换反应的△H>0 |
| B.步骤③的化学方程式为:CO·+OH·+H2O(g)=COOH·+H2O· |
| C.步骤⑤只有非极性键H—H键形成 |
| D.该历程中最大能垒(活化能)E正=2.02eV |
您最近一年使用:0次
2020-05-09更新
|
605次组卷
|
2卷引用:山东省德州市2020届高三第一次模拟考试化学试题
8 . 下列反应类型正确的是
A.卤素互化物 拟卤素 拟卤素 与水反应 与水反应 非氧化还原反应 非氧化还原反应 |
B.白烟实验检验氨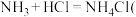 白烟 白烟 离子反应 离子反应 |
C.乙醇的催化氧化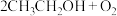 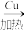  吸热反应 吸热反应 |
D.卤代乙醇法制环氧乙烷第一步反应 取代反应 取代反应 |
您最近一年使用:0次
9 . I.NO是一种常见化合物,对其进行研究具有重要的价值和意义。
(1)2NO(g)+O2(g)=2NO2(g) △H=akJ/mol的反应历程与能量变化关系如图所示。
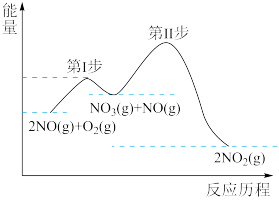
①a___ 0(填>或<)
②已知:第Ⅱ步反应为:NO3(g)+NO(g)=2NO2(g) △H=bkJ/mol
第I步反应的热化学方程式为___ 。
(2)汽车尾气中常含有NO。NH3在加热和催化剂存在的条件下能消除NO的污染。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=—905kJ/mol
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=—1268kJ/mol
NH3与NO反应的热化学方程式为___ 。
(3)工业上NO的重要来源是NH3,NH3也可作为燃料设计成碱性燃料电池,在碱性条件下,燃料电池产物主要为N2。燃料电池负极的电极反应式为___ 。氨气作为燃料的电池和含碳化合物作为燃料的电池相比,主要的优点是___ 。
II.含乙酸钠和对氯酚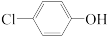 的废水可通过如下装置处理,其原理如图所示:
的废水可通过如下装置处理,其原理如图所示:
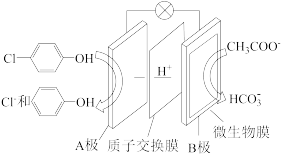
(1)写出HCO3-的电子式___ 。乙酸钠中含有的化学键类型有___ 。
(2)电池的正极是___ ,溶液中H+的移动方向是___ (填A→B或B→A)
(3)B极发生的电极反应方程式为___ 。
(1)2NO(g)+O2(g)=2NO2(g) △H=akJ/mol的反应历程与能量变化关系如图所示。

①a
②已知:第Ⅱ步反应为:NO3(g)+NO(g)=2NO2(g) △H=bkJ/mol
第I步反应的热化学方程式为
(2)汽车尾气中常含有NO。NH3在加热和催化剂存在的条件下能消除NO的污染。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=—905kJ/mol
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=—1268kJ/mol
NH3与NO反应的热化学方程式为
(3)工业上NO的重要来源是NH3,NH3也可作为燃料设计成碱性燃料电池,在碱性条件下,燃料电池产物主要为N2。燃料电池负极的电极反应式为
II.含乙酸钠和对氯酚
 的废水可通过如下装置处理,其原理如图所示:
的废水可通过如下装置处理,其原理如图所示:
(1)写出HCO3-的电子式
(2)电池的正极是
(3)B极发生的电极反应方程式为
您最近一年使用:0次
2019-12-31更新
|
292次组卷
|
2卷引用:华南师范大学附中2020届高三上学期第三次月考理综化学试题
18-19高三·浙江·阶段练习
名校
10 . 下列说法正确的是
| A.如不小心被同样温度的液态水和水蒸气烫伤,往往是被水蒸气烫伤更严重 |
| B.所有有O2参与的反应都是放热反应 |
C.绝热密闭容器,中间活塞能自由移动,在两边各加入等量的反应物,发生如图的反应,反应达到平衡后,最终活塞仍处于正中间,则这两个反应放出或吸收的热量相同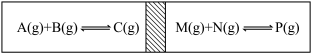 |
D.已知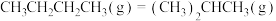 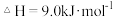 ,则常温下 ,则常温下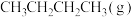 完全燃烧放出的热量比 完全燃烧放出的热量比 完全燃烧放出的热量多9kJ 完全燃烧放出的热量多9kJ |
您最近一年使用:0次
2019-11-08更新
|
397次组卷
|
3卷引用:【新东方】高中化学126



