名校
1 . 下列与化学反应能量变化相关的叙述中错误的是
| A.放热反应的反应速率总是大于吸热反应的反应速率 |
| B.物质发生化学变化一定伴随能量的变化 |
C.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
D.水凝结成冰的过程中, 、 、 |
您最近一年使用:0次
2022-12-09更新
|
488次组卷
|
4卷引用:山东省青岛第二中学2020-2021学年高二上学期期末化学试题
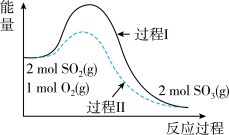
2 . 一定温度下,密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
 2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
2SO3(g) △H。测得能量变化如图所示,下列说法不正确的是
| A.该反应的△H>0 |
| B.反应物断键吸收的总能量小于生成物成键释放的总能量 |
| C.过程Ⅱ可能使用了催化剂,但不可以提高SO2的平衡转化率 |
| D.过程Ⅰ、Ⅱ达到平衡的时间不相同 |
您最近一年使用:0次
解题方法
3 . 化学反应伴随着能量变化,下列说法正确的是
| A.需要加热的反应一定是吸热反应,不需要加热的反应一定是放热反应 |
B.单质硫燃烧热的热化学方程式:S(s)+ O2(g)=SO3(g) ΔH=a kJ·mol-1 O2(g)=SO3(g) ΔH=a kJ·mol-1 |
C.C(s,石墨) C(s,金刚石) ΔH=+1.9 kJ·mol-1,由此推断石墨比金刚石稳定 C(s,金刚石) ΔH=+1.9 kJ·mol-1,由此推断石墨比金刚石稳定 |
| D.已知:2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
解题方法
4 . 回答下列问题
(1)下列反应中,属于放热反应的是__________ ,属于吸热反应的是________ 。
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有______________________ 。
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有____________ ;表示中和热的热化学方程式有_____________________ 。
(1)下列反应中,属于放热反应的是
①水的分解 ②木炭燃烧 ③炸药爆炸 ④Ba(OH)2·8H2O与NH4Cl反应
⑤冰融化 ⑥氢气还原氧化铜 ⑦浓硫酸的稀释 ⑧酸碱中和反应
(2)已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+1/2O2(g)=CO2(g) ΔH=+ 283 kJ·mol-1
⑤H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-517.6 kJ·mol-1
⑧C(s)+1/2O2(g)=CO(g); △H =-393.5 kJ/mol
①上述热化学方程式中,不正确的有
②上述正确的热化学方程式中,表示燃烧热的热化学方程式有
您最近一年使用:0次
5 . 下列过程既是氧化还原反应,又是吸热反应的是
| A.Na2O2溶于水 |
| B.Ba(OH)2·8H2O与NH4Cl(s)混合并搅拌 |
| C.灼热的炭与CO2反应 |
| D.铝热反应 |
您最近一年使用:0次
6 . 将镁条投入到盛有稀硫酸的试管中,发生剧烈反应,用手触摸试管外壁感觉烫手。这个实验事实说明该反应
| A.为放热反应 | B.为化合反应 |
| C.反应过程中热能转化为化学能 | D.反应物的总能量低于生成物的总能量 |
您最近一年使用:0次
21-22高一·全国·假期作业
7 . I.火箭推进器中盛有强还原剂液态肼 和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol
和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol 混合反应,生成氮气和水蒸气,放出256.0kJ的热量(相当于25℃、101kPa下测得的热量)。
混合反应,生成氮气和水蒸气,放出256.0kJ的热量(相当于25℃、101kPa下测得的热量)。
(1)反应的热化学方程式为_______ 。
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___ 。
II.回答下列问题:
(3)在25℃、101kPa下,已知 气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190kJ,该反应的热化学方程式是
气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190kJ,该反应的热化学方程式是_______ 。
(4)根据下图写出反应的热化学方程式:_______ 。
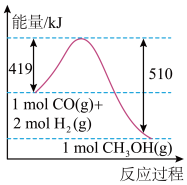
(5)由金红石 制取单质Ti的步骤为:
制取单质Ti的步骤为:
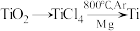
已知:I.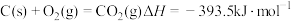
II.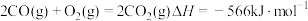
III.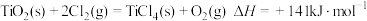
①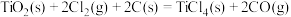 的
的 =
=_______ 。
②反应 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是_______ 。
 和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol
和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol 混合反应,生成氮气和水蒸气,放出256.0kJ的热量(相当于25℃、101kPa下测得的热量)。
混合反应,生成氮气和水蒸气,放出256.0kJ的热量(相当于25℃、101kPa下测得的热量)。(1)反应的热化学方程式为
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
II.回答下列问题:
(3)在25℃、101kPa下,已知
 气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190kJ,该反应的热化学方程式是
气体在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190kJ,该反应的热化学方程式是(4)根据下图写出反应的热化学方程式:

(5)由金红石
 制取单质Ti的步骤为:
制取单质Ti的步骤为: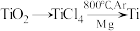
已知:I.
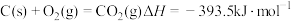
II.
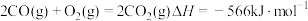
III.
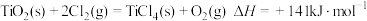
①
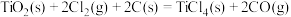 的
的 =
=②反应
 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是
您最近一年使用:0次
解题方法
8 . 2SO2+O2 2SO3该反应是放热反应,下列说法不正确的是
2SO3该反应是放热反应,下列说法不正确的是
 2SO3该反应是放热反应,下列说法不正确的是
2SO3该反应是放热反应,下列说法不正确的是| A.形成SO3中的硫氧键放出能量 |
| B.断开SO2中的硫氧键放出能量 |
| C.反应物的总能量大于生成物的总能量 |
| D.放热反应的逆反应一定是吸热反应 |
您最近一年使用:0次
2022-12-03更新
|
202次组卷
|
2卷引用:江苏省盐城市时杨中学2021-2022学年高二上学期期中考试化学试题
9 . 如图是H2和Cl2反应生成HCl的能量变化示意图,由图可知
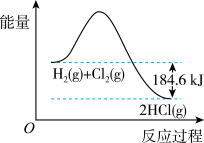

| A.反应物的能量总和于生成物的能量 |
| B.生成1molHCl(g)需放出92.3kJ的能量 |
| C.H2(g) + Cl2(g) → 2HCl(g) - 184.6kJ |
| D.H2(g) + Cl2(g) → 2HCl(g) + Q (Q>184.6kJ) |
您最近一年使用:0次
10 . 下列说法不正确 的是
| A.焦炭在高温下与水蒸气的反应是吸热反应 |
| B.氢氧化钾与硝酸的反应是放热反应 |
| C.化学反应的过程,都可以看成是“贮存”在物质内部的能量转化为热能等而被释放出来的过程 |
| D.燃料在有足量空气的环境中且与空气充分接触就能充分燃烧 |
您最近一年使用:0次



