名校
1 . 合成甲醇的绿色新途径是利用含有 的工业废气为碳源,涉及的主要反应如下:
的工业废气为碳源,涉及的主要反应如下:
Ⅰ.
 kJ⋅mol
kJ⋅mol
Ⅱ.
 kJ⋅mol
kJ⋅mol
Ⅲ. ___________
(1)已知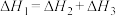 ,写出反应Ⅲ的热化学方程式:
,写出反应Ⅲ的热化学方程式:___________ ; 、
、 与
与 分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,其关系为
分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,其关系为
___________ 。
(2)在恒容密闭容器中通入 与
与 ,使其物质的量浓度均为1.0 mol⋅L
,使其物质的量浓度均为1.0 mol⋅L ,在一定条件下发生反应:
,在一定条件下发生反应: 。测得平衡时
。测得平衡时 的体积分数与温度及压强的关系如图所示。回答下列问题:
的体积分数与温度及压强的关系如图所示。回答下列问题:
___________ (填“<”“>”或“=”)0。
②压强 、
、 、
、 由大到小的顺序为
由大到小的顺序为___________ ;压强为 时,b点处
时,b点处
___________ (填“>”“<”或“=”)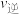 。
。
(3)工业上可利用甲烷还原NO减少氮氧化物的排放。向2 L恒容密闭容器中通入2 mol 、4 mol
、4 mol  ,一定条件下发生反应:
,一定条件下发生反应: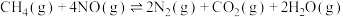 ,测得
,测得 的物质的量随时间变化的关系如表。
的物质的量随时间变化的关系如表。
①下列措施能够加快该反应速率的是___________ (填标号)。
A.使用催化剂 B.升高温度 C.及时分离水 D.充入He增大体系压强
②0~20min内,用NO表示该反应的平均速率为___________ mol⋅L ⋅min
⋅min 。
。
③平衡时, 的体积分数为
的体积分数为___________ 。
④若反应体系中的初始压强为3p,则该反应的压强平衡常数
___________ (只列算式不计算出结果)(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 的工业废气为碳源,涉及的主要反应如下:
的工业废气为碳源,涉及的主要反应如下:Ⅰ.

 kJ⋅mol
kJ⋅mol
Ⅱ.

 kJ⋅mol
kJ⋅mol
Ⅲ. ___________

(1)已知
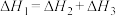 ,写出反应Ⅲ的热化学方程式:
,写出反应Ⅲ的热化学方程式: 、
、 与
与 分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,其关系为
分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,其关系为
(2)在恒容密闭容器中通入
 与
与 ,使其物质的量浓度均为1.0 mol⋅L
,使其物质的量浓度均为1.0 mol⋅L ,在一定条件下发生反应:
,在一定条件下发生反应: 。测得平衡时
。测得平衡时 的体积分数与温度及压强的关系如图所示。回答下列问题:
的体积分数与温度及压强的关系如图所示。回答下列问题: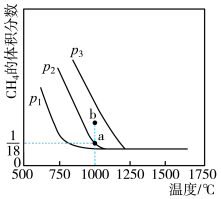

②压强
 、
、 、
、 由大到小的顺序为
由大到小的顺序为 时,b点处
时,b点处
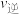 。
。(3)工业上可利用甲烷还原NO减少氮氧化物的排放。向2 L恒容密闭容器中通入2 mol
 、4 mol
、4 mol  ,一定条件下发生反应:
,一定条件下发生反应: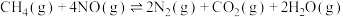 ,测得
,测得 的物质的量随时间变化的关系如表。
的物质的量随时间变化的关系如表。| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
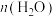 /mol /mol | 0 | 0.6 | 1.0 | 1.3 | 1.5 | 1.5 |
A.使用催化剂 B.升高温度 C.及时分离水 D.充入He增大体系压强
②0~20min内,用NO表示该反应的平均速率为
 ⋅min
⋅min 。
。③平衡时,
 的体积分数为
的体积分数为④若反应体系中的初始压强为3p,则该反应的压强平衡常数

您最近半年使用:0次
2 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。___________ ;
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为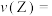
___________ ;
(3)2min反应达到平衡时体系内的压强比起始时的压强___________ (填增大、减小或无变化);平衡时混合气体密度和起始时相比___________ 。(填增大、减小或无变化)
(4)下列措施能加快反应速率的是___________。
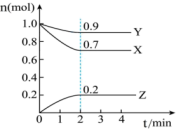
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为
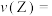
(3)2min反应达到平衡时体系内的压强比起始时的压强
(4)下列措施能加快反应速率的是___________。
| A.升高温度 | B.选择高效的催化剂 | C.恒容时充入X | D.恒容时充入氩气 |
您最近半年使用:0次
解题方法
3 . 某实验小组用酸性 溶液和
溶液和 (草酸)反应研究影响反应速率的因素,反应的方程式为
(草酸)反应研究影响反应速率的因素,反应的方程式为 。他们通过测定单位时间内生成
。他们通过测定单位时间内生成 的体积,探究某种影响化学反应速率的因素,设计方案如下(
的体积,探究某种影响化学反应速率的因素,设计方案如下( 溶液已酸化):
溶液已酸化):
(1)酸性 溶液中所加的酸应是(填字母序号)___________。
溶液中所加的酸应是(填字母序号)___________。
(2)该实验探究的是___________ 对化学反应速率的影响。
(3)实验停止前,相同时间内针筒中所得 体积较大是
体积较大是___________ (填实验序号)。
(4)若实验①在2min末注射器的活塞从最左端(刻度为20mL)向右移动到了V mL的位置,则这段时间内的平均反应速率可表示为
___________  。
。
(5)若实验②在t min收集了2.24mL (标准状况),则t min末
(标准状况),则t min末 的物质的量浓度为
的物质的量浓度为___________  。
。
(6)该小组同学发现反应速率总是如图,其中 ~
~ 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①___________ ,②___________
 溶液和
溶液和 (草酸)反应研究影响反应速率的因素,反应的方程式为
(草酸)反应研究影响反应速率的因素,反应的方程式为 。他们通过测定单位时间内生成
。他们通过测定单位时间内生成 的体积,探究某种影响化学反应速率的因素,设计方案如下(
的体积,探究某种影响化学反应速率的因素,设计方案如下( 溶液已酸化):
溶液已酸化):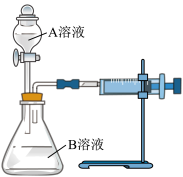
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.2  溶液 溶液 | 30mL 0.01  溶液 溶液 |
| ② | 20mL 0.1  溶液 溶液 | 30mL 0.01  溶液 溶液 |
(1)酸性
 溶液中所加的酸应是(填字母序号)___________。
溶液中所加的酸应是(填字母序号)___________。| A.硫酸 | B.盐酸 | C.硝酸 | D.以上三种酸都可 |
(2)该实验探究的是
(3)实验停止前,相同时间内针筒中所得
 体积较大是
体积较大是(4)若实验①在2min末注射器的活塞从最左端(刻度为20mL)向右移动到了V mL的位置,则这段时间内的平均反应速率可表示为

 。
。(5)若实验②在t min收集了2.24mL
 (标准状况),则t min末
(标准状况),则t min末 的物质的量浓度为
的物质的量浓度为 。
。(6)该小组同学发现反应速率总是如图,其中
 ~
~ 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①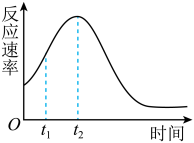
您最近半年使用:0次
名校
解题方法
4 . 实现“碳中和”,综合利用 具有重要的意义。一定条件下,
具有重要的意义。一定条件下, 与
与 制备气态甲醇的反应方程式为
制备气态甲醇的反应方程式为 。
。
(1)一定温度下,在恒容密闭容器中进行该反应,当进行到某一时刻, 、
、 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,反应达到平衡时,下列数据不可能出现的是___________。
,反应达到平衡时,下列数据不可能出现的是___________。
(2)在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。
①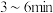 内,
内,
___________ 。
②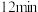 末时,混合气体中
末时,混合气体中 的物质的量分数为
的物质的量分数为___________ 。已知: 的物质的量分数
的物质的量分数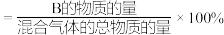 。
。
③第 时
时
___________ 第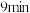 时
时 (填“>”“<”或“=”),第
(填“>”“<”或“=”),第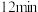 时,
时,
___________ 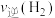 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)保持压强为 ,向密闭容器中投入一定量
,向密闭容器中投入一定量 和
和 发生上述反应,若投料比
发生上述反应,若投料比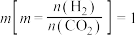 ,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是
,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是___________ (填字母)。
a.容器内气体的密度不再变化
b.容器内气体的平均相对分子质量不再变化
c. 的体积分数不再变化
的体积分数不再变化
d.断裂 个
个 键的同时生成
键的同时生成 个水分子(设
个水分子(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 具有重要的意义。一定条件下,
具有重要的意义。一定条件下, 与
与 制备气态甲醇的反应方程式为
制备气态甲醇的反应方程式为 。
。(1)一定温度下,在恒容密闭容器中进行该反应,当进行到某一时刻,
 、
、 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,反应达到平衡时,下列数据不可能出现的是___________。
,反应达到平衡时,下列数据不可能出现的是___________。A.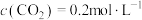 , , |
B. , ,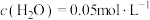 |
C. , ,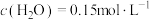 |
D. , ,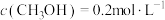 |
 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。时间 | 0 | 3 | 6 | 9 | 12 |
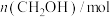 | 0 | 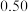 |  |  |  |
 | 1 | 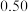 | 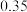 |  |  |
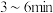 内,
内,
②
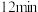 末时,混合气体中
末时,混合气体中 的物质的量分数为
的物质的量分数为 的物质的量分数
的物质的量分数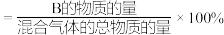 。
。③第
 时
时
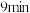 时
时 (填“>”“<”或“=”),第
(填“>”“<”或“=”),第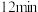 时,
时,
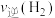 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)保持压强为
 ,向密闭容器中投入一定量
,向密闭容器中投入一定量 和
和 发生上述反应,若投料比
发生上述反应,若投料比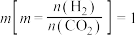 ,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是
,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是a.容器内气体的密度不再变化
b.容器内气体的平均相对分子质量不再变化
c.
 的体积分数不再变化
的体积分数不再变化d.断裂
 个
个 键的同时生成
键的同时生成 个水分子(设
个水分子(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近半年使用:0次
名校
5 . 回答下列问题:
Ⅰ.在一定温度下, 密闭容器内某一反应中气体
密闭容器内某一反应中气体 、气体
、气体 的物质的量随时间变化的曲线如图:
的物质的量随时间变化的曲线如图:___________ 。
(2)比较 时刻,正逆反应速率大小:
时刻,正逆反应速率大小:
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(3) 时刻反应物的转化率为
时刻反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示。
(5)①本实验待测数据可以是___________ ,实验Ⅰ和实验Ⅱ可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是___________ 。
(6)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中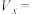
___________ 。
Ⅰ.在一定温度下,
 密闭容器内某一反应中气体
密闭容器内某一反应中气体 、气体
、气体 的物质的量随时间变化的曲线如图:
的物质的量随时间变化的曲线如图: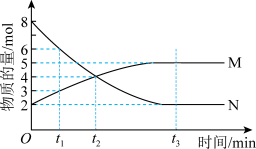
(2)比较
 时刻,正逆反应速率大小:
时刻,正逆反应速率大小:
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(3)
 时刻反应物的转化率为
时刻反应物的转化率为(4)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示。
| 实验序号 | 纯锌粉 |  硫酸溶液 硫酸溶液 | 温度 | 硫酸铜固体 | 加入蒸馏水 |
| Ⅰ |  | 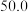 | 25 | 0 | 0 |
| Ⅱ |  |  | 25 | 0 |  |
| Ⅲ |  | 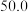 | 25 |  | 0 |
| Ⅳ |  | 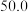 | 25 |  | 0 |
(5)①本实验待测数据可以是
②实验Ⅲ和实验Ⅳ的目的是
(6)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积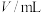 | ||||
 溶液 溶液 | 水 |  溶液 溶液 |  溶液 溶液 | 淀粉溶液 | |
| ① |  |  |  |  |  |
| ② |  |  |  |  |  |
| ③ |  |  |  |  |  |
您最近半年使用:0次
解题方法
6 . 某温度下,在一个 的密闭容器中,加入
的密闭容器中,加入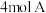 和
和 发生反应:
发生反应: ,反应
,反应 后达到平衡,测得生成
后达到平衡,测得生成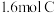 ,则下列说法正确的是
,则下列说法正确的是
 的密闭容器中,加入
的密闭容器中,加入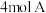 和
和 发生反应:
发生反应: ,反应
,反应 后达到平衡,测得生成
后达到平衡,测得生成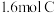 ,则下列说法正确的是
,则下列说法正确的是A.前 ,D的平均反应速率为 ,D的平均反应速率为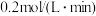 |
B.达到平衡时,B的平衡转化率是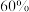 |
| C.升高该体系的温度,化学平衡常数不变 |
| D.增加C,逆向反应速率增大 |
您最近半年使用:0次
名校
7 . Ⅰ. 甲醇是重要的化工原料,发展前景广阔。
温度为T1时,向容积为2L的密闭容器甲、乙中分别充入一定量的CO和H2O(g),发生反应:CO(g) + H2O(g)⇌CO2(g) + H2(g)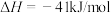 。相关数据如下:
。相关数据如下:
(1)甲容器中,反应在t1 min 内的平均速率v(H2)= ___________ mol/(L·min)。
(2)甲容器中,平衡时,反应放出的热量___________ kJ。
(3)T1时,反应的平衡常数K甲=___________ 。
(4)乙容器中,a=___________ mol。
II.已知:①N2(g)+O2(g) ⇌2NO(g) △H1=+180kJ mol-1
mol-1
②C(s)+O2(g)=CO2(g) △H2=-393kJ mol-1
mol-1
③2C(s)+O2(g)=2CO(g) △H3=-221kJ mol-1
mol-1
(5)若某反应的平衡常数表达式为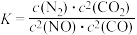 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:___________ 。
(6)欲研究在某催化剂作用下2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如下图所示,A、B两点对应温度下正反应速率变化的原因可能是___________ ,A、B两点对应温度下该反应的活化能Ea(A)___________ Ea(B)(填“>”或“<”)。 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数 =
=___________ 。
(8)用NH3可以消除NO污染:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(1),该反应速率v正=k正 c4(NH3)
c4(NH3) c6(NO),v逆=K逆
c6(NO),v逆=K逆 c5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)-9
c5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)-9 s-1,当平衡时NH3转化率为
s-1,当平衡时NH3转化率为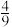 ,v逆=
,v逆=___________ mol L-1
L-1 s-1。
s-1。
温度为T1时,向容积为2L的密闭容器甲、乙中分别充入一定量的CO和H2O(g),发生反应:CO(g) + H2O(g)⇌CO2(g) + H2(g)
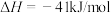 。相关数据如下:
。相关数据如下:| 容器 | 甲 | 乙 | ||
| 反应物 | CO | H2O | CO | H2O |
| 起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
| 平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
| 达到平衡的时间(min) | t1 | t2 | ||
(2)甲容器中,平衡时,反应放出的热量
(3)T1时,反应的平衡常数K甲=
(4)乙容器中,a=
II.已知:①N2(g)+O2(g) ⇌2NO(g) △H1=+180kJ
 mol-1
mol-1②C(s)+O2(g)=CO2(g) △H2=-393kJ
 mol-1
mol-1③2C(s)+O2(g)=2CO(g) △H3=-221kJ
 mol-1
mol-1(5)若某反应的平衡常数表达式为
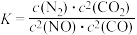 ,请写出此反应的热化学方程式:
,请写出此反应的热化学方程式:(6)欲研究在某催化剂作用下2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如下图所示,A、B两点对应温度下正反应速率变化的原因可能是
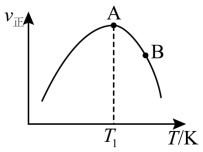
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。在某温度下,原料组成n(CO):n(NO)=1:1,初始总压为100kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20kPa,则该反应的相对压力平衡常数 =
=(8)用NH3可以消除NO污染:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(1),该反应速率v正=k正
 c4(NH3)
c4(NH3) c6(NO),v逆=K逆
c6(NO),v逆=K逆 c5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)-9
c5(N2),若将9molNH3和11molNO投入真空容器中恒温恒容(温度298K、体积为10L)进行反应,已知该条件下k正=6.4×102(mol/L)-9 s-1,当平衡时NH3转化率为
s-1,当平衡时NH3转化率为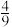 ,v逆=
,v逆= L-1
L-1 s-1。
s-1。
您最近半年使用:0次
8 . 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率 (H2)为
(H2)为____________ mol·L-1·min-1, CO2和H2的转化率比是___________ 。___________ 。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。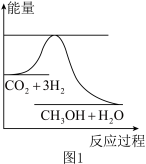
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率
 (H2)为
(H2)为
您最近半年使用:0次
名校
9 . 已知反应: ,其浓度数据如下:
,其浓度数据如下:

当用Y浓度的减少来表示该化学反应的速率时,其速率为
 ,其浓度数据如下:
,其浓度数据如下:
当用Y浓度的减少来表示该化学反应的速率时,其速率为
A.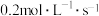 | B.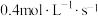 |
C.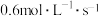 | D. |
您最近半年使用:0次
7日内更新
|
44次组卷
|
2卷引用:云南省临沧市沧源佤族自治县民族中学2022-2023学年高二上学期第二次月考化学试题
名校
解题方法
10 . Ⅰ.某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。___________ 。
(2)反应开始至2min时,B的平均反应速率为___________ 。
(3)能说明该反应已达到平衡状态的是___________ (填字母)。
a.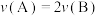 b.容器内压强保持不变
b.容器内压强保持不变
c. d.容器内混合气体的密度保持不变
d.容器内混合气体的密度保持不变
e.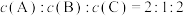 f.混合气体的平均相对分子质量保持不变
f.混合气体的平均相对分子质量保持不变
(4)将a mol A与b mol B的混合气体通入5L的密闭容器中并发生上述反应,反应到某时刻各物质的量恰好满足: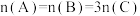 ,则原混合气体中
,则原混合气体中
___________ 。
Ⅱ.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(5)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(6) “即热饭盒”给人们生活带来方便,它可利用下面___________ (填字母)反应释放的热量加热食物。
A,生石灰和水 B.浓硫酸和水
(7)如图是CO和 反应生成
反应生成 的能量变化图,写出该反应的热化学方程式:
的能量变化图,写出该反应的热化学方程式:___________ 。
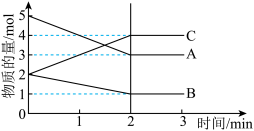
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是
a.
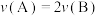 b.容器内压强保持不变
b.容器内压强保持不变c.
 d.容器内混合气体的密度保持不变
d.容器内混合气体的密度保持不变e.
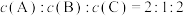 f.混合气体的平均相对分子质量保持不变
f.混合气体的平均相对分子质量保持不变(4)将a mol A与b mol B的混合气体通入5L的密闭容器中并发生上述反应,反应到某时刻各物质的量恰好满足:
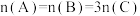 ,则原混合气体中
,则原混合气体中
Ⅱ.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(5)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(6) “即热饭盒”给人们生活带来方便,它可利用下面
A,生石灰和水 B.浓硫酸和水
(7)如图是CO和
 反应生成
反应生成 的能量变化图,写出该反应的热化学方程式:
的能量变化图,写出该反应的热化学方程式: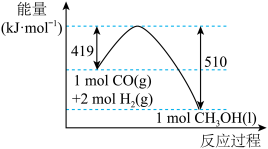
您最近半年使用:0次



