名校
1 .  溶液与
溶液与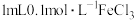 溶液发生反应:
溶液发生反应: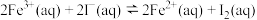 ,达到平衡。下列说法不正确的是
,达到平衡。下列说法不正确的是
 溶液与
溶液与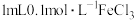 溶液发生反应:
溶液发生反应: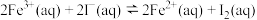 ,达到平衡。下列说法不正确的是
,达到平衡。下列说法不正确的是| A.加入苯,振荡,平衡正向移动 |
| B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈红色,表明该化学反应存在限度 |
C.加入 固体,平衡逆向移动 固体,平衡逆向移动 |
D.该反应的平衡常数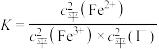 |
您最近半年使用:0次
2 . 目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。___________ 。
(2)温度降低,平衡常数K___________ (填“增大”、“不变”或“减小”)。
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率 (H2)为
(H2)为____________ mol·L-1·min-1, CO2和H2的转化率比是___________ 。___________ 。
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。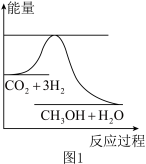
(2)温度降低,平衡常数K
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率
 (H2)为
(H2)为
您最近半年使用:0次
名校
3 . 工业上用CH4催化还原NO2可以消除氮氧化物的污染,反应原理为: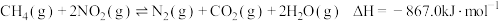 。不同的催化剂催化该反应的最佳活性温度不同。下列说法正确的是
。不同的催化剂催化该反应的最佳活性温度不同。下列说法正确的是
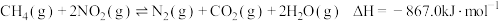 。不同的催化剂催化该反应的最佳活性温度不同。下列说法正确的是
。不同的催化剂催化该反应的最佳活性温度不同。下列说法正确的是A.上述反应平衡常数 |
| B.其他条件不变时,NO2去除率随温度升高而增大的原因可能是催化剂的活性增强或平衡常数变大 |
| C.其他条件不变时,在恒压条件下通入一定量的惰性气体可以提高CH4的平衡转化率 |
| D.反应中若采用高分子分离膜及时分离出水蒸气,可以使正反应速率增大,NO2去除率增大 |
您最近半年使用:0次
4 . 氯气在生产、生活中应用广泛.实验室用 和浓盐酸常温下反应制取
和浓盐酸常温下反应制取 ,工业上用电解饱和食盐水制备
,工业上用电解饱和食盐水制备 ,也可用地康法制备
,也可用地康法制备 .
.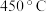 ,以
,以 作催化剂,地康法原理如图所示.氨气可以检验
作催化剂,地康法原理如图所示.氨气可以检验 是否发生泄露,遇
是否发生泄露,遇 泄漏时反应有白烟生成.
泄漏时反应有白烟生成. 可用于制备氯水或含
可用于制备氯水或含 等成分的消毒剂,也可用于处理含氰
等成分的消毒剂,也可用于处理含氰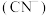 废水.
废水. ,下列说法正确的是
,下列说法正确的是
 和浓盐酸常温下反应制取
和浓盐酸常温下反应制取 ,工业上用电解饱和食盐水制备
,工业上用电解饱和食盐水制备 ,也可用地康法制备
,也可用地康法制备 .
.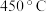 ,以
,以 作催化剂,地康法原理如图所示.氨气可以检验
作催化剂,地康法原理如图所示.氨气可以检验 是否发生泄露,遇
是否发生泄露,遇 泄漏时反应有白烟生成.
泄漏时反应有白烟生成. 可用于制备氯水或含
可用于制备氯水或含 等成分的消毒剂,也可用于处理含氰
等成分的消毒剂,也可用于处理含氰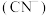 废水.
废水.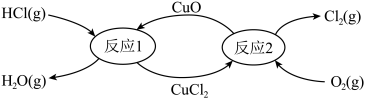
 ,下列说法正确的是
,下列说法正确的是A.反应的平衡常数可表示为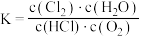 |
B.其他条件不变,升高温度 的平衡转化率降低说明该反应 的平衡转化率降低说明该反应 |
C. 的使用可以增大反应的活化能 的使用可以增大反应的活化能 |
D.每生成 时,转移电子的数目为 时,转移电子的数目为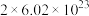 |
您最近半年使用:0次
5 . 碳粉高温下还原 制取纳米级
制取纳米级 :
: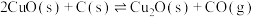
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是
 制取纳米级
制取纳米级 :
: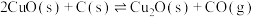
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是A.升高温度, 增大、 增大、 减小 减小 |
B.保持温度不变,通入少量CO,达新平衡后 变大 变大 |
C.加入少量碳粉,可提高 的平衡转化率 的平衡转化率 |
D.分离出CO,有利于 的生成 的生成 |
您最近半年使用:0次
6 . 常温下,用 溶液滴定磷酸的稀溶液,溶液的
溶液滴定磷酸的稀溶液,溶液的 与
与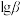 关系如图所示,
关系如图所示, 为
为 、
、 、
、 。下列说法错误的是
。下列说法错误的是
 溶液滴定磷酸的稀溶液,溶液的
溶液滴定磷酸的稀溶液,溶液的 与
与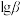 关系如图所示,
关系如图所示, 为
为 、
、 、
、 。下列说法错误的是
。下列说法错误的是
A.直线 表示 表示 与 与 的关系 的关系 |
B.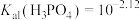 |
C. 的平衡常数为 的平衡常数为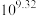 |
D. 点溶液的 点溶液的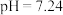 |
您最近半年使用:0次
名校
解题方法
7 . 反应 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
 ,可用于去除氮氧化物。
,可用于去除氮氧化物。 催化该反应的过程如图所示。下列说法正确的是
催化该反应的过程如图所示。下列说法正确的是
A. 位于元素周期表 位于元素周期表 区 区 |
B.反应过程中, 参与反应,降低了反应的焓变 参与反应,降低了反应的焓变 |
C.该反应的平衡常数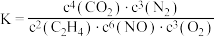 |
D.其他条件不变时,增大 , ,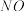 的平衡转化率下降 的平衡转化率下降 |
您最近半年使用:0次
解题方法
8 . 亚硝酰氯(NOCl)是有机物合成中的重要试剂。已知:
①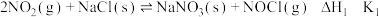
②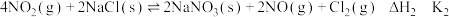
③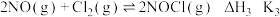
下列关系式正确的是
①
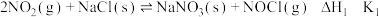
②
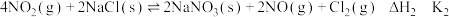
③
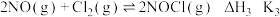
下列关系式正确的是
A. | B. |
C. | D.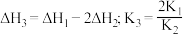 |
您最近半年使用:0次
名校
9 . 可以利用 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是
 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是| A.该反应△S>0 |
B.反应的平衡常数表达式为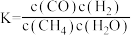 |
| C.上述反应中消耗1molCH4,转移电子的数目约为2×6.02×1023 |
| D.其他条件相同时,增大压强,可以提高CH4的平衡转化率 |
您最近半年使用:0次
名校
10 . 金属硫化物(MxSy)催化反应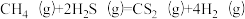 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
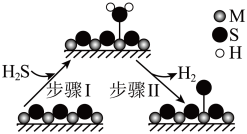
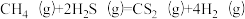 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
A.该反应的 S<0 S<0 |
B.该反应的平衡常数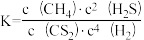 |
| C.其他条件相同,增大体系压强,能提高H2S的平衡转化率 |
| D.题图所示的反应机理中,步骤I可理解为H2S中带部分负电荷的S与催化剂中的M之间发生作用 |
您最近半年使用:0次



