1 . 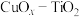 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: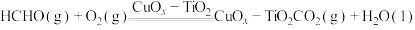 。下列关于
。下列关于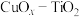 催化氧化甲醛的反应说法正确的是
催化氧化甲醛的反应说法正确的是
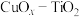 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: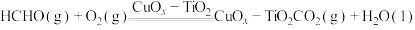 。下列关于
。下列关于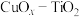 催化氧化甲醛的反应说法正确的是
催化氧化甲醛的反应说法正确的是A.该反应 , , | B.HCHO、 、 、 均为极性分子 均为极性分子 |
C.升高温度, 增大, 增大, 减小 减小 | D.使用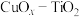 催化剂降低了该反应的焓变 催化剂降低了该反应的焓变 |
您最近半年使用:0次
2 . 烯丙醇是生产甘油、医药、农药、香料和化妆品的中间体。已知烯丙醇与水在一定条件下发生加成反应的原理如下:
Ⅰ:CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1
Ⅱ:CH2=CHCH2OH(g)+H2O(g) CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2
已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
(1)△H2=_______ kJ/mol;反应CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1_______ △S1' (填“>”“=”或“<”)。
(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
(3)已知:反应的压强平衡常数(K)满足方程Kp=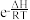 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为_______ 和_______ 。
①该温度下,反应Ⅱ的压强平衡常数K=_______ 。
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将_______ (填“增大”“减小”或“不变”),解释其原因为_______ 。
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
①该条件下,相同时间内,阳极产物中含量最多的为_______ 。
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为_______ 。
Ⅰ:CH2=CHCH2OH(g)+H2O(g)
 HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1Ⅱ:CH2=CHCH2OH(g)+H2O(g)
 CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2 已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
| 物质 | CH2=CHCH2OH(g) | H2O(g) | HOCH2CH2CH2OH(g) | CH3CH(OH)CH2OH(g) |
| 标准摩尔生成焓/(kJ/mol) | -171.8 | -241.8 | -464.9 | -485.7 |
(1)△H2=
 HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
| A.容器内气体的压强不变 | B.容器内温度不变 |
| C.容器内气体的密度不变 | D.容器内气体的平均相对分子质量不变 |
(3)已知:反应的压强平衡常数(K)满足方程Kp=
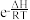 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为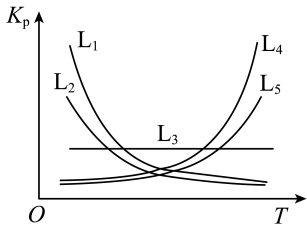
①该温度下,反应Ⅱ的压强平衡常数K=
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
| 反应 | 烯丙醇→丙烯酸 | 烯丙醇→丙烯醛 | 烯丙醇→丙二酸 |
| 活化能(单位:eV) | 8.6a | 2.5 a | 13.7a |
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为
您最近半年使用:0次
解题方法
3 . 下列内容与结论相对应的是
| 选项 | 内容 | 结论 |
| A |  | 该过程的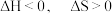 |
| B | 常温下,硝酸铵固体溶于水可自发进行 | 该过程的 |
| C | 一个反应的 | 反应一定不能自发进行 |
| D |  能自发进行 能自发进行 | 则该反应的 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 一块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a),Cu(b)不动。再由Cu(a)、Cu(b)及CuSO4溶液组成电池:Cu(a)|CuSO4(cmol·L-1)|Cu(b),测得电动势E>0,因为Cu(a)的
| A.△S>0,△H=0 | B.△S>0,△H<0 |
| C.△S<0,△H=0 | D.△S<0,△H<0 |
您最近半年使用:0次
5 .  可以作为固态氮肥,并改善土壤酸性,通过
可以作为固态氮肥,并改善土壤酸性,通过 反应制备,下列说法错误的是
反应制备,下列说法错误的是
 可以作为固态氮肥,并改善土壤酸性,通过
可以作为固态氮肥,并改善土壤酸性,通过 反应制备,下列说法错误的是
反应制备,下列说法错误的是| A.该反应为熵增过程 | B.该反应实现了氮的固定 |
| C.该反应需在无水条件下进行 | D. 的电子式为 的电子式为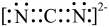 |
您最近半年使用:0次
名校
6 . 可以利用 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是
 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是| A.该反应△S>0 |
B.反应的平衡常数表达式为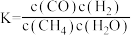 |
| C.上述反应中消耗1molCH4,转移电子的数目约为2×6.02×1023 |
| D.其他条件相同时,增大压强,可以提高CH4的平衡转化率 |
您最近半年使用:0次
名校
7 . 金属硫化物(MxSy)催化反应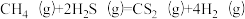 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
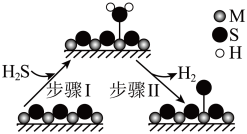
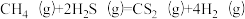 ,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
,既可以除去天然气中的H2S,又可以获得H2.下列说法正确的是
A.该反应的 S<0 S<0 |
B.该反应的平衡常数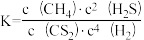 |
| C.其他条件相同,增大体系压强,能提高H2S的平衡转化率 |
| D.题图所示的反应机理中,步骤I可理解为H2S中带部分负电荷的S与催化剂中的M之间发生作用 |
您最近半年使用:0次
解题方法
8 . CaCN2可以作为固态氮肥,并改善土壤酸性,通过 反应制备。下列说法错误的是
反应制备。下列说法错误的是
 反应制备。下列说法错误的是
反应制备。下列说法错误的是| A.该反应为熵增过程 |
| B.该反应实现了氮的固定 |
| C.该反应需在无水条件下进行 |
D. 的电子式为 的电子式为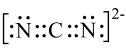 |
您最近半年使用:0次
9 . 高温结构陶瓷氮化硅由石英与焦炭在高温的氮气流中通过以下反应制备: ,下列说法正确的是(
,下列说法正确的是( 为阿伏伽德罗常数的值)
为阿伏伽德罗常数的值)
 ,下列说法正确的是(
,下列说法正确的是( 为阿伏伽德罗常数的值)
为阿伏伽德罗常数的值)A. 和 和 是氧化剂 是氧化剂 | B. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
C.每消耗 转移的电子数为 转移的电子数为 | D.从熵变角度分析,反应更易生成 |
您最近半年使用:0次
2024-04-03更新
|
99次组卷
|
2卷引用:2024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题
10 . 一定条件下,银催化剂表面上存在反应: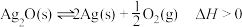 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是

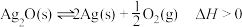 ,起始状态Ⅰ中有
,起始状态Ⅰ中有 、
、 和
和 ,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
,经下列过程达到各平衡状态(已知状态Ⅰ和Ⅲ的固体质量相等),下列叙述正确的是
A.从Ⅰ到Ⅱ的过程 |
B.反应的平衡压强: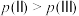 |
C.平衡常数: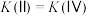 |
D.若体积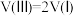 ,则 ,则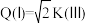 |
您最近半年使用:0次



