1 . 室温下10mL 均为3的醋酸和盐酸两种溶液(不考虑挥发),下列叙述正确的是
均为3的醋酸和盐酸两种溶液(不考虑挥发),下列叙述正确的是
 均为3的醋酸和盐酸两种溶液(不考虑挥发),下列叙述正确的是
均为3的醋酸和盐酸两种溶液(不考虑挥发),下列叙述正确的是A.使温度都升高20℃后,盐酸的 大 大 |
B.分别加水稀释到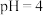 时,盐酸加水多 时,盐酸加水多 |
C.分别加水稀释到100mL后,醋酸溶液的 大 大 |
D.分别加少量的醋酸钠晶体后,盐酸的 增大,醋酸溶液的 增大,醋酸溶液的 减小 减小 |
您最近一年使用:0次
2024-02-02更新
|
182次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—提升篇
解题方法
2 . 人体血液的正常pH范围是7.35—7.45,而缓冲体系对稳定体系的酸碱度发挥重要作用,在人体血液中主要存在的缓冲体系是
A.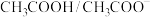 | B.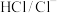 |
C.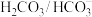 | D.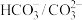 |
您最近一年使用:0次
2024-02-01更新
|
88次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—巩固篇
3 . 常温下,下列事实能证明浓度为 的HA是弱酸的是
的HA是弱酸的是
 的HA是弱酸的是
的HA是弱酸的是A.用电导仪测得其导电能力比 的盐酸弱 的盐酸弱 |
B.将该酸加水稀释10倍后,测得溶液的 |
C.加入等体积 的 的 恰好完全中和 恰好完全中和 |
| D.向该溶液中滴加甲基橙,溶液显红色 |
您最近一年使用:0次
2024-01-28更新
|
177次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—提升篇
解题方法
4 . 华容县有很多风味独特的美食,其中火锅类菜品以酸辣香鲜出名。火锅底料的配料有食盐、白糖、陈醋、味精、辣椒、黄酒、生姜、油脂等。下列配料属于弱电解质的是
| A.C2H5OH | B.CH3COOH | C.NaCl | D.白糖 |
您最近一年使用:0次
2024-01-27更新
|
81次组卷
|
2卷引用:3.1.1强电解质和弱电解质课后作业—基础篇
5 . 常温下,向

 溶液中缓慢滴加
溶液中缓慢滴加 盐酸,溶液中各离子(
盐酸,溶液中各离子( 、
、 、
、 )物质的量随盐酸物质的量的变化如图所示。已知:碳酸
)物质的量随盐酸物质的量的变化如图所示。已知:碳酸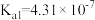 ,
,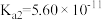 。下列说法正确的是
。下列说法正确的是


 溶液中缓慢滴加
溶液中缓慢滴加 盐酸,溶液中各离子(
盐酸,溶液中各离子( 、
、 、
、 )物质的量随盐酸物质的量的变化如图所示。已知:碳酸
)物质的量随盐酸物质的量的变化如图所示。已知:碳酸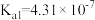 ,
,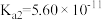 。下列说法正确的是
。下列说法正确的是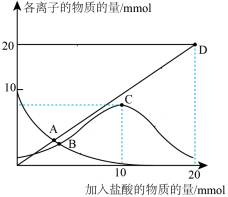
A.A点溶液中所有阴离子为 、 、 、 、 |
B.B点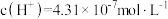 |
C.C点满足关系: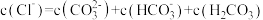 |
| D.从A点至D点,水的电离程度一直增大 |
您最近一年使用:0次
2024-06-24更新
|
90次组卷
|
2卷引用:3.3.1盐类的水解课后作业—提升篇
6 . 常温下,有关下列4种溶液的叙述中错误的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氢氧化钠溶液 | 氨水 | 盐酸 | 醋酸 |
| pH | 11 | 11 | 3 | 3 |
| A.等体积的③、④溶液分别与足量镁反应,生成H2的量:④>③ |
| B.在溶液③④中分别加入适量的醋酸钠固体,两种溶液的pH均增大 |
| C.温度升高至100℃,四种溶液的pH均不变 |
| D.将溶液①④等体积混合,所得溶液显酸性 |
您最近一年使用:0次
2024-01-23更新
|
154次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—提升篇
名校
7 . 向一定浓度的 与
与 的混合液中滴加稀醋酸,溶液导电能力随加入
的混合液中滴加稀醋酸,溶液导电能力随加入 溶液的体积变化如图所示,下列说法错误的是
溶液的体积变化如图所示,下列说法错误的是
 与
与 的混合液中滴加稀醋酸,溶液导电能力随加入
的混合液中滴加稀醋酸,溶液导电能力随加入 溶液的体积变化如图所示,下列说法错误的是
溶液的体积变化如图所示,下列说法错误的是
A. 段,溶液导电能力减弱是由于溶液离子数目基本不变,体积增大,离子浓度减小 段,溶液导电能力减弱是由于溶液离子数目基本不变,体积增大,离子浓度减小 |
B.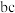 段,发生反应的离子方程式为 段,发生反应的离子方程式为 |
C.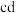 段,由于 段,由于 是弱酸,离子个数减少,故溶液导电能力下降 是弱酸,离子个数减少,故溶液导电能力下降 |
D.d点以后,随着 溶液的滴加,溶液导电能力不可能增强 溶液的滴加,溶液导电能力不可能增强 |
您最近一年使用:0次
2024-01-14更新
|
302次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—提升篇
名校
8 . 下列说法中正确的是
| A.电解氯化铜溶液就是氯化铜的电离 |
| B.电解氯化铜溶液是化学变化,不通电也能发生 |
| C.氯化铜溶液是强电解质 |
| D.电解是最强的氧化还原手段,不能自发进行的氧化还原也可以发生 |
您最近一年使用:0次
名校
解题方法
9 . 在0.1 mol/L的醋酸溶液中,以下微粒数目最小的是
| A.CH3COOH | B.CH3COO- | C.H+ | D.H2O |
您最近一年使用:0次
2024-06-10更新
|
225次组卷
|
3卷引用:3.1.2弱电解质的电离平衡课后作业—基础篇
名校
10 . 常温时,下列关于醋酸溶液的说法中不正确的是
A.向 的醋酸溶液中加入 的醋酸溶液中加入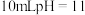 的NaOH溶液,混合液的 的NaOH溶液,混合液的 |
B.向 的醋酸溶液中加入醋酸钠固体,溶液的pH增大 的醋酸溶液中加入醋酸钠固体,溶液的pH增大 |
C.向 的醋酸溶液中加水稀释,醋酸的电离程度增大,但 的醋酸溶液中加水稀释,醋酸的电离程度增大,但 减小 减小 |
D. 醋酸溶液 醋酸溶液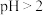 ,说明醋酸为弱电解质 ,说明醋酸为弱电解质 |
您最近一年使用:0次
2024-01-11更新
|
195次组卷
|
2卷引用:3.1.2弱电解质的电离平衡课后作业—提升篇



