名校
1 . 近日,科学家利用光催化剂 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下: 和
和 。
。
②几种氢氧化物沉淀的 如表所示。
如表所示。
回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为_________ 。浸渣1中,除了 外还有一种单质为
外还有一种单质为_________ 。
(2)调 的最低值为
的最低值为_________ 。滤液3可以循环用于“_________ ”工序(填名称)。
(3)“氯化”的化学方程式为___________________________ 。
(4)已知辉铋矿中所含 元素的质量分数为
元素的质量分数为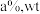 这种矿石经上述转化最终制得
这种矿石经上述转化最终制得 ,则铋的收率为
,则铋的收率为_________ ( )。
)。
(5) 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有_________ 个,相邻2个 的核间距为
的核间距为_________  。
。
 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:
 和
和 。
。②几种氢氧化物沉淀的
 如表所示。
如表所示。氢氧化物 |
|
|
|
开始沉淀 | 7.5 | 1.6 | 4.0 |
沉淀完全 | 9.7 | 3.1 | 5.5 |
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 外还有一种单质为
外还有一种单质为(2)调
 的最低值为
的最低值为(3)“氯化”的化学方程式为
(4)已知辉铋矿中所含
 元素的质量分数为
元素的质量分数为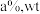 这种矿石经上述转化最终制得
这种矿石经上述转化最终制得 ,则铋的收率为
,则铋的收率为 )。
)。(5)
 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有 的核间距为
的核间距为 。
。
您最近一年使用:0次
2024-03-17更新
|
188次组卷
|
2卷引用:湖南省衡阳市衡阳县2023-2024学年高二下学期7月期末化学试题
名校
解题方法
2 . 钪(Sc)是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪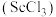 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有 、
、 、
、 、
、 、
、 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下: 难溶于盐酸。
难溶于盐酸。
②常温下,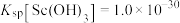 ,
, 。
。
回答下列问题:
(1)某次实验中需要使用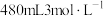 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为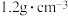 ,质量分数为
,质量分数为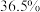 )配制实验所需要的盐酸,则需要量取浓盐酸的体积为
)配制实验所需要的盐酸,则需要量取浓盐酸的体积为___________  。
。
(2)滤渣1的主要成分是___________ (填化学式)。“酸浸”时温度过高,酸浸速率反而减慢,其原因是___________ 。
(3)常温下,“调 ”时,溶液中
”时,溶液中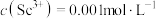 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是___________ (当溶液中某离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
(4)“氧化”时反应的离子方程式为___________ 。
(5)实验室模拟流程中“灼烧”得到 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为___________ ,“加热氯化”步骤中所加入焦炭过量,写出由 制备三氯化钪反应的化学方程式:
制备三氯化钪反应的化学方程式:___________ 。
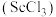 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有 、
、 、
、 、
、 、
、 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下:
 难溶于盐酸。
难溶于盐酸。②常温下,
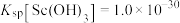 ,
, 。
。回答下列问题:
(1)某次实验中需要使用
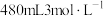 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为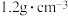 ,质量分数为
,质量分数为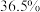 )配制实验所需要的盐酸,则需要量取浓盐酸的体积为
)配制实验所需要的盐酸,则需要量取浓盐酸的体积为 。
。(2)滤渣1的主要成分是
(3)常温下,“调
 ”时,溶液中
”时,溶液中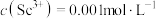 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是(4)“氧化”时反应的离子方程式为
(5)实验室模拟流程中“灼烧”得到
 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为 制备三氯化钪反应的化学方程式:
制备三氯化钪反应的化学方程式:
您最近一年使用:0次
2024-06-04更新
|
116次组卷
|
3卷引用:T16-工业流程题
3 . 硫酸铝是一种具有广泛用途的重要化工产品,以高岭土(含 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[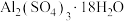 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施_______ (写出一条,合理即可)。
(2)滤渣1经过处理可作为制备水玻璃( 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式_______ 。
(3)加入试剂除铁前,滤液1中的阳离子除了 、
、 外还有的阳离子是
外还有的阳离子是_______ (填离子符号)。滤渣2主要成分为 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理_______ 。
(4)向滤液1中加入的试剂可以是 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因_______ 。
(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于_______ (保留小数点一位)。
(6)某兴趣小组为了测定晶体中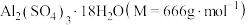 的质量分数,进行如下实验:
的质量分数,进行如下实验:
①准确称取1.00g晶体样品,溶于一定量水中;
②滴入 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。
则晶体中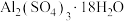 的质量分数是
的质量分数是_______ 。
 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[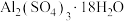 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施
(2)滤渣1经过处理可作为制备水玻璃(
 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式(3)加入试剂除铁前,滤液1中的阳离子除了
 、
、 外还有的阳离子是
外还有的阳离子是 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理(4)向滤液1中加入的试剂可以是
 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于
(6)某兴趣小组为了测定晶体中
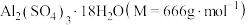 的质量分数,进行如下实验:
的质量分数,进行如下实验:①准确称取1.00g晶体样品,溶于一定量水中;
②滴入
 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。则晶体中
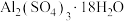 的质量分数是
的质量分数是
您最近一年使用:0次
解题方法
4 . 回答下列问题
(1)已知 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为___________ 。
(2)常温下,用 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡___________ (填“向左”、“向右”或“不”)移动。试计算该溶液中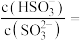
___________ (常温下 的电离平衡常数
的电离平衡常数 ,
, )。
)。
(3)保险粉样品中 的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为
的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为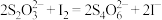 。准确称取
。准确称取 样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用
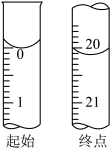
样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用 碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是
碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是___________ 。滴定起始和终点的液面位置如图所示。则样品的纯度为___________ 。(设 的摩尔质量为
的摩尔质量为 )
)
(4)化工生产中常用 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为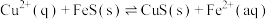 。下列有关叙述正确的是
。下列有关叙述正确的是___________ 。
a、
b、达到平衡时
c、该反应平衡常数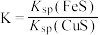
(1)已知
 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为(2)常温下,用
 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡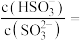
 的电离平衡常数
的电离平衡常数 ,
, )。
)。(3)保险粉样品中
 的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为
的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为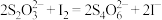 。准确称取
。准确称取 样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用
样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用 碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是
碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是 的摩尔质量为
的摩尔质量为 )
)
(4)化工生产中常用
 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为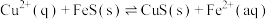 。下列有关叙述正确的是
。下列有关叙述正确的是a、

b、达到平衡时

c、该反应平衡常数
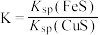
您最近一年使用:0次
名校
解题方法
5 . 铁、镍及其化合物在工业上有广泛的应用。
Ⅰ.从某矿渣[成分为 (铁酸镍)、
(铁酸镍)、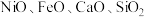 等]中回收
等]中回收 的工艺流程如下:
的工艺流程如下: 在350℃分解生成
在350℃分解生成 和
和 。回答下列问题:
。回答下列问题:
(1)用95℃热水浸泡的目的是________________ ;
(2)矿渣中部分 焙烧时与
焙烧时与 反应生成
反应生成 的化学方程式是
的化学方程式是________ ;
(3)向“浸取液”中加入 以除去溶液中
以除去溶液中 (浓度为
(浓度为 ),除钙率为
),除钙率为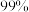 时应控制溶液中
时应控制溶液中 浓度至少是
浓度至少是________  ;
;
(4)从 溶液中获得
溶液中获得 晶体的操作依次是
晶体的操作依次是________ ,过滤,洗涤,干燥;
(5)“煅烧”时剩余固体质量分数与温度变化曲线如右图,该曲线中B段所表示的固体物质的化学式是________ ;
(6)基态镍离子 的核外最外层电子排布式是
的核外最外层电子排布式是________ ;
(7) 晶体结构与
晶体结构与 晶体类似,其晶胞的棱长为
晶体类似,其晶胞的棱长为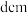 ,则该晶体中距离最近的两个阳离子核间的距离是
,则该晶体中距离最近的两个阳离子核间的距离是________  (用含有
(用含有 的代数式表示)。在一定温度下,
的代数式表示)。在一定温度下, 晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,计算每平方米面积上分散的该晶体的质量是
晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,计算每平方米面积上分散的该晶体的质量是________  (已知氧离子的半径为
(已知氧离子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
Ⅰ.从某矿渣[成分为
 (铁酸镍)、
(铁酸镍)、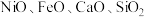 等]中回收
等]中回收 的工艺流程如下:
的工艺流程如下: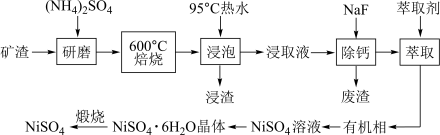
 在350℃分解生成
在350℃分解生成 和
和 。回答下列问题:
。回答下列问题:(1)用95℃热水浸泡的目的是
(2)矿渣中部分
 焙烧时与
焙烧时与 反应生成
反应生成 的化学方程式是
的化学方程式是(3)向“浸取液”中加入
 以除去溶液中
以除去溶液中 (浓度为
(浓度为 ),除钙率为
),除钙率为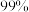 时应控制溶液中
时应控制溶液中 浓度至少是
浓度至少是 ;
;(4)从
 溶液中获得
溶液中获得 晶体的操作依次是
晶体的操作依次是(5)“煅烧”时剩余固体质量分数与温度变化曲线如右图,该曲线中B段所表示的固体物质的化学式是
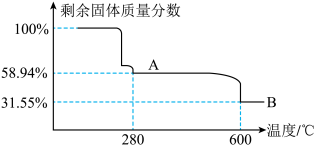
(6)基态镍离子
 的核外最外层电子排布式是
的核外最外层电子排布式是(7)
 晶体结构与
晶体结构与 晶体类似,其晶胞的棱长为
晶体类似,其晶胞的棱长为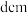 ,则该晶体中距离最近的两个阳离子核间的距离是
,则该晶体中距离最近的两个阳离子核间的距离是 (用含有
(用含有 的代数式表示)。在一定温度下,
的代数式表示)。在一定温度下, 晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,计算每平方米面积上分散的该晶体的质量是
晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,计算每平方米面积上分散的该晶体的质量是 (已知氧离子的半径为
(已知氧离子的半径为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
2024-03-22更新
|
461次组卷
|
4卷引用:湖南省邵阳市2024届高三二模化学试题
名校
解题方法
6 . 过硼酸钠是一种用途广泛的无机过氧化物,可用作织物的漂白、染色,医药上可作为消毒剂和杀菌剂。一种由硼镁矿(Mg2B2O5•H2O)制取过硼酸钠(NaBO3•4H2O)的工艺流程图如下所示。

已知:①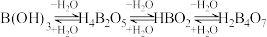 ,若pH>10时,以
,若pH>10时,以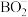 形式存在;若pH<9.6时,以
形式存在;若pH<9.6时,以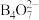 形式存在。
形式存在。
②过硼酸钠为白色晶体,微溶于水,其水溶液不稳定,存在于冷的溶液中,难溶于乙醇。
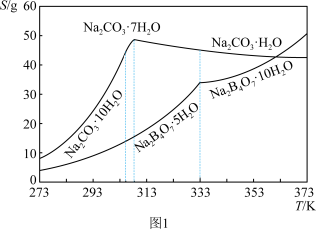
③硼砂(Na2B4O7•10H2O)为白色晶体,溶于水吸热,在水中溶解度如图1所示。
回答下列问题:
(1)步骤Ⅰ中为充分快速使硼镁矿浸出,可采取的措施___________ 。(填两项操作即可)
(2)根据题中信息,写出步骤Ⅱ中的化学方程式___________ 。
(3)下列说法正确的是___________。
(4)步骤Ⅲ的回流反应过程需要控制恒温水浴(0℃左右)的方法是___________ 。
(5)请选出正确的操作排序完成装置A中的回流反应:按图2组装好装置
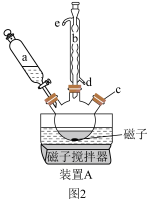
→( )→ ( )→ ( )→打开磁力搅拌器→打开冷凝水→( )→( )。_________
①用纸槽向c处加入硼砂(Na2B4O7•10H2O);
②打开a处旋塞加入双氧水;
③调高恒温水浴温度;
④调低恒温水浴温度;
⑤c处加入氢氧化钠溶液。
(6)已知过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得样品质量随温度的变化如图所示,则T3时所得晶体的化学式为___________ 。
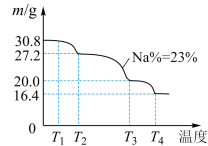
(7)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO2,则产品中钠的质量分数___________ (填“升高”、“降低”或“不变”)。

已知:①
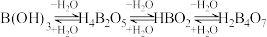 ,若pH>10时,以
,若pH>10时,以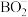 形式存在;若pH<9.6时,以
形式存在;若pH<9.6时,以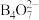 形式存在。
形式存在。②过硼酸钠为白色晶体,微溶于水,其水溶液不稳定,存在于冷的溶液中,难溶于乙醇。
③硼砂(Na2B4O7•10H2O)为白色晶体,溶于水吸热,在水中溶解度如图1所示。

回答下列问题:
(1)步骤Ⅰ中为充分快速使硼镁矿浸出,可采取的措施
(2)根据题中信息,写出步骤Ⅱ中的化学方程式
(3)下列说法正确的是___________。

A.步骤Ⅱ中通入的CO2目的是降低溶液pH值使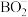 转为 转为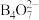 |
| B.步骤Ⅰ、Ⅱ中操作①为过滤,操作②为蒸发浓缩、趁热抽滤 |
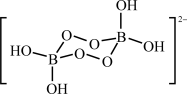
| C.步骤Ⅲ发生化学反应生成过硼酸钠(其阴离子结构如图所示),其中硼元素的化合价升高 |
| D.步骤Ⅳ中宜选用的洗涤剂和干燥方式分别为蒸馏水和减压干燥 |
(5)请选出正确的操作排序完成装置A中的回流反应:按图2组装好装置

→( )→ ( )→ ( )→打开磁力搅拌器→打开冷凝水→( )→( )。
①用纸槽向c处加入硼砂(Na2B4O7•10H2O);
②打开a处旋塞加入双氧水;
③调高恒温水浴温度;
④调低恒温水浴温度;
⑤c处加入氢氧化钠溶液。
(6)已知过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得样品质量随温度的变化如图所示,则T3时所得晶体的化学式为

(7)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO2,则产品中钠的质量分数
您最近一年使用:0次
名校
解题方法
7 . 某废钒渣(主要成分为V2O3,含有少量Al2O3、CaO)为原料生产V2O5的工艺流程如图:
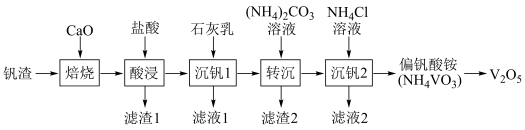
已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为_______ 。
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为_______ 。
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是_______ 。
(4)反应Ca3(VO4)2(s)+3 (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为_______ (用含m,n的代数式表示),已知:Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n。
(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是_______ 。
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知 被还原为Mn2+,假设杂质不参与反应。
被还原为Mn2+,假设杂质不参与反应。
①滴定时装KMnO4溶液为_______ 滴定管(填“酸式”或“碱式”)
②则产品中V2O5的质量分数是_______ (V2O5的摩尔质量为Mg·mol-1)。
(7)下列操作会导致测定的纯度偏高的是_______。

已知:钒酸(H3VO4)是强酸,NH4VO3难溶于水;+5价钒在溶液中的主要存在形式与溶液pH的关系如表。
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO |  | V2O | VO |
(1)向钒渣中加入生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式为
(2)已知Ca(VO3)2难溶于水,可溶于盐酸。若“酸浸”时溶液的pH=4,则Ca(VO3)2溶于盐酸的离子方程式为
(3)已知加入石灰乳后生成Ca3(VO4)2沉淀,则加入石灰乳的作用是
(4)反应Ca3(VO4)2(s)+3
 (aq)⇌2VO
(aq)⇌2VO (aq)+3CaCO3(s)的平衡常数为
(aq)+3CaCO3(s)的平衡常数为(5)沉钒2过程中加入氯化铵溶液,控制溶液的pH=7.5,当pH>8时,NH4VO3的产量明显降低,原因是
(6)测定产品中V2O5的纯度:取ag产品用硫酸溶解得(VO2)2SO4溶液,加入b1mLclmol·L-1(NH4)2Fe(SO4)2溶液(VO
 +2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知
+2H++Fe2+=VO2++Fe3++H2O),再用c2mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知 被还原为Mn2+,假设杂质不参与反应。
被还原为Mn2+,假设杂质不参与反应。①滴定时装KMnO4溶液为
②则产品中V2O5的质量分数是
(7)下列操作会导致测定的纯度偏高的是_______。
| A.锥形瓶水洗后未干燥 |
| B.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| C.滴定终点时俯视读数 |
| D.滴定管用蒸馏水洗净后未用标准溶液润洗 |
您最近一年使用:0次
名校
解题方法
8 . 磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,作为信息产业和机电工业的重要基础功能材料,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要成分为MnO2)和黄铁矿(主要成分为FeS2)为主要原料制备碳酸锰的主要工艺流程如图:
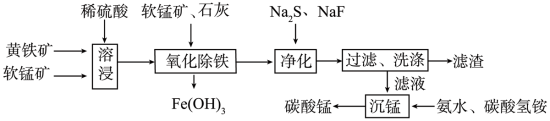
已知:几种金属离子沉淀的pH如表。
回答下列问题:
(1)为了提高溶浸工序中原料的浸出效率,采取的措施不合理的有____ 。
(2)溶浸过程中主要产生的金属阳离子为Fe3+、Mn2+,还含有少量Fe2+、Cu2+、Ca2+。在加入石灰调节溶液的pH前,先加入适量的软锰矿,其发生反应的离子方程式为____ ,加入石灰调节溶液pH的范围为____ 。
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质,故滤渣主要是CaF2和____ (填化学式)。若测得滤液中c(F-)为0.001mol•L-1,则净化工序中Ca2+是否沉淀完全?____ (填“是”或“否”)[已知:Ksp(CaF2)=1.46×10-10]。
(4)有人认为净化工序中使用NaF会引起污染,建议用(NH4)2CO3代替NaF,但是用(NH4)2CO3代替NaF的缺点是____ 。
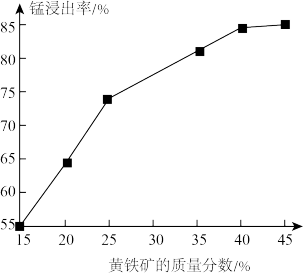
(5)如图为黄铁矿的质量分数对锰浸出率的影响,仅据图中信息,黄铁矿的质量分数应保持在____ %左右。

已知:几种金属离子沉淀的pH如表。
| Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.2 | 3.7 | 7.8 | 10.4 |
回答下列问题:
(1)为了提高溶浸工序中原料的浸出效率,采取的措施不合理的有
| A.搅拌 | B.适当升高温度 | C.研磨矿石 | D.加入足量的水 |
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质,故滤渣主要是CaF2和
(4)有人认为净化工序中使用NaF会引起污染,建议用(NH4)2CO3代替NaF,但是用(NH4)2CO3代替NaF的缺点是
(5)如图为黄铁矿的质量分数对锰浸出率的影响,仅据图中信息,黄铁矿的质量分数应保持在

您最近一年使用:0次
2022-11-12更新
|
295次组卷
|
2卷引用:湖南省长沙市明德中学2022-2023学年高二上学期期中考试化学试题
9 . 锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为 ,含少量
,含少量 、
、 、FeO、
、FeO、 等杂质)为原料制备锰酸锂的流程如下图所示。
等杂质)为原料制备锰酸锂的流程如下图所示。 ,
,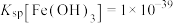 ,
, ,
, 时
时 开始沉淀。
开始沉淀。
回答下列问题:
(1)Mn在元素周期表中的位置是_______ ,基态Mn原子的价电子排布式为_______ 。
(2)“氧化除杂”时使用的试剂X可以选择 溶液或
溶液或 固体,这一步的目的是
固体,这一步的目的是_______ 。
(3)“氧化除杂”时需使溶液中 、
、 浓度小于
浓度小于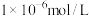 ,则应控制溶液pH范围为
,则应控制溶液pH范围为_______ 。
(4)用过二硫酸钾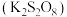 可以缓慢地氧化
可以缓慢地氧化 为
为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(5)反应生成的锰酸锂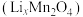 中的Li含量可变,锰酸锂可充电电池的总反应为
中的Li含量可变,锰酸锂可充电电池的总反应为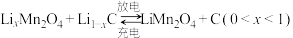 ,装置示意图如图。
,装置示意图如图。_______ 。
②充电时,若有1mol电子转移,石墨电极增重_______ g。
 ,含少量
,含少量 、
、 、FeO、
、FeO、 等杂质)为原料制备锰酸锂的流程如下图所示。
等杂质)为原料制备锰酸锂的流程如下图所示。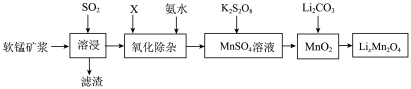
 ,
,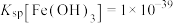 ,
, ,
, 时
时 开始沉淀。
开始沉淀。回答下列问题:
(1)Mn在元素周期表中的位置是
(2)“氧化除杂”时使用的试剂X可以选择
 溶液或
溶液或 固体,这一步的目的是
固体,这一步的目的是(3)“氧化除杂”时需使溶液中
 、
、 浓度小于
浓度小于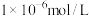 ,则应控制溶液pH范围为
,则应控制溶液pH范围为(4)用过二硫酸钾
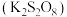 可以缓慢地氧化
可以缓慢地氧化 为
为 ,该反应的离子方程式为
,该反应的离子方程式为(5)反应生成的锰酸锂
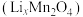 中的Li含量可变,锰酸锂可充电电池的总反应为
中的Li含量可变,锰酸锂可充电电池的总反应为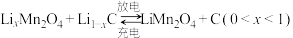 ,装置示意图如图。
,装置示意图如图。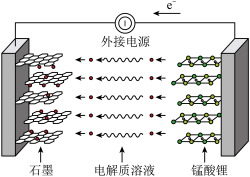
②充电时,若有1mol电子转移,石墨电极增重
您最近一年使用:0次
名校
10 . 钴的消耗量近40%用于充电电池材料,如用于锂离子电池的钴酸锂,用于镍氢电池的氧化亚钴等。钴在地壳中的平均含量为0.001%(质量),大多伴生于镍、铜、铁、铅、锌、银、锰等矿床中。以炼锌净化渣(含有Co、Zn、Fe、Cu、Pb、 等)为原料提取钴的工艺流程如图所示:
等)为原料提取钴的工艺流程如图所示: ,
,
回答下列问题:
(1)为了提高炼锌净化渣的浸出速率,工业上常用的方法是_______ (写两种)。
(2) 的最高能层的电子排布式为
的最高能层的电子排布式为_______ ,“浸出渣”中一定含有的物质为_______ (填化学式)。
(3)119g过硫酸钠( )中含有
)中含有 数目为
数目为_______ ,“氧化”过程中,发生的最主要的离子方程式为_______ 。
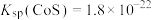
(4) 常用作沉淀剂,在“铜渣”中检测不到
常用作沉淀剂,在“铜渣”中检测不到 ,“除铜液”中
,“除铜液”中 浓度为0.18 mol⋅L
浓度为0.18 mol⋅L ,则此时溶液的
,则此时溶液的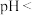
_______ [已知常温下,饱和 水溶液中存在关系式:
水溶液中存在关系式: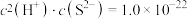 (mol⋅L
(mol⋅L )
) ]。
]。
(5)电动汽车正逐步取代油车,其中大部分电动汽车使用的是钴酸锂( )电池,电解质为一种能传导
)电池,电解质为一种能传导 的高分子材料,电池反应式为:
的高分子材料,电池反应式为: ,充电时阳极的电极反应式为
,充电时阳极的电极反应式为_______ 。用此锂电池电解精炼铜,若电路中通过3mol电子时,阴极增重_______ g。
 等)为原料提取钴的工艺流程如图所示:
等)为原料提取钴的工艺流程如图所示: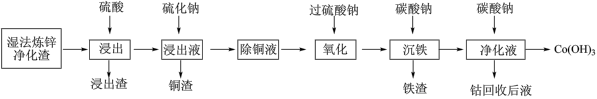
 ,
,
回答下列问题:
(1)为了提高炼锌净化渣的浸出速率,工业上常用的方法是
(2)
 的最高能层的电子排布式为
的最高能层的电子排布式为(3)119g过硫酸钠(
 )中含有
)中含有 数目为
数目为(4)
 常用作沉淀剂,在“铜渣”中检测不到
常用作沉淀剂,在“铜渣”中检测不到 ,“除铜液”中
,“除铜液”中 浓度为0.18 mol⋅L
浓度为0.18 mol⋅L ,则此时溶液的
,则此时溶液的
 水溶液中存在关系式:
水溶液中存在关系式: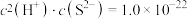 (mol⋅L
(mol⋅L )
) ]。
]。(5)电动汽车正逐步取代油车,其中大部分电动汽车使用的是钴酸锂(
 )电池,电解质为一种能传导
)电池,电解质为一种能传导 的高分子材料,电池反应式为:
的高分子材料,电池反应式为: ,充电时阳极的电极反应式为
,充电时阳极的电极反应式为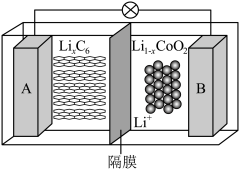
您最近一年使用:0次