名校
解题方法
1 . 镍及其化合物在工业上有广泛用途,以某地红土镍矿(主要成分NiO、MgO、 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示: 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;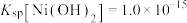 。
。
②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
回答下列问题:
(1)“浸取”时需将矿样研磨的目的是______ ,“滤渣1”的成分______ (填化学式)。
(2)“滤液1”中加入 的作用是
的作用是______ (用离子反应方程式表示)。
(3)操作II为达到实验目的,由表中的数据判断通入 调节溶液pH的范围是
调节溶液pH的范围是______ 。
(4)“滤液1”中是否存在 ,可用
,可用______ 检验。
(5)“沉镍”中pH调为8.5,则滤液中 的浓度为
的浓度为______  。
。
(6)操作V是______ 、过滤、洗涤。
(7) 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为______ 。
 、
、 和铁的氧化物)为原料,采用酸溶法制取
和铁的氧化物)为原料,采用酸溶法制取 和
和 ,工业流程如图所示:
,工业流程如图所示: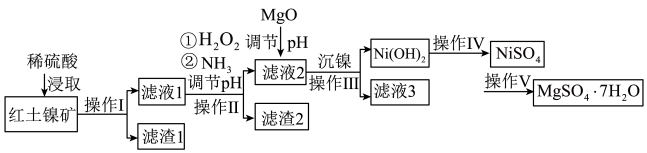
 易溶于水,
易溶于水, 和NiOOH不溶于水;
和NiOOH不溶于水;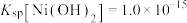 。
。②在上述流程中,某些金属离子开始沉淀和沉淀完全时的pH如下:
沉淀物 |
|
|
|
|
|
开始沉淀时的pH | 7.1 | 7.6 | 2.7 | 3.4 | 9.2 |
沉淀完全( | 9.0 | 9.6 | 3.2 | 4.7 | 11.1 |
(1)“浸取”时需将矿样研磨的目的是
(2)“滤液1”中加入
 的作用是
的作用是(3)操作II为达到实验目的,由表中的数据判断通入
 调节溶液pH的范围是
调节溶液pH的范围是(4)“滤液1”中是否存在
 ,可用
,可用(5)“沉镍”中pH调为8.5,则滤液中
 的浓度为
的浓度为 。
。(6)操作V是
(7)
 在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
在碱性溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH,该反应的离子方程式为
您最近一年使用:0次
2023-02-10更新
|
1084次组卷
|
8卷引用:湖南省株洲市炎陵县2023-2024学年高二下学期开学化学试题
名校
解题方法
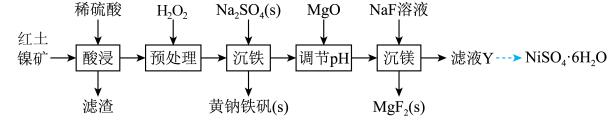
2 . 镍目前有广泛的用途,不仅可以用于不锈钢的制取中,目前也是三元锂电池中的重要元素。由红土镍矿(主要成分为NiO,还含有少量MgO2SiO2以及铁的氧化物等)可以制取黄钠铁矾[Na2Fe6(SO4)4(OH)12]和NiSO4·6H2O。
(1)Ni的价电子排布式为______ 。Ni(CO)4是用于烯烃、H2、CO制备高一级醛的重要催化剂,Ni(CO)4的空间结构类似于CH4分子,其空间结构为______ 。
(2)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是______ (任写一条即可);“预处理”中,发生的离子方程式可能为______ 。
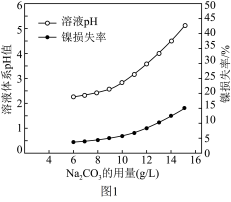
(3)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3溶液的用量对体系pH和镍的损失影响如图1所示。当Na2CO3溶液的用量超过6g/L时,镍的损失率会增大,其可能的原因是______ 。(Fe3+、Ni2+开始沉淀的pH分别为2.2、7.5)
(4)若溶液中c(Mg2+)为0.1mol/L,溶液的体积为1L,则要使溶液中c(Mg2+)=7.4×10-7mol/L,则应加入固体NaF为______ mol[忽略体积的变化,已知Ksp(MgF2)=7.4×10-11]。“沉镁”时应保证MgO已将溶液的pH调节至5.5~6.0的原因是______ 。
(5)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备NiSO4·6H2O的实验方案:______ 。[可选用的试剂:稀硫酸,NaOH溶液、BaCl2溶液、Ca(OH)2、蒸馏水]


(1)Ni的价电子排布式为
(2)为加快红土镍矿的溶解,在酸浸步骤中可以采取的措施是
(3)“沉铁”中若采用Na2CO3作为除铁所需钠源,Na2CO3溶液的用量对体系pH和镍的损失影响如图1所示。当Na2CO3溶液的用量超过6g/L时,镍的损失率会增大,其可能的原因是
(4)若溶液中c(Mg2+)为0.1mol/L,溶液的体积为1L,则要使溶液中c(Mg2+)=7.4×10-7mol/L,则应加入固体NaF为

(5)硫酸钠与硫酸镍晶体溶解度曲线图如图2所示,请设计由滤液Y制备NiSO4·6H2O的实验方案:

您最近一年使用:0次
2023-02-05更新
|
784次组卷
|
2卷引用:湖南省醴陵市第一中学2023届高三第六次月考化学试题
名校
解题方法
3 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.14g聚乙烯与聚丙烯的混合物,含C—H键的数目为2 |
B. 和 和 均能通过化合反应制取 均能通过化合反应制取 |
| C.实验室观察气体燃烧时火焰的颜色所用的尖嘴玻璃管材质为石英玻璃 |
D.碘化银与硫化氢反应的化学方程式: |
您最近一年使用:0次
2023-02-03更新
|
297次组卷
|
4卷引用:湖南省醴陵市第一中学2023届高三第六次月考化学试题
2022·河北·模拟预测
名校
解题方法
4 . 工业上以硼镁矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 、
、 和
和 等)为原料生产硼酸晶体的工艺流程如图所示。
等)为原料生产硼酸晶体的工艺流程如图所示。
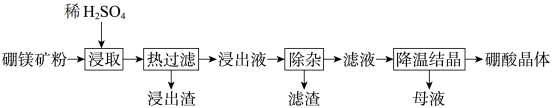
已知:① 的溶解度随温度的升高显著增大;
的溶解度随温度的升高显著增大;
② 、
、 、
、 和
和 以氢氧化物的形式完全沉淀时,溶液的
以氢氧化物的形式完全沉淀时,溶液的 分别为3.2、9.7、5.2和12.4。
分别为3.2、9.7、5.2和12.4。
下列说法错误的是
 ,还含有少量
,还含有少量 、
、 、
、 、
、 和
和 等)为原料生产硼酸晶体的工艺流程如图所示。
等)为原料生产硼酸晶体的工艺流程如图所示。
已知:①
 的溶解度随温度的升高显著增大;
的溶解度随温度的升高显著增大;②
 、
、 、
、 和
和 以氢氧化物的形式完全沉淀时,溶液的
以氢氧化物的形式完全沉淀时,溶液的 分别为3.2、9.7、5.2和12.4。
分别为3.2、9.7、5.2和12.4。下列说法错误的是
| A.“浸取”时要分批慢慢加入稀硫酸 |
B.“热过滤”的目的是防止温度降低时 从溶液中析出 从溶液中析出 |
C.“除杂”时需向“浸出液”中依次加入 和 和 溶液,以除去 溶液,以除去 、 、 、 、 等杂质离子 等杂质离子 |
| D.“母液”中的溶质主要是硫酸镁 |
您最近一年使用:0次
2023-01-20更新
|
691次组卷
|
8卷引用:湖南省攸县第一中学2023届高三第七次月考化学试题
湖南省攸县第一中学2023届高三第七次月考化学试题(已下线)2022年河北省新高考测评卷(一)(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)(已下线)专题14 物质的反应和转化-三年(2020-2022)高考真题分项汇编超重点7 金属与非金属交界处的3种重要元素湖南省常德市第一中学2022-2023学年高三下学期第六次月考化学试题湖南省衡阳八中2022-2023学年高三第四次月考化学试题天津经济技术开发区第一中学(泰达一中)2023-2024学年高三上学期期中考试化学试卷
名校
5 . NOx是主要大气污染物,可用氨催化吸收法除去。
Ⅰ.氨催化吸收法除NOx:某同学采用以下装置或步骤模拟处理过程。回答下列问题:
(1)实验室制备氨气的发生装置,可以选择图中装置中的______ 。(填标号)。
(2)将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按如图装置进行实验。______ (填名称)。
②氨气与NOx反应的化学方程式为______ 。
Ⅱ.从铜氨废液含{[Cu(NH3)3·CO]+、[Cu(NH3)2]2+、[Cu(NH3)4]2+、NH3、CH3COO-、CO 等}中回收铜的工艺流程如图:
等}中回收铜的工艺流程如图:
(3)步骤(I)中被氧化的元素是______ 。
(4)步骤(III)“沉铜”时,利用Na2S溶液而不选用NaOH溶液“沉铜”的优点是______ 。
(5)步骤(IV)反应中,氧化剂与还原剂的物质的量之比为______ 。
(6)碱式氯化铜在400℃时能完全分解为CuO、H2O和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为______ 。
Ⅰ.氨催化吸收法除NOx:某同学采用以下装置或步骤模拟处理过程。回答下列问题:
(1)实验室制备氨气的发生装置,可以选择图中装置中的
A.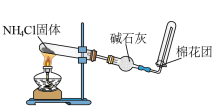 | B.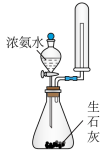 | C.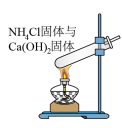 | D.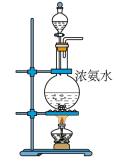 |
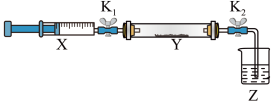
②氨气与NOx反应的化学方程式为
Ⅱ.从铜氨废液含{[Cu(NH3)3·CO]+、[Cu(NH3)2]2+、[Cu(NH3)4]2+、NH3、CH3COO-、CO
 等}中回收铜的工艺流程如图:
等}中回收铜的工艺流程如图: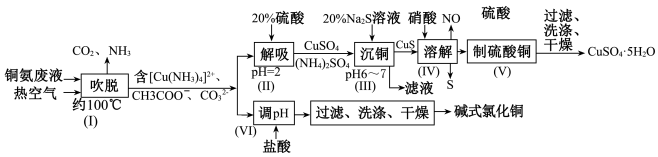
(3)步骤(I)中被氧化的元素是
(4)步骤(III)“沉铜”时,利用Na2S溶液而不选用NaOH溶液“沉铜”的优点是
(5)步骤(IV)反应中,氧化剂与还原剂的物质的量之比为
(6)碱式氯化铜在400℃时能完全分解为CuO、H2O和HCl。为测定碱式氯化铜的组成进行如下实验:准确称取42.9g碱式氯化铜,加热到400℃使其完全分解,剩余固体32.0g,将生成的气体通过浓硫酸的洗气瓶,浓硫酸增重3.6g。碱式氯化铜的化学式为
您最近一年使用:0次
2023-01-04更新
|
228次组卷
|
2卷引用:湖南省株洲市南方中学2023届高三第六次月考化学试题
解题方法
6 . 化学与生产、生活、科技及环境等密切相关。下面说法正确的是
| A.长时间放置的油脂会因水解而变质 |
B.纳米铁粉和FeS都可以高效地去除被污染水体中的 、 、 、 、 等重金属离子,其原理相同 等重金属离子,其原理相同 |
| C.“建本雕版印刷技艺”使用的木质雕版主要成分为纤维素 |
| D.活性炭具有消毒杀菌作用 |
您最近一年使用:0次
7 . 下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向两份蛋白质溶液中分别滴加饱和 | 均有固体析出 | 蛋白质均发生变性 |
B | 淀粉溶液和稀 | 有砖红色沉淀产生 | 淀粉发生了水解 |
C | 将 | 沉淀由白色变为红褐色 | 验证 |
D | 将乙醇和浓硫酸共热至170℃后,将生成的气体通入酸性 |
| 证明乙烯能使 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 25℃时,向10mL 0.05 的
的 溶液中通入氨气,测得溶液中的p(OH)与p(Mg)之间的变化曲线如图所示。已知:
溶液中通入氨气,测得溶液中的p(OH)与p(Mg)之间的变化曲线如图所示。已知: ,
, ,
,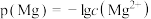 ,忽略反应过程中溶液体积的变化。下列说法正确的是
,忽略反应过程中溶液体积的变化。下列说法正确的是
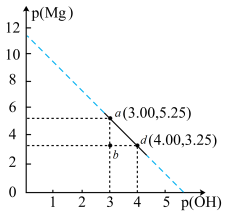
 的
的 溶液中通入氨气,测得溶液中的p(OH)与p(Mg)之间的变化曲线如图所示。已知:
溶液中通入氨气,测得溶液中的p(OH)与p(Mg)之间的变化曲线如图所示。已知: ,
, ,
,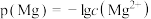 ,忽略反应过程中溶液体积的变化。下列说法正确的是
,忽略反应过程中溶液体积的变化。下列说法正确的是
A.a点溶液满足: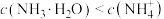 | B.b点溶液中会产生 沉淀 沉淀 |
C.d点溶液满足: | D.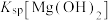 的数量级是 的数量级是 |
您最近一年使用:0次
2022-11-30更新
|
240次组卷
|
5卷引用:湖南省株洲市炎陵县2023-2024学年高二下学期开学化学试题
名校
解题方法
9 . 工业废料的回收是重要的研究课题,铁钴渣其主要成分为Co、Fe、Zn,含少量Pb和 ,图是一种分类回收的工艺流程。
,图是一种分类回收的工艺流程。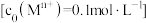 形成氢氧化物沉淀的pH范围如下。
形成氢氧化物沉淀的pH范围如下。
回答下列问题:
(1)提高酸浸出速率的措施有______ (任写两条),铅渣的成分为______ (填化学式)。
(2)“除铁”时,加入试剂A的目的是______ ,生成铁渣需要控制的pH范围为______ 。
(3)“氧化沉钴”时将 转化为CoOOH,则该反应的离子方程式为
转化为CoOOH,则该反应的离子方程式为____________ 。由流程可知, 和
和 的氧化性强弱关系为
的氧化性强弱关系为
______  (填“>”或“<”)。
(填“>”或“<”)。
(4)已知常温下,溶度积常数: ,
,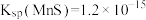 ,且常温下“沉锌”后滤液中
,且常温下“沉锌”后滤液中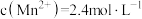 ,则滤液中的
,则滤液中的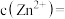
______  。
。
(5)已知:
则“系列操作”得到 晶体的步骤为
晶体的步骤为______ 、洗涤、低温干燥。
 ,图是一种分类回收的工艺流程。
,图是一种分类回收的工艺流程。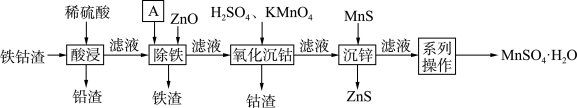
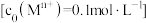 形成氢氧化物沉淀的pH范围如下。
形成氢氧化物沉淀的pH范围如下。| 沉淀物 |  |  |  | 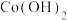 |
| 开始沉淀pH | 8.3 | 2.7 | 7.6 | 7.6 |
| 完全沉淀pH | 9.8 | 3.2 | 9.7 | 9.2 |
(1)提高酸浸出速率的措施有
(2)“除铁”时,加入试剂A的目的是
(3)“氧化沉钴”时将
 转化为CoOOH,则该反应的离子方程式为
转化为CoOOH,则该反应的离子方程式为 和
和 的氧化性强弱关系为
的氧化性强弱关系为
 (填“>”或“<”)。
(填“>”或“<”)。(4)已知常温下,溶度积常数:
 ,
,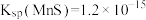 ,且常温下“沉锌”后滤液中
,且常温下“沉锌”后滤液中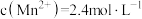 ,则滤液中的
,则滤液中的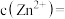
 。
。(5)已知:
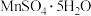 |  | ||||||
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 78 | 82 | 90 | 83 | 72 | 60 | 40 |
 晶体的步骤为
晶体的步骤为
您最近一年使用:0次
2022-11-24更新
|
527次组卷
|
7卷引用:湖南省株洲市第二中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
10 . 下列实验设计方案、现象和结论均正确的是
方案设计 | 现象和结论 | |
A | 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH溶液并加热,冷却到室温后滴加AgNO3溶液 | 产生白色沉淀,则该卤代烃中含有氯元素 |
B | 向2 mL 0.1 mol/L NaOH溶液中加入2 mL 0.1 mol/L MgCl2溶液,再滴加几滴0.1 mol/LFeCl3溶液 | 先产生白色沉淀,再转化为红褐色沉淀,则Ksp[Mg(OH)2]> Ksp[Fe(OH)3] |
C | 室温下,用pH试纸分别测试CH3COONa溶液和NaNO2溶液的pH | pH(CH3COONa)=9,pH(NaNO2)=8,则酸性: HNO2>CH3COOH |
D | 将氯气通入紫色石蕊溶液中 | 溶液先变红后褪色,则氯气具有酸性和漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-19更新
|
419次组卷
|
2卷引用:湖南株洲南方中学2022-2023学年高三第四次月考化学试题




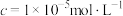 )时的pH
)时的pH 溶液和
溶液和 溶液
溶液 混合加热后,再加NaOH溶液至碱性后加入新制的
混合加热后,再加NaOH溶液至碱性后加入新制的 溶液加入
溶液加入 悬浊液中,振荡
悬浊液中,振荡
 溶液中
溶液中

