1 . 已知溶剂分子结合 的能力会影响酸给出
的能力会影响酸给出 的能力,某温度下部分酸在冰醋酸中的
的能力,某温度下部分酸在冰醋酸中的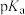 如下表所示,下列说法错误的是
如下表所示,下列说法错误的是
 的能力会影响酸给出
的能力会影响酸给出 的能力,某温度下部分酸在冰醋酸中的
的能力,某温度下部分酸在冰醋酸中的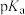 如下表所示,下列说法错误的是
如下表所示,下列说法错误的是| 分子式 |  |  | HCl |  |
 | 4.87 | 7.24(一级) | 8.9 | 9.4 |
A. 在冰醋酸中的电离方程式: 在冰醋酸中的电离方程式: |
B.在冰醋酸中酸性: |
C.结合 的能力: 的能力: |
D.相同温度下醋酸在液氨中的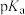 大于其在水中的 大于其在水中的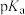 |
您最近半年使用:0次
名校
2 . 下列解释事实的化学用语书写不正确 的是
A.0.1mo/L醋酸溶液 |
B.钢铁制品在潮湿空气中的电化学腐蚀的正极反应: |
C.可用Na2CO3溶液清洗油污: |
D.用饱和Na2CO3溶液处理锅炉水垢中的CaSO4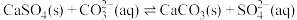 |
您最近半年使用:0次
解题方法
3 . 在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的,如 和
和 。下列方程式不正确的是
。下列方程式不正确的是
 和
和 。下列方程式不正确的是
。下列方程式不正确的是A.氢氧化铍溶于强碱: |
B.可溶性铝盐净水原理: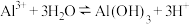 |
C.硅与氢氧化钠溶液反应: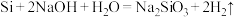 |
D.硼酸的电离方程式: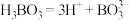 |
您最近半年使用:0次
4 . 下列电离方程式的书写正确的是
A.熔融状态下 的电离: 的电离: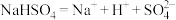 |
B. 水溶液的电离: 水溶液的电离: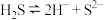 |
C. 的电离: 的电离: |
D.氨水的电离: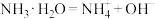 |
您最近半年使用:0次
名校
解题方法
5 . 三氯氧磷( )可用作半导体掺杂剂。工业上采用直接氧化法由
)可用作半导体掺杂剂。工业上采用直接氧化法由 制备
制备 ,反应原理为:
,反应原理为: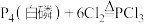 ,
, 。
。
已知: 、
、 的部分性质如下:
的部分性质如下:
某实验小组模拟该工艺设计实验装置如图(部分加热和夹持装置已略去):___________ 。
(2)装置乙的主要作用为:①干燥气体,②___________ ,③___________ 。
(3)装置丙的温度需控制在60-65°℃的原因是___________ 。
(4)提纯 (含少量杂质
(含少量杂质 ),可采用的方法是
),可采用的方法是___________ 。
(5) 遇水生成弱电解质亚磷酸
遇水生成弱电解质亚磷酸 ,已知
,已知 与过量NaOH反应生成
与过量NaOH反应生成 。
。
①写出 的电离方程式:
的电离方程式:___________ 。
② 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为___________ 。
(6)通过测定三氯氧磷产品中Cl元素含量,可进一步计算产品的纯度,实验步骤如下:
I.取mg产品于锥形瓶中,加入足量NaOH溶液,待水解完全后滴加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入 溶液至
溶液至 完全沉淀;
完全沉淀;
Ⅲ.向其中加入少量硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用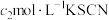 溶液进行滴定,至终点时消耗KSCN溶液
溶液进行滴定,至终点时消耗KSCN溶液 。
。
(已知: 溶于酸,AgSCN是白色沉淀;
溶于酸,AgSCN是白色沉淀;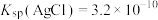 ,
,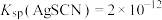 )
)
①步骤Ⅳ中选用的指示剂为___________ 。
A. B.
B. C.淀粉 D.甲基橙
C.淀粉 D.甲基橙
②产品中氯元素的百分含量表达式为:___________ 。
③下列操作会使测得的氯元素含量偏小的是___________ 。
A.配制 标准溶液时仰视容量瓶刻度线
标准溶液时仰视容量瓶刻度线
B.实验过程中未加入硝基苯
C.滴定前滴定管尖嘴处有气泡,滴定后无气泡
D.滴定时锥形瓶未干燥
 )可用作半导体掺杂剂。工业上采用直接氧化法由
)可用作半导体掺杂剂。工业上采用直接氧化法由 制备
制备 ,反应原理为:
,反应原理为: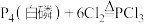 ,
, 。
。已知:
 、
、 的部分性质如下:
的部分性质如下:| 熔点/℃ | 沸点/℃ | 其它 | |
 | -112 | 75.5 |  和 和 互溶,均为无色液体,遇水均剧烈水解 互溶,均为无色液体,遇水均剧烈水解 |
 | 2 | 105.3 |
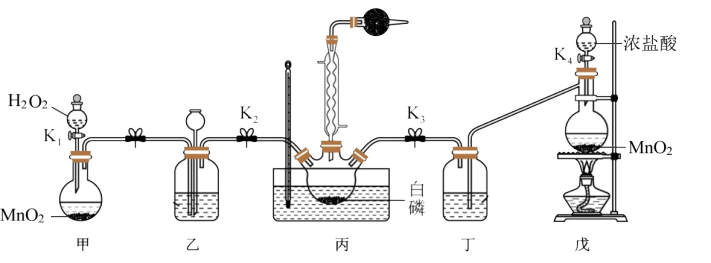
(2)装置乙的主要作用为:①干燥气体,②
(3)装置丙的温度需控制在60-65°℃的原因是
(4)提纯
 (含少量杂质
(含少量杂质 ),可采用的方法是
),可采用的方法是(5)
 遇水生成弱电解质亚磷酸
遇水生成弱电解质亚磷酸 ,已知
,已知 与过量NaOH反应生成
与过量NaOH反应生成 。
。①写出
 的电离方程式:
的电离方程式:②
 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为(6)通过测定三氯氧磷产品中Cl元素含量,可进一步计算产品的纯度,实验步骤如下:
I.取mg产品于锥形瓶中,加入足量NaOH溶液,待水解完全后滴加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入
 溶液至
溶液至 完全沉淀;
完全沉淀;Ⅲ.向其中加入少量硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用
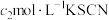 溶液进行滴定,至终点时消耗KSCN溶液
溶液进行滴定,至终点时消耗KSCN溶液 。
。(已知:
 溶于酸,AgSCN是白色沉淀;
溶于酸,AgSCN是白色沉淀;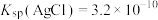 ,
,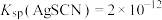 )
)①步骤Ⅳ中选用的指示剂为
A.
 B.
B. C.淀粉 D.甲基橙
C.淀粉 D.甲基橙②产品中氯元素的百分含量表达式为:
③下列操作会使测得的氯元素含量偏小的是
A.配制
 标准溶液时仰视容量瓶刻度线
标准溶液时仰视容量瓶刻度线B.实验过程中未加入硝基苯
C.滴定前滴定管尖嘴处有气泡,滴定后无气泡
D.滴定时锥形瓶未干燥
您最近半年使用:0次
名校
解题方法
6 . 已知五种前四周期的元素X、Y、Z、Q、T。其中,基态X原子的M层上有6种运动状态不同的电子;基态Y原子的简化电子排布式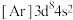 ,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
(1)试推断这五种元素的符号:X:_____ ,Y:_____ ,Z:_____ ,Q:_____ ,T:_____ 。
(2)Y在元素周期表中的位置为_____________ 。
(3)基态Z原子的轨道表示式为_____________ 。
(4)对于T原子的p轨道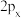 、
、 、
、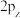 间的差异,下列说法错误的是
间的差异,下列说法错误的是____ (填字母)。
a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为______________ 。
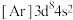 ,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:
,基态Z原子的L层的p能级有一个空轨道;基态Q原子的L层的p能级只有一对成对电子;基态T原子的M层上p轨道为半充满状态。根据题给信息,回答问题:(1)试推断这五种元素的符号:X:
(2)Y在元素周期表中的位置为
(3)基态Z原子的轨道表示式为
(4)对于T原子的p轨道
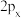 、
、 、
、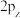 间的差异,下列说法错误的是
间的差异,下列说法错误的是a.电子云形状相同 b.原子轨道的对称类型不同
c.电子的能量不同 d.电子云空间伸展方向不同
(5)Z元素的最高价氧化物对应水化物的电离方程式为
您最近半年使用:0次
名校
解题方法
7 . 已知如下四种物质① ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式_____ 。
2.向②的溶液中滴加几滴浓盐酸,平衡_____ 移动(填“正向”、“逆向”或“不移动”),平衡时溶液中
_____ (填“增大”、“减小”或者“不变”),
_____ (填“增大”、“减小”或者“不变”)。
3.将 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是_____ (填化学式),该溶液显酸性,原因是_____ (请用文字结合该溶液中两个相关平衡方程式加以说明)。
4.将标准状况下2.24L④缓慢通入 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为_____ ,该溶液中各离子浓度大小关系_____ 。
5.将足量④缓慢通入 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度_____ 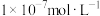 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH_____ (填“增大”、“减小”、或“不变”)。
 ②
② ③NaOH④
③NaOH④
1.写出①的电离方程式
2.向②的溶液中滴加几滴浓盐酸,平衡


3.将
 的①溶液和
的①溶液和 的③溶液等体积混合后得到的溶液中主要溶质是
的③溶液等体积混合后得到的溶液中主要溶质是4.将标准状况下2.24L④缓慢通入
 的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为
的③的溶液中,气体被充分吸收,得到碳酸钠与碳酸氢钠物质的量之比为5.将足量④缓慢通入
 的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度
的③的溶液中,充分反应后所得溶液显碱性,则溶液中水电离出的氢氧根离子浓度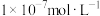 (填“大于”、“小于”、或“等于”),加水稀释后pH
(填“大于”、“小于”、或“等于”),加水稀释后pH
您最近半年使用:0次
解题方法
8 . 氮的常见氢化物有氨 和肼
和肼 。
。 与水反应可产生
与水反应可产生 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生
、K)反应产生 。
。 中一个H被
中一个H被 取代可得
取代可得 ,常温下
,常温下 为液体,具有很高的燃烧热
为液体,具有很高的燃烧热 。以硫酸为电解质,通过催化电解可将
。以硫酸为电解质,通过催化电解可将 转化为
转化为 ;碱性条件下,
;碱性条件下, 氧化
氧化 也可制备
也可制备 。下列说法正确的是
。下列说法正确的是
 和肼
和肼 。
。 与水反应可产生
与水反应可产生 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生
、K)反应产生 。
。 中一个H被
中一个H被 取代可得
取代可得 ,常温下
,常温下 为液体,具有很高的燃烧热
为液体,具有很高的燃烧热 。以硫酸为电解质,通过催化电解可将
。以硫酸为电解质,通过催化电解可将 转化为
转化为 ;碱性条件下,
;碱性条件下, 氧化
氧化 也可制备
也可制备 。下列说法正确的是
。下列说法正确的是A. 中 中 键与π键的数目比例为 键与π键的数目比例为 |
B.液氨电离可表示为: |
C. 的结构式为 的结构式为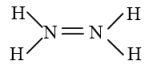 |
D. 中存在 中存在 与 与 之间的强烈相互作用 之间的强烈相互作用 |
您最近半年使用:0次
9 . 按要求填空:
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为___________ 。
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式___________ 。
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:___________ 。
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:___________ 。
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式___________ 。
(1)某元素的最外层电子排布式是4s24p5,则其元素符号为
(2)写出以惰性电极为材料电解饱和MgCl2溶液的离子方程式
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出H3BO3在水中的电离方程式:
(4)50mL0.50mol/LHCl溶液与50mL0.55mol/LNaOH溶液充分反应,测得此过程放出akJ的热量,写出该过程表示中和热(数值要求化简)的热化学方程式:
(5)将AlCl3溶液蒸干并灼烧得不到无水AlCl3,但将SOCl2(亚硫酰氯)与AlCl3·6H2O混合并加热,可获得无水AlCl3,试写出此混合加热过程的化学方程式
您最近半年使用:0次
10 . 下列方程式与所给事实相符的是
A.常温下,0.1mol·L-1 H3PO4溶液pH约为3.1:H3PO4=3H++PO |
B.还原铁粉与水蒸气反应有可燃性气体产生:3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
| C.向H218O中加入Na2O2,产生无色气体:2H218O+2Na2O2=4Na++4OH-+18O2↑ |
D.向NH4HSO4溶液中滴加过量NaOH溶液,产生无色气体:NH +OH-=NH3↑+H2O +OH-=NH3↑+H2O |
您最近半年使用:0次



