1 . 在一定条件下,饱和NaHCO3溶液中存在下列平衡:HCO
 H++CO
H++CO 。欲提高该溶液中CO
。欲提高该溶液中CO 的浓度,可采用的方法是(忽略溶液体积变化)
的浓度,可采用的方法是(忽略溶液体积变化)

 H++CO
H++CO 。欲提高该溶液中CO
。欲提高该溶液中CO 的浓度,可采用的方法是(忽略溶液体积变化)
的浓度,可采用的方法是(忽略溶液体积变化)| A.通入少量氨气 | B.加入少量NaOH固体 |
| C.加入少量冰醋酸 | D.加入少量NaHCO3固体 |
您最近半年使用:0次
名校
2 . 在一定温度下,冰醋酸加水稀释过程中的导电能力变化如图所示,请回答:
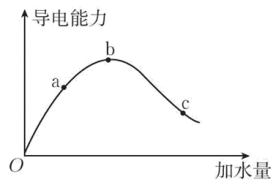
(1)“O”点导电能力为0的理由是___________ 。
(2)a、b、c三点,溶液中c(H+)由大到小的顺序为___________ 。
(3)若使c点溶液中c(CH3COO-)增大,溶液的c(H+)减小,可采取的措施有:
①___________
②___________
③___________ 。

(1)“O”点导电能力为0的理由是
(2)a、b、c三点,溶液中c(H+)由大到小的顺序为
(3)若使c点溶液中c(CH3COO-)增大,溶液的c(H+)减小,可采取的措施有:
①
②
③
您最近半年使用:0次
名校
3 . 下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近半年使用:0次
名校
4 . 下列事实中不能用勒夏特列原理来解释的是
| A.500℃左右比室温更有利于合成氨的反应(合成氨放热反应) |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.高压对合成氨有利 |
| D.向H2S水溶液中加入NaOH有利于S2-增多 |
您最近半年使用:0次
名校
5 . 常温下,一种解释乙酰水杨酸(用 表示,
表示, )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
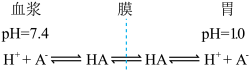
假设离子不会穿过组织薄膜,而未电离的 则可自由穿过该膜且达到平衡。下列说法错误的是
则可自由穿过该膜且达到平衡。下列说法错误的是
 表示,
表示, )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
假设离子不会穿过组织薄膜,而未电离的
 则可自由穿过该膜且达到平衡。下列说法错误的是
则可自由穿过该膜且达到平衡。下列说法错误的是A.血浆中 电离程度比胃中大 电离程度比胃中大 | B.在胃中, |
C.在血浆中, | D.血浆与胃中 相同 相同 |
您最近半年使用:0次
2023-12-15更新
|
1373次组卷
|
7卷引用:辽宁省辽东南协作校2023-2024学年高二上学期12月月考化学(A卷)试题
辽宁省辽东南协作校2023-2024学年高二上学期12月月考化学(A卷)试题(已下线)化学01(14+4模式)2024年1月“九省联考”考前化学猜想卷江西省上饶市婺源县天佑中学2023-2024学年高二上学期12月考试化学试题吉林省梅河口市第五中学2023-2024学年高二上学期12月月考化学试题江西省上饶市第一中学2023-2024学年高二下学期开学考试化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
6 . 金属钒在新能源动力电池中有重要作用。含钒尖晶石是钒渣中最主要的含钒物相,其主要成分有V2O3、FeO、Fe2O3、Al2O3、SiO2,采用以下工艺流程制备V2O5。
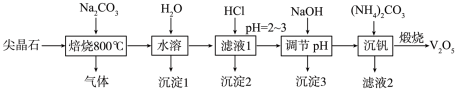
已知:溶液的酸性较强时,+5价钒主要以 的形式存在。
的形式存在。
(1)“焙烧”过程中被氧化的元素是___________ 。
(2)“焙烧"时,V2O3与Na2CO3反应的化学方程式是___________ 。
(3)“沉淀1”的成分是___________ 。
(4)“沉淀2”加热分解后固体产物的用途___________ (任写一种)。
(5)“沉钒”析出NH4VO3晶体时,需要加入过量(NH4)2CO3,其原因_____ (结合平衡移动原理解释)。
(6)沉钒过程中,沉钒率随溶液pH的变化如图1所示。沉钒率随溶液pH的增加先升高后降低的原因可能是___________ 。

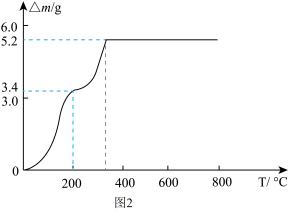
(7)取23.4 g NH4VO3固体加热时,固体减少的质量(△m)随温度的变化曲线如图2所示。加热到200℃时,产生气体的分子式是___________ 。

已知:溶液的酸性较强时,+5价钒主要以
 的形式存在。
的形式存在。(1)“焙烧”过程中被氧化的元素是
(2)“焙烧"时,V2O3与Na2CO3反应的化学方程式是
(3)“沉淀1”的成分是
(4)“沉淀2”加热分解后固体产物的用途
(5)“沉钒”析出NH4VO3晶体时,需要加入过量(NH4)2CO3,其原因
(6)沉钒过程中,沉钒率随溶液pH的变化如图1所示。沉钒率随溶液pH的增加先升高后降低的原因可能是

(7)取23.4 g NH4VO3固体加热时,固体减少的质量(△m)随温度的变化曲线如图2所示。加热到200℃时,产生气体的分子式是

您最近半年使用:0次
7 . 已知25℃时,关于0.1mol/L醋酸溶液( ),下列说法正确的是
),下列说法正确的是
 ),下列说法正确的是
),下列说法正确的是A.升高温度,醋酸的电离程度增大, 增大 增大 |
B.向该溶液中通入HCl气体,平衡逆向移动, 减小 减小 |
| C.该温度下,该溶液中醋酸的电离程度大于0.01mol/L醋酸溶液中醋酸的电离程度 |
D.加水稀释后,溶液中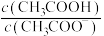 增大 增大 |
您最近半年使用:0次
2023-11-09更新
|
511次组卷
|
5卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期中考试化学试题
名校
8 . 已知:① 是二元弱酸;②
是二元弱酸;②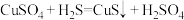 ,向
,向 溶液中通入或加入少量的以下物质:①
溶液中通入或加入少量的以下物质:① ;②
;② ;③
;③ 。其中能使溶液中
。其中能使溶液中 增大的是
增大的是
 是二元弱酸;②
是二元弱酸;②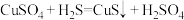 ,向
,向 溶液中通入或加入少量的以下物质:①
溶液中通入或加入少量的以下物质:① ;②
;② ;③
;③ 。其中能使溶液中
。其中能使溶液中 增大的是
增大的是| A.①② | B.②③ | C.①③ | D.①②③ |
您最近半年使用:0次
名校
9 . 在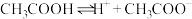 形成的平衡中,要使
形成的平衡中,要使 的电离程度及
的电离程度及 都增大,可采取的措施是
都增大,可采取的措施是
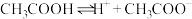 形成的平衡中,要使
形成的平衡中,要使 的电离程度及
的电离程度及 都增大,可采取的措施是
都增大,可采取的措施是| A.通入HCl | B.加少量NaOH固体 | C.升温 | D.加水 |
您最近半年使用:0次
解题方法
10 . 某二元有机弱酸 易溶于水,向1.0L
易溶于水,向1.0L 溶液中加入NaOH固体,保持溶液为常温,测得pX随着pH的变化曲线如图所示。已知:
溶液中加入NaOH固体,保持溶液为常温,测得pX随着pH的变化曲线如图所示。已知: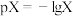 [
[ 为
为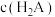
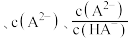 ]。下列说法正确的是
]。下列说法正确的是

 易溶于水,向1.0L
易溶于水,向1.0L 溶液中加入NaOH固体,保持溶液为常温,测得pX随着pH的变化曲线如图所示。已知:
溶液中加入NaOH固体,保持溶液为常温,测得pX随着pH的变化曲线如图所示。已知: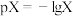 [
[ 为
为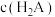
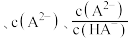 ]。下列说法正确的是
]。下列说法正确的是
A.曲线甲表示 随着溶液pH的变化曲线 随着溶液pH的变化曲线 |
B.常温时, 的两级电离常数的关系: 的两级电离常数的关系: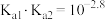 |
| C.NaHA溶液使pH试纸变蓝 |
D. 时, 时,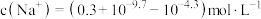 |
您最近半年使用:0次



