解题方法
1 . 利用氟磷灰石[主要成分为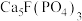 杂质为
杂质为 等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾(
等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾( ),工艺流程如下。
),工艺流程如下。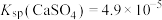 ,
,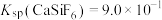 ,
,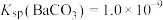 ,
,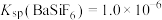 ,
,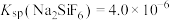 。
。
(1)“酸浸Ⅰ”中生成 ,其化学方程式为
,其化学方程式为______ 。
(2)“酸浸Ⅱ”中,滤渣的主要成分为______ 。
(3)“脱氟”中试剂X为______ (填“ ”或“
”或“ ”);当
”);当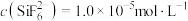 时,溶液中试剂X电离出的剩余金属阳离子的浓度为
时,溶液中试剂X电离出的剩余金属阳离子的浓度为______  。
。
(4)“中和法”为获得较高纯度的 ,控制pH范围为
,控制pH范围为______ ;在此pH范围内纯度的 溶液中各微粒浓度大小关系为
溶液中各微粒浓度大小关系为______ 。
已知:溶液中 、
、 、
、 、
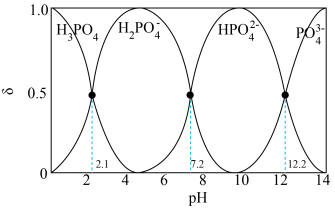
、 的分布分数
的分布分数 随pH变化曲线如图。[如
随pH变化曲线如图。[如 分布分数:
分布分数: ]
]______ 。
②分析产品室可得到 的原因
的原因______ 。
③相较于“中和法”,“电解法”的优点有______ (写出2条即可)。
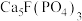 杂质为
杂质为 等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾(
等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾( ),工艺流程如下。
),工艺流程如下。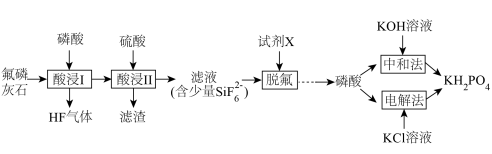
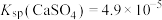 ,
,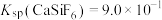 ,
,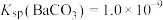 ,
,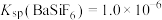 ,
,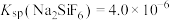 。
。(1)“酸浸Ⅰ”中生成
 ,其化学方程式为
,其化学方程式为(2)“酸浸Ⅱ”中,滤渣的主要成分为
(3)“脱氟”中试剂X为
 ”或“
”或“ ”);当
”);当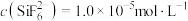 时,溶液中试剂X电离出的剩余金属阳离子的浓度为
时,溶液中试剂X电离出的剩余金属阳离子的浓度为 。
。(4)“中和法”为获得较高纯度的
 ,控制pH范围为
,控制pH范围为 溶液中各微粒浓度大小关系为
溶液中各微粒浓度大小关系为已知:溶液中
 、
、 、
、 、
、 的分布分数
的分布分数 随pH变化曲线如图。[如
随pH变化曲线如图。[如 分布分数:
分布分数: ]
]
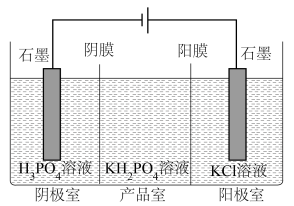
②分析产品室可得到
 的原因
的原因③相较于“中和法”,“电解法”的优点有
您最近半年使用:0次
2 . 已知 的
的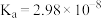 ,
, 的
的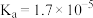 ,下列有关说法正确的是
,下列有关说法正确的是
 的
的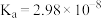 ,
, 的
的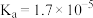 ,下列有关说法正确的是
,下列有关说法正确的是A.温度一定时在 的叠氮酸中加入少量 的叠氮酸中加入少量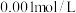 的稀盐酸,溶液的 的稀盐酸,溶液的 不会改变 不会改变 |
B.等浓度等体积的 和溶液 和溶液 前者所含离子总数比后者多 前者所含离子总数比后者多 |
C.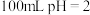 的新制氯水中: 的新制氯水中: |
D.将 通入 通入 溶液中,若溶液呈中性,则溶液中存在4种微粒 溶液中,若溶液呈中性,则溶液中存在4种微粒 |
您最近半年使用:0次
解题方法
3 . 已知某二元弱酸为 ,常温下,向某浓度的
,常温下,向某浓度的 溶液中逐滴加入一定物质的量浓度的
溶液中逐滴加入一定物质的量浓度的 溶液,混合溶液的
溶液,混合溶液的 与离子浓度的关系如图所示。下列说法错误的是
与离子浓度的关系如图所示。下列说法错误的是
 ,常温下,向某浓度的
,常温下,向某浓度的 溶液中逐滴加入一定物质的量浓度的
溶液中逐滴加入一定物质的量浓度的 溶液,混合溶液的
溶液,混合溶液的 与离子浓度的关系如图所示。下列说法错误的是
与离子浓度的关系如图所示。下列说法错误的是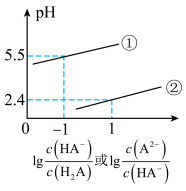
A.曲线②表示 与 与 的变化关系 的变化关系 |
B.物质的量浓度相等的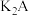 和 和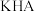 混合溶液中,离子浓度大小关系为: 混合溶液中,离子浓度大小关系为: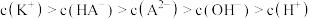 |
C.常温下, 的 的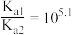 |
D.常温下, 的 的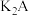 溶液中水电离产生的 溶液中水电离产生的 为 为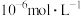 |
您最近半年使用:0次
4 . 盐与碱的反应是水溶液中常见的反应,某学习小组展开相关探究。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=
①步骤a需要称量NaOH固体为______ g(保留一位小数)
②步骤b需要用到下图所示仪器中的______ (填名称)。______ mol·g-1
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关
(2)NH4Cl溶液显酸性,用离子方程式解释原因:______ 。
(3)小组同学设计实验探究[c )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
①实验结果显示,NaCl溶液不具备抗碱能力,即曲线______ (填曲线标号)表示溶液1.
②实验结果显示,当[c( )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液______ (填溶液组号)
③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=______ (精确至小数点后1位)。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=

①步骤a需要称量NaOH固体为
②步骤b需要用到下图所示仪器中的
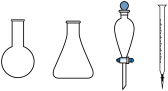
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与
 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关(2)NH4Cl溶液显酸性,用离子方程式解释原因:
(3)小组同学设计实验探究[c
 )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示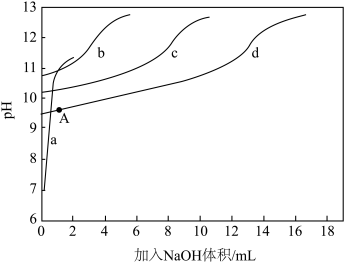
| 溶液组号 | 组成 | 体积/mL |
| 1 | 0.2mol·L-1NaCl溶液 | 15 |
| 2 | 0.1mol·L-1NH4Cl | 3 |
| 0.1mol·L-1氨水 | 12 | |
| 3 | 0.1mol·L-1NH4Cl | 7.5 |
| 0.1mol·L-1氨水 | 7.5 | |
| 4 | 0.1mol·L-1NH4Cl | 12 |
| 0.1mol·L-1氨水 | 3 |
②实验结果显示,当[c(
 )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=
您最近半年使用:0次
5 . 缓冲溶液是指加少量水稀释或外加少量酸、碱,自身pH不发生显著变化的溶液。1L含1mol乳酸(HLac)和1mol乳酸钠(NaLac)的溶液就是一种缓冲溶液,该溶液的pH为3.85。下图是此缓冲溶液的pH随通入HCl(g)或加入NaOH(s)的物质的量变化的示意图(溶液体积保持1L),已知lg3=0.48。下列说法错误的是
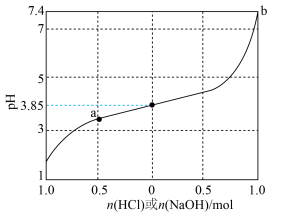
A.此缓冲溶液中(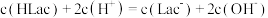 |
| B.通过计算可得出,a点溶液的pH约为3.37 |
| C.根据图像可以判断,b点溶液已失去缓冲能力 |
D.当加入NaOH,且横坐标为0.5时,对应溶液中(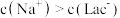 |
您最近半年使用:0次
解题方法
6 . 肼为二元弱碱,在水中的电离方式与氨相似。常温下,向一定浓度肼 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为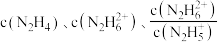 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是
 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为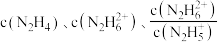 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是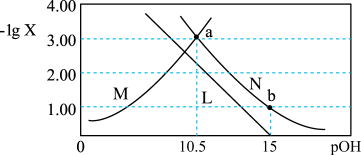
A.曲线N表示 与 与 的变化关系 的变化关系 |
B.常温下,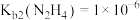 |
C.a点溶液中: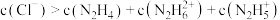 |
D.b点溶液中: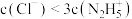 |
您最近半年使用:0次
7 . 常温下,向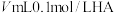 溶液中滴入
溶液中滴入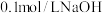 溶液,溶液中由水电离出的氢氧根离子浓度的负对数
溶液,溶液中由水电离出的氢氧根离子浓度的负对数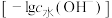 与所加
与所加 溶液体积的关系如图所示。下列说法错误的是
溶液体积的关系如图所示。下列说法错误的是
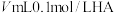 溶液中滴入
溶液中滴入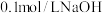 溶液,溶液中由水电离出的氢氧根离子浓度的负对数
溶液,溶液中由水电离出的氢氧根离子浓度的负对数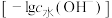 与所加
与所加 溶液体积的关系如图所示。下列说法错误的是
溶液体积的关系如图所示。下列说法错误的是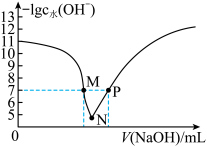
A.常温下,水解常数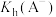 约为 约为 |
| B.M点、P点所对应的溶液均显中性 |
C.N点溶液中存在: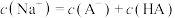 |
D.N点溶液中存在: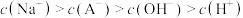 |
您最近半年使用:0次
8 . 二元有机酸(H2X)的电离常数Kal=1.67×10﹣8、Ka2=3.34×10﹣17。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中c2(H+)与c2(Ba2+)的关系如图所示。下列说法不正确的是
已知:HY是一元强酸,BaY2易溶于水。0.382=0.1444,0.192=0.0361
已知:HY是一元强酸,BaY2易溶于水。0.382=0.1444,0.192=0.0361

| A.NaHX溶液显碱性 |
| B.溶度积Ksp(BaX)=6.18×10﹣23mol2⋅L﹣2 |
| C.b点:2c(Ba2+)+c(H+)=2c(X2﹣)+c(HX﹣)+c(OH﹣) |
| D.若0.1 mol BaX溶于25 mLx mol⋅L﹣1HY溶液中得到c点溶液,则x≈8.38 |
您最近半年使用:0次
解题方法
9 . Na2CO3溶液中各离子浓度关系正确的选项有
A.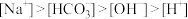 | B. |
C.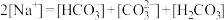 | D. |
您最近半年使用:0次
10 . 肼在水溶液中为二元弱碱,在水中的电离方式与氨相似。常温下,向0.1mol·L-1肼溶液中,滴加稀盐酸调节pH。溶液中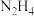 、
、 、
、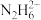 占含氮物种的物质的量分数为
占含氮物种的物质的量分数为 (如
(如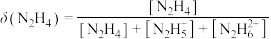 ),
), 随溶液pH变化的曲线如下图所示:
随溶液pH变化的曲线如下图所示:
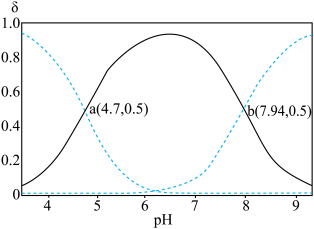
(1)常温下中性溶液中,各含氮物种的浓度大小关系为______________。
(2)室温时,反应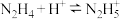 平衡常数K的数值为_____________。
平衡常数K的数值为_____________。
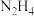 、
、 、
、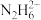 占含氮物种的物质的量分数为
占含氮物种的物质的量分数为 (如
(如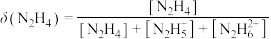 ),
), 随溶液pH变化的曲线如下图所示:
随溶液pH变化的曲线如下图所示:
(1)常温下中性溶液中,各含氮物种的浓度大小关系为______________。
A.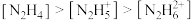 | B.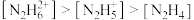 |
C.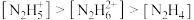 | D.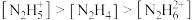 |
(2)室温时,反应
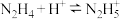 平衡常数K的数值为_____________。
平衡常数K的数值为_____________。A.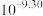 | B.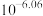 | C. | D. |
您最近半年使用:0次



