1 . 回答下列问题。
(1)根据所学知识回答下列问题:
(1)已知:①N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.0kJ·mol-1;
②H2(g)+ O2(g)=H2O(g) ΔH=-240.0kJ·mol-1;
O2(g)=H2O(g) ΔH=-240.0kJ·mol-1;
③2Fe(s)+ O2(g)=Fe2O3(s) ΔH=-1644.0kJ·mol-1
O2(g)=Fe2O3(s) ΔH=-1644.0kJ·mol-1
则反应2NH3(g)+Fe2O3(s)=N2(g)+3H2O(g)+2Fe(s) ΔH=___________ kJ·mol-1.
(2)反应NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49kJ·mol-1自发进行的条件是___________ (填“高温”或“低温”)。
(3)工业上以含SO2的废气为原料,用电化学的方法制取硫酸的装置图如下:___________ 。
(4)常温下,pH=3的醋酸溶液中,由水电离产生的
___________ mol∙L−1.
(5)pH=2的CH3COOH和pH=12的NaOH溶液等体积混合后溶液呈___________ (填“酸性”“碱性”或“中性”)
(6)KAl(SO4)2‧12H2O可用作净水剂,其原理是___________ (用离子方程式说明)。
(7)已知常温下,Ka(HCN)=6.2×10-10。常温下,含等物质的量浓度的HCN与NaCN的混合溶液显___________ (填“酸”“碱”或“中”)性。
(8)某 溶液中含有
溶液中含有 杂质,溶液中
杂质,溶液中 的浓度为0.020mol∙L−1,通常认为残留在溶液中的离子浓度小于
的浓度为0.020mol∙L−1,通常认为残留在溶液中的离子浓度小于 时即沉淀完全(注:lg5=0.7),已知
时即沉淀完全(注:lg5=0.7),已知 ,
,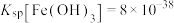 ,若将该溶液的pH调至4.0,
,若将该溶液的pH调至4.0,___________ (填“是”或“否”)可以达到除去 杂质而不损失
杂质而不损失 的目的。
的目的。
(1)根据所学知识回答下列问题:
(1)已知:①N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.0kJ·mol-1;
②H2(g)+
 O2(g)=H2O(g) ΔH=-240.0kJ·mol-1;
O2(g)=H2O(g) ΔH=-240.0kJ·mol-1;③2Fe(s)+
 O2(g)=Fe2O3(s) ΔH=-1644.0kJ·mol-1
O2(g)=Fe2O3(s) ΔH=-1644.0kJ·mol-1则反应2NH3(g)+Fe2O3(s)=N2(g)+3H2O(g)+2Fe(s) ΔH=
(2)反应NH2COONH4(s)⇌CO(NH2)2(s)+H2O(g) ΔH2=+72.49kJ·mol-1自发进行的条件是
(3)工业上以含SO2的废气为原料,用电化学的方法制取硫酸的装置图如下:
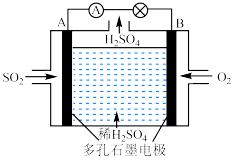
(4)常温下,pH=3的醋酸溶液中,由水电离产生的

(5)pH=2的CH3COOH和pH=12的NaOH溶液等体积混合后溶液呈
(6)KAl(SO4)2‧12H2O可用作净水剂,其原理是
(7)已知常温下,Ka(HCN)=6.2×10-10。常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
(8)某
 溶液中含有
溶液中含有 杂质,溶液中
杂质,溶液中 的浓度为0.020mol∙L−1,通常认为残留在溶液中的离子浓度小于
的浓度为0.020mol∙L−1,通常认为残留在溶液中的离子浓度小于 时即沉淀完全(注:lg5=0.7),已知
时即沉淀完全(注:lg5=0.7),已知 ,
,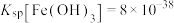 ,若将该溶液的pH调至4.0,
,若将该溶液的pH调至4.0, 杂质而不损失
杂质而不损失 的目的。
的目的。
您最近半年使用:0次
2 . 已知常温下溶液中CH3COOH和CH3COO-的物质的量分数与pH的关系如图所示。下列说法正确的是
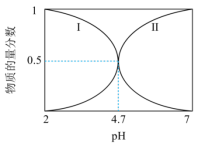
| A.图中曲线I表示的是CH3COO- |
| B.常温下,Ka(CH3COOH)=1×10-4.7 |
| C.0.1mol•L-1CH3COONa溶液中存在等式:c(Na+)+c(CH3COO-)=0.2mol•L-1 |
| D.常温下,浓度均为0.1mol•L-1的CH3COOH和CH3COONa混合溶液中:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
您最近半年使用:0次
3 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

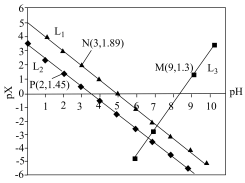
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的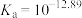 |
C.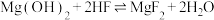 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近半年使用:0次
名校
4 . 常温下,用NaOH溶液滴定H2C2O4溶液,溶液中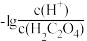 [或
[或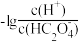 和
和 [或
[或 ]的关系如图所示,下列说法错误的是
]的关系如图所示,下列说法错误的是
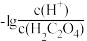 [或
[或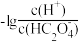 和
和 [或
[或 ]的关系如图所示,下列说法错误的是
]的关系如图所示,下列说法错误的是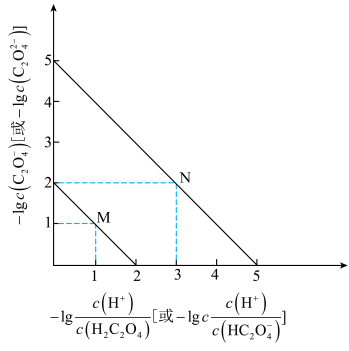
A.直线M表示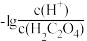 和 和 的关系 的关系 |
B.滴定过程中,当pH=5时,c(Na+)-3c( )<0 )<0 |
C.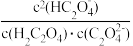 随pH的升高而减小 随pH的升高而减小 |
D.NaHC2O4溶液中,c(Na+)> c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近半年使用:0次
名校
5 . 已知H2A为二元弱酸,Ka1(H2A)=1.0×10 3,常温下向Na2A溶液中逐惭加入一元弱酸HB溶液,溶液离子浓度变化关系如图所示。下列说法正确的是
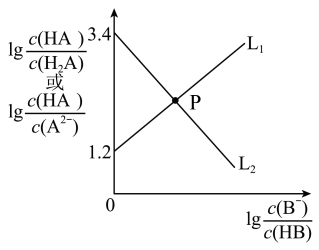
| A.K(HB)=10 2.8 |
| B.NaHA溶液呈碱性 |
| C.交点P对应溶液存在: c(H+)+c(A2-)+c(HA-)=c(B-)+c(OH-) |
| D.Na2A溶液中滴入足量HB溶液的离子方程式为A2-+HB=HA-+B- |
您最近半年使用:0次
6 . 草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX[X表示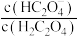 或
或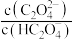 ]随pH的变化关系如图所示。下列说法不正确的是
]随pH的变化关系如图所示。下列说法不正确的是

A.Ⅰ中X表示的是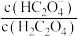 |
B.当溶液pH=4.19时,c(Na+)>3c( ) ) |
C.已知:25℃时,NH3∙H2O的电离常数为 ,则(NH4)2C2O4溶液呈酸性 ,则(NH4)2C2O4溶液呈酸性 |
D.0.1mol∙L-1NaHC2O4溶液中:c(Na+)>c( )>c( )>c( )>c(H2C2O4) )>c(H2C2O4) |
您最近半年使用:0次
解题方法
7 . 室温下,向浓度均为 的
的 和
和 混合溶液
混合溶液 中滴加
中滴加 标准盐酸,溶液
标准盐酸,溶液 与
与 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是
 的
的 和
和 混合溶液
混合溶液 中滴加
中滴加 标准盐酸,溶液
标准盐酸,溶液 与
与 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是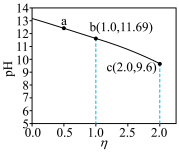
A.水的电离程度: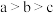 |
B.常温下, 的水解常数 的水解常数 约为 约为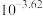 |
C.c点溶液中: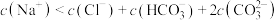 |
D.b点溶液中: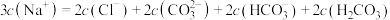 |
您最近半年使用:0次
名校
8 . 25℃时,向 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸
的盐酸 ,或向
,或向 的
的 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液
溶液 (无气体逸出),溶液的pH与
(无气体逸出),溶液的pH与 [
[ 或
或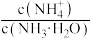 ]的关系如图所示。
]的关系如图所示。不正确 的是
 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸
的盐酸 ,或向
,或向 的
的 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液
溶液 (无气体逸出),溶液的pH与
(无气体逸出),溶液的pH与 [
[ 或
或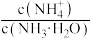 ]的关系如图所示。
]的关系如图所示。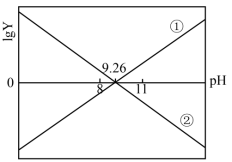
A.曲线①中的 |
B.当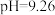 时,恒有关系: 时,恒有关系: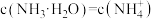 |
C.当 时,两溶液pH均大于9.26 时,两溶液pH均大于9.26 |
D.25℃时, 的 的 溶液的pH约为4.63 溶液的pH约为4.63 |
您最近半年使用:0次
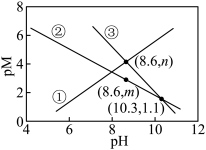
9 . 萍乡孽龙洞属于天然溶洞,它的形成与岩石中的CaCO3和空气中CO2溶于天然水体形成的含碳物种的浓度有密切关系。常温下,某溶洞水体中pM随pH的变化关系如图所示。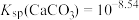 ,
, ,M为
,M为 、
、 或Ca2+]下列说法正确的是
或Ca2+]下列说法正确的是
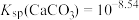 ,
, ,M为
,M为 、
、 或Ca2+]下列说法正确的是
或Ca2+]下列说法正确的是A.曲线①代表 与pH的关系 与pH的关系 |
| B.m=2.57 |
C. 的数量级为 的数量级为 |
D.pH由4到8的过程中 增大的比 增大的比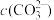 快 快 |
您最近半年使用:0次
解题方法
10 . 常温下,将 溶液滴入三元酸
溶液滴入三元酸 溶液中,混合溶液中
溶液中,混合溶液中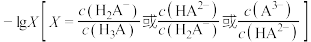 随
随 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
 溶液滴入三元酸
溶液滴入三元酸 溶液中,混合溶液中
溶液中,混合溶液中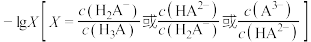 随
随 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
A.曲线 表示 表示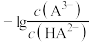 随 随 的变化关系 的变化关系 |
B.当 时,混合溶液中 时,混合溶液中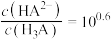 |
C.常温下,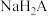 溶液中: 溶液中: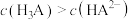 |
D.当 时, 时, |
您最近半年使用:0次



