解题方法
1 . 按要求写出下列离子方程式
(1)(NH4)2SO4水解:_______ 。
(2)NaHCO3水解:_______ 。
(3)Ag2CrO4沉淀溶解平衡:_______ 。
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+ O2=H2O。则负极反应式:
O2=H2O。则负极反应式:_______ 、正极反应式_______ 。
(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:_______ 。
②简要说明白色固体转化为黑色固体的原因:_______ 。
(1)(NH4)2SO4水解:
(2)NaHCO3水解:
(3)Ag2CrO4沉淀溶解平衡:
(4)氢氧燃料电池(酸性):已知总电极反应式为H2+
 O2=H2O。则负极反应式:
O2=H2O。则负极反应式:(5)已知AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。向AgCl和水形成的悬浊液中加入足量的Na2S溶液并振荡,结果白色固体完全转化为黑色固体:
①写出白色固体转化为黑色固体的化学方程式:
②简要说明白色固体转化为黑色固体的原因:
您最近半年使用:0次
2 . 平衡有多种类型,如化学平衡、溶解平衡、电离平衡。下列不存在平衡的是(不考虑水的电离平衡)
| A.稀醋酸溶液中 | B.氯化银悬浊液中 |
| C.氮气与氢气反应的混合物中 | D.稀氯化钠水溶液中 |
您最近半年使用:0次
3 . 氯化银沉淀的溶解度为零。( )
您最近半年使用:0次
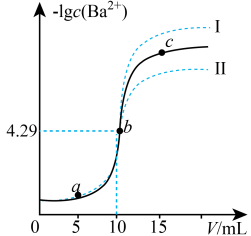
4 . 25℃时,向10mL0.10mol/LBaCl2溶液中滴加0.10mol/LNa2SO3溶液,滴加过程中溶液中-lgc(Ba2+)与Na2SO3溶液体积(V)的关系如图所示;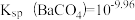 ,下列说法不正确的是
,下列说法不正确的是
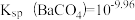 ,下列说法不正确的是
,下列说法不正确的是
| A.Ksp(BaCO3)=10-8.58 |
B.NH4HA溶液中: |
| C.若改用0.20mol/LNa2SO3溶液来滴定,则恰好反应点由b移至a |
| D.若把Na2SO3溶液换成等浓度Na2SO4溶液,则曲线变为I |
您最近半年使用:0次
名校
5 . 用数字传感器探究AgCl的沉淀溶解平衡。实验测得悬浊液中溶解的氯化物浓度变化如图所示,其中a点表示AgCl溶于KNO3溶液形成的悬浊液,下列说法正确的是
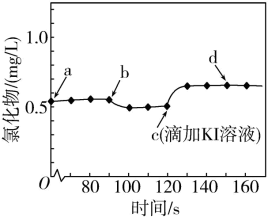
| A.b点可能加入了KCl溶液 |
| B.d点c(Ag+)<c(Cl-) |
| C.c点后无黄色沉淀生成 |
| D.由图无法得知:Ksp(AgI)<Ksp(AgCl) |
您最近半年使用:0次
名校
解题方法
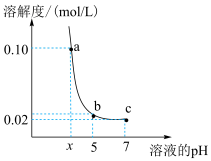
6 . 常温下,利用硝酸调节溶液的 ,实验测得醋酸银的溶解度
,实验测得醋酸银的溶解度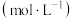 随着
随着 的变化曲线如图所示.已知:常温下,
的变化曲线如图所示.已知:常温下, ,在酸性条件下忽略
,在酸性条件下忽略 的水解.下列说法错误的是
的水解.下列说法错误的是
 ,实验测得醋酸银的溶解度
,实验测得醋酸银的溶解度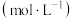 随着
随着 的变化曲线如图所示.已知:常温下,
的变化曲线如图所示.已知:常温下, ,在酸性条件下忽略
,在酸性条件下忽略 的水解.下列说法错误的是
的水解.下列说法错误的是
A.x的取值范围: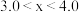 |
B.b点的溶液中存在: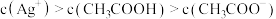 |
C.c点溶液中: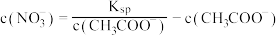 |
D.随着酸性的增强, 会结合 会结合 ,使醋酸银的沉淀溶解平衡正向移动 ,使醋酸银的沉淀溶解平衡正向移动 |
您最近半年使用:0次
2024-03-18更新
|
176次组卷
|
3卷引用:河北省保定市部分高中2023-2024学年高三下学期开学化学试题
名校
7 . 下列方程式书写正确的是
A.NaHSO4在水溶液中的电离方程式:NaHSO4=Na++HSO |
B.H2SO3的电离方程式:H2SO3 2H++SO 2H++SO |
C.CaCO3的电离方程式:CaCO3=Ca2++CO |
D.CaCO3沉淀溶解平衡方程式:CaCO3=2Na2+ + CO |
您最近半年使用:0次
名校
8 . 已知相同温度下,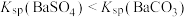 。某温度下,饱和溶液中
。某温度下,饱和溶液中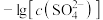 、
、 与
与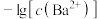 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
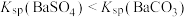 。某温度下,饱和溶液中
。某温度下,饱和溶液中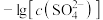 、
、 与
与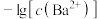 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是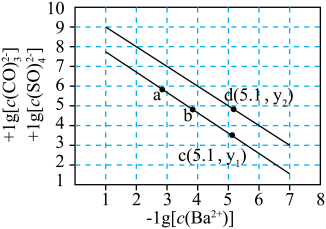
A.线②代表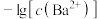 与 与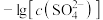 的关系 的关系 |
B.该温度下 的 的 值为 值为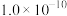 |
C.加适量 固体可使溶液由 固体可使溶液由 点变到 点变到 点 点 |
D.当 时,则两溶液中 时,则两溶液中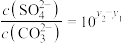 |
您最近半年使用:0次
2024-02-17更新
|
68次组卷
|
2卷引用:河北省百师联盟2023-2024学年高二上学期1月期末大联考化学试题
解题方法
9 . 下列化学用语正确的是
A.硫酸氢钠溶液的电离方程式: |
B.硫酸钡的溶解平衡: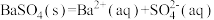 |
C.NH4Cl溶于D2O中的水解平衡: |
D.氢氟酸的电离方程式: |
您最近半年使用:0次
名校
解题方法
10 . 化学在生产、生活、实验中有着重要的应用,下列说法正确的是。
A.燃煤中加入 可以减少酸雨的形成及温室气体的排放 可以减少酸雨的形成及温室气体的排放 |
B.利用 合成了脂肪酸:实现了无机小分子向有机高分子的转变 合成了脂肪酸:实现了无机小分子向有机高分子的转变 |
| C.碳酸钡可用于胃肠X射线造影检查 |
| D.配制氯化铁溶液时,将氯化铁固体溶解在较浓的盐酸中再加水稀释 |
您最近半年使用:0次



