2024高三下·全国·专题练习
解题方法
1 . 工业上利用软锰矿(主要成分为 ,含
,含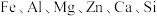 等元素)与纤维素制备
等元素)与纤维素制备 ,工艺如下图所示。
,工艺如下图所示。 范围如下:
范围如下:
“中和”步骤要调节溶液 ,最适宜的
,最适宜的 范围是
范围是_____ 。
(2)“氧化”时,氧化时间对产品中的锰含量及溶液pH的影响如下图。最佳的氧化时间为_____  ;下列说法错误的是
;下列说法错误的是_____ 。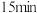 ,主要发生的反应是
,主要发生的反应是 下降较慢
下降较慢
B.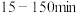 ,主要发生的反应是
,主要发生的反应是 ,
, 下降较快
下降较快
C.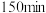 之后,
之后, 趋于稳定,则
趋于稳定,则 已完全氧化
已完全氧化
D. 后,继续通入空气,可能将产品氧化生成
后,继续通入空气,可能将产品氧化生成 及
及 ,使产品中锰含量下降
,使产品中锰含量下降
 ,含
,含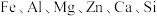 等元素)与纤维素制备
等元素)与纤维素制备 ,工艺如下图所示。
,工艺如下图所示。
 范围如下:
范围如下:| 金属离子 |  |  |  |  |  |
开始沉淀的 | 1.5 | 3.0 | 8.9 | 6.0 | 8.1 |
完全沉淀的 | 2.8 | 4.7 | 10.9 | 8.0 | 10.1 |
 ,最适宜的
,最适宜的 范围是
范围是(2)“氧化”时,氧化时间对产品中的锰含量及溶液pH的影响如下图。最佳的氧化时间为
 ;下列说法错误的是
;下列说法错误的是
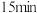 ,主要发生的反应是
,主要发生的反应是 下降较慢
下降较慢B.
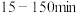 ,主要发生的反应是
,主要发生的反应是 ,
, 下降较快
下降较快C.
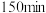 之后,
之后, 趋于稳定,则
趋于稳定,则 已完全氧化
已完全氧化D.
 后,继续通入空气,可能将产品氧化生成
后,继续通入空气,可能将产品氧化生成 及
及 ,使产品中锰含量下降
,使产品中锰含量下降
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 一种由菱镁矿(主要成分 ,还含少量
,还含少量 和
和 )制备高纯
)制备高纯 的工艺流程如下:
的工艺流程如下:
(1)“浸取”时加入的盐酸不宜过量太多的原因是___________ 。
(2)“调pH”时,发生反应的离子方程式为___________ 。某同学认为“氧化”步骤可省略,直接用 调节pH值得到
调节pH值得到 沉淀,该想法不合理的原因是
沉淀,该想法不合理的原因是___________ 。
 ,还含少量
,还含少量 和
和 )制备高纯
)制备高纯 的工艺流程如下:
的工艺流程如下:
| 金属离子 |  |  |  |
| 开始沉淀的pH | 7.6 | 1.9 | 8.4 |
| 沉淀完全的pH | 9.6 | 3.2 | 10.8 |
(2)“调pH”时,发生反应的离子方程式为
 调节pH值得到
调节pH值得到 沉淀,该想法不合理的原因是
沉淀,该想法不合理的原因是
您最近半年使用:0次
3 . 过氧化钙( CaO2)是一种白色晶体粉末,极微溶于水,不溶于醇类、乙醚等,105℃左右干燥即得白色或淡黄色粉末CaO2,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2,易与酸反应生成H2O2。
CaO2)是一种白色晶体粉末,极微溶于水,不溶于醇类、乙醚等,105℃左右干燥即得白色或淡黄色粉末CaO2,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2,易与酸反应生成H2O2。

您最近半年使用:0次
解题方法
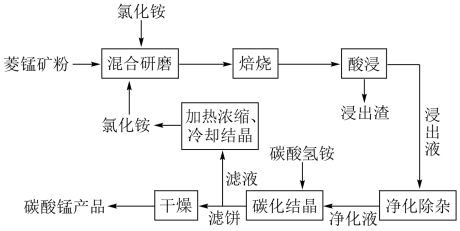
4 . 工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示: 其余为
其余为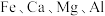 等元素。
等元素。
②部分阳离子沉淀时溶液的 :
:
③“焙烧”过程中主要反应为 。
。
(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、 分别为
分别为___________ 、___________ 、___________ 。 ,作用是
,作用是___________ ,再调节溶液 的范围为
的范围为___________ ,将 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将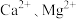 变为氟化物沉淀除去。
变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为___________ 。
(4)上述流程中可循环使用的物质是___________ (填化学式)。
(5)现用滴定法测定产品中锰的含量。实验步骤:称取 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应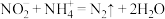 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用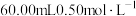 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为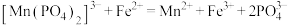 ;用
;用 酸性
酸性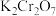 溶液恰好除去过量的
溶液恰好除去过量的 。
。
①酸性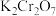 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
②试样中锰的质量分数为___________ 。
 其余为
其余为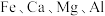 等元素。
等元素。②部分阳离子沉淀时溶液的
 :
:| 离子 |  |  |  |  |  |
开始沉淀的 | 4.1 | 2.2 | 10.6 | 8.1 | 9.1 |
沉淀完全的 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
 。
。(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、
 分别为
分别为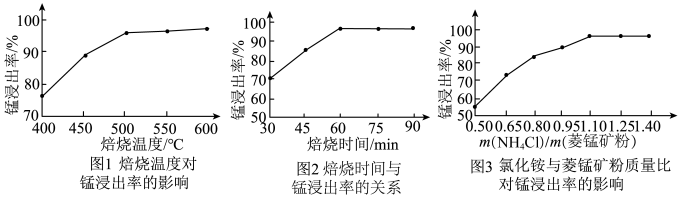
 ,作用是
,作用是 的范围为
的范围为 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将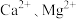 变为氟化物沉淀除去。
变为氟化物沉淀除去。(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为
(4)上述流程中可循环使用的物质是
(5)现用滴定法测定产品中锰的含量。实验步骤:称取
 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应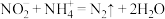 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用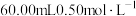 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为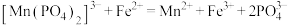 ;用
;用 酸性
酸性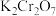 溶液恰好除去过量的
溶液恰好除去过量的 。
。①酸性
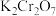 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为②试样中锰的质量分数为
您最近半年使用:0次
5 . 我国是世界上稀土资源最丰富的国家,冶炼提纯技术位于世界前茅。从某种磷精矿(主要成分为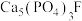 ,含少量
,含少量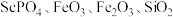 )分离稀土元素钪(
)分离稀土元素钪( )的工业流程如下:
)的工业流程如下:_______ 。
(2)“萃取”的目的是富集 ,但其余元素也会按一定比例进入萃取剂中。
,但其余元素也会按一定比例进入萃取剂中。
①通过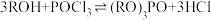 制得有机磷萃取剂
制得有机磷萃取剂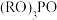 ,其中
,其中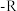 代表烃基,
代表烃基,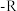 对
对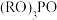 产率的影响如下表。
产率的影响如下表。
由表可知:随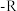 中碳原子数增加,
中碳原子数增加,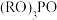 产率降低,请从结构的角度分析原因
产率降低,请从结构的角度分析原因_______ 。
②“反萃取”的目的是分离 和
和 元素。向“萃取液”中通入
元素。向“萃取液”中通入 ,
,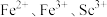 的沉淀率随
的沉淀率随 的变化如图。试剂X为
的变化如图。试剂X为_______ (填“ ”或“
”或“ ”),应调节
”),应调节 为
为_______ 。 得到
得到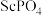 沉淀的过程为:
沉淀的过程为:
i.
ii._______ (写出该过程的化学方程式)。
(3)草酸钪晶体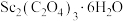 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。250℃晶体主要成分是
随温度的变化情况如图所示。250℃晶体主要成分是_______ (填化学式),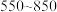 ℃反应的化学方程式为
℃反应的化学方程式为_______ 。 的一种氢化物晶胞结构如图,晶体中H周围与其最近的
的一种氢化物晶胞结构如图,晶体中H周围与其最近的 的个数为
的个数为_______ 。 为阿伏伽德罗常数的值,晶胞参数为
为阿伏伽德罗常数的值,晶胞参数为 ,则该晶胞的密度为
,则该晶胞的密度为_______  。
。
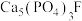 ,含少量
,含少量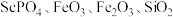 )分离稀土元素钪(
)分离稀土元素钪( )的工业流程如下:
)的工业流程如下: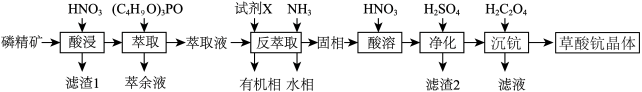
(2)“萃取”的目的是富集
 ,但其余元素也会按一定比例进入萃取剂中。
,但其余元素也会按一定比例进入萃取剂中。①通过
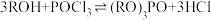 制得有机磷萃取剂
制得有机磷萃取剂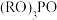 ,其中
,其中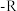 代表烃基,
代表烃基,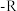 对
对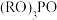 产率的影响如下表。
产率的影响如下表。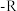 | 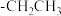 | 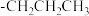 | 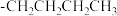 |
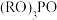 产率/ 产率/ | 82 | 62 | 20 |
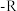 中碳原子数增加,
中碳原子数增加,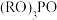 产率降低,请从结构的角度分析原因
产率降低,请从结构的角度分析原因②“反萃取”的目的是分离
 和
和 元素。向“萃取液”中通入
元素。向“萃取液”中通入 ,
, 的沉淀率随
的沉淀率随 的变化如图。试剂X为
的变化如图。试剂X为 ”或“
”或“ ”),应调节
”),应调节 为
为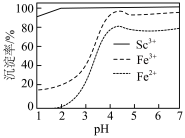
 得到
得到 沉淀的过程为:
沉淀的过程为:i.

ii.
(3)草酸钪晶体
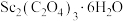 在空气中加热,
在空气中加热, 随温度的变化情况如图所示。250℃晶体主要成分是
随温度的变化情况如图所示。250℃晶体主要成分是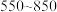 ℃反应的化学方程式为
℃反应的化学方程式为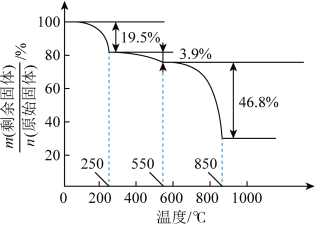
 的一种氢化物晶胞结构如图,晶体中H周围与其最近的
的一种氢化物晶胞结构如图,晶体中H周围与其最近的 的个数为
的个数为 为阿伏伽德罗常数的值,晶胞参数为
为阿伏伽德罗常数的值,晶胞参数为 ,则该晶胞的密度为
,则该晶胞的密度为 。
。
您最近半年使用:0次
6 . 已知相同温度下,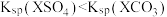 。某温度下,
。某温度下,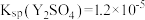 ,相应物质饱和溶液中
,相应物质饱和溶液中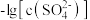 、
、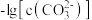 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
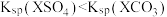 。某温度下,
。某温度下,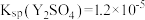 ,相应物质饱和溶液中
,相应物质饱和溶液中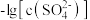 、
、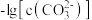 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是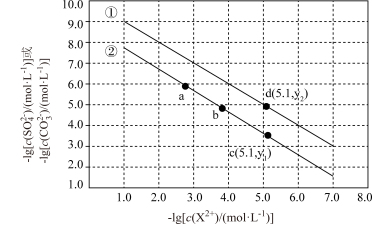
A.该温度下: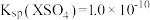 |
B.曲线①中 |
C.加适量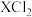 固体(易溶于水)可使溶液由c点变到b点 固体(易溶于水)可使溶液由c点变到b点 |
D.该温度下,向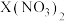 、 、 均为 均为 的混合溶液中滴加 的混合溶液中滴加 溶液,先生成 溶液,先生成 沉淀 沉淀 |
您最近半年使用:0次
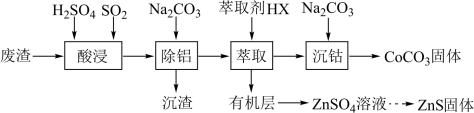
7 . CoCO3可用作选矿剂、催化剂及涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
(1)“酸浸”时需控制温度在40℃左右,原因是___________ 。
(2)“除铝”时发生反应的离子方程式为___________ 。
(3)上述“萃取”过程可表示为 。
。
①下列说法不正确的是___________ 。
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。___________
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因___________ 。
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有___________ 。
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为___________ 。
(1)“酸浸”时需控制温度在40℃左右,原因是
(2)“除铝”时发生反应的离子方程式为
(3)上述“萃取”过程可表示为
 。
。①下列说法不正确的是
A.可将废渣粉碎以提高酸浸效率
B.“除铝”时,应加入过量的Na2CO3溶液
C.可选择CCl4作为萃取剂
D.往萃取后的有机层中加水可获得ZnSO4溶液
②若萃取操作是在实验室完成,请选择合适的编号,按正确的操作顺序(有的操作可重复使用),完成萃取实验(假设只放气一次)。
倒入溶液和萃取剂→___________→___________→___________→___________→f→___________→___________→使下层液体慢慢流出→c→上层液体从上口倒出
a.打开分液漏斗上口玻璃塞;b.塞上分液漏斗上口玻璃塞;c.关闭分液漏斗旋塞;
d打开分液漏斗旋塞;e.倒转分液漏斗振摇;
f.将分液漏斗放在铁圈上静置;g.手持分液漏斗静置。
(4)“沉钴”时,溶液滴加过快会导致产品不纯,请解释可能原因
(5)该工艺的副产物ZnS可参与H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该过程中涉及到的化学反应有
(6)在空气中煅烧CoCO3生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴氧化物的化学式为
您最近半年使用:0次
8 . 实验室安全至关重要。下列做法错误的是
| A.取用液溴时,需带手套和护目镜,在通风橱中进行 |
| B.误食钡盐,可通过服用纯碱溶液解毒 |
| C.电器、有机物等起火,用二氧化碳灭火器灭火 |
| D.皮肤被钠灼烧,用乙醇洗、水洗,最后涂上烫伤膏 |
您最近半年使用:0次
9 . 下列实验操作及现象所对应的结论或解释正确的是
| 选项 | 实验操作及现象 | 结论或解释 |
| A | 将某铁的氧化物溶于足量浓盐酸,再向其中加入少量酸性 溶液, 溶液, 溶液褪色 溶液褪色 | 铁的氧化物中含有二价铁 |
| B | 向 与稀硫酸反应的体系中加入几滴硫酸铜溶液,产生气泡速率变快 与稀硫酸反应的体系中加入几滴硫酸铜溶液,产生气泡速率变快 | 硫酸铜具有催化作用 |
| C | 向盛有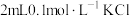 溶液的试管中滴加2滴 溶液的试管中滴加2滴  溶液,产生白色沉淀,再滴加4滴 溶液,产生白色沉淀,再滴加4滴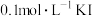 溶液,沉淀转变为黄色 溶液,沉淀转变为黄色 | 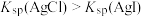 |
| D | 向 溶液中通入 溶液中通入 气体,产生黑色沉淀 气体,产生黑色沉淀 | 酸性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 宏观辨识与微观探析是化学学科核心素养之一。下列反应的离子方程式书写正确的是
A.将NH3通入稀硝酸中: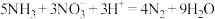 |
B.向FeCl3溶液中加入KSCN溶液: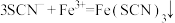 |
C.将Na2SO3溶液与酸性高锰酸钾溶液混合: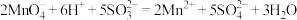 |
D.Mg(OH)2溶于NH4Cl溶液中: |
您最近半年使用:0次



