1 . 某研究性学习小组用如图所示的装置进行实验,探究原电池、电解池和电解精炼钴的工作原理。一段时间后装置甲的两极均有气体产生,且X极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。请根据实验现象及所查资料,回答下列问题:
查阅资料:高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
(2)装置丙中,若外电路中有0.2 mol电子转移,则有___________ mol  透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:___________ 。
(3)反应过程中,X极处发生的电极反应为 和
和___________ 。
(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为___________ mL(均已折算为标准状况时的气体体积)。
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中
___________ (填“变大”“变小”或“不变”),该电解池总反应的化学方程式是___________ 。
(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有___________ 。
查阅资料:高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
| A.X(Fe) | B.Y(C) | C.Co | D.Zn |
(2)装置丙中,若外电路中有0.2 mol电子转移,则有
 透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:(3)反应过程中,X极处发生的电极反应为
 和
和(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中

(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有
您最近一年使用:0次
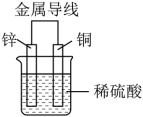
2 . 如图为Zn-Cu原电池的示意图,请回答:_______ 极,铜片为原电池的_______ 极 (填“正”或“负”) 。
(2)锌电极反应式是_______ ,属于_______ 反应(填“氧化”或“还原”);铜电极反应式是_______ ,属于_______ 反应(同上)。
(3)若锌片减轻0.1mol,则另一极放出气体的物质的量为_______ mol。
(2)锌电极反应式是
(3)若锌片减轻0.1mol,则另一极放出气体的物质的量为
您最近一年使用:0次
解题方法
3 . 利用光电化学方法将乙二醇( )转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
)转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
 )转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是
)转化为甲酸盐,同时产生绿色氢气。该装置以NaOH溶液为电解质溶液,工作原理示意图如图所示。已知:实验测定,实际上电路通过0.4mol电子时生成6.8gHCOONa;电解过程中的法拉第效率等于实际甲酸盐量与理论量之比。下列叙述正确的是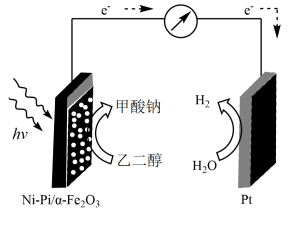
A. 极发生还原反应 极发生还原反应 |
B.装置工作时, 向Pt极迁移 向Pt极迁移 |
C.Pt极反应式为 |
| D.生成HCOONa的法拉第效率为75% |
您最近一年使用:0次
解题方法
4 . 一种电池装置如图所示,它能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。下列说法不正确 的是
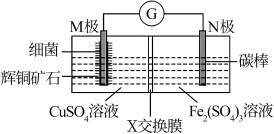
| A.N极为正极 |
| B.X交换膜为阴离子交换膜 |
C.M极产生的Cu2+和SO 的物质的量之比为2:1 的物质的量之比为2:1 |
| D.外电路上每通过2mol电子,左室溶液增重32g |
您最近一年使用:0次
5 . 由辉铜矿石(主要成分是Cu2S)制CuSO4的工作原理如图所示。下列说法不正确的是
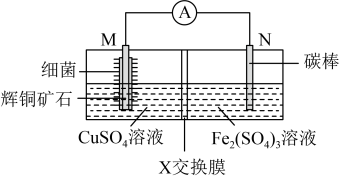

| A.N极为正极 |
| B.X交换膜为阴离子交换膜 |
C.M极上的电极反应式为:Cu2S+10e-+4H2O=2Cu2++8H++ |
| D.该电池工作时在某一温度范围内反应速率最快 |
您最近一年使用:0次
2024-04-10更新
|
134次组卷
|
2卷引用:重庆市鲁能巴蜀中学校2023-2024学年高二上学期1月期末化学试题
6 . 某化学实验探究小组探究MnO2与某些盐溶液的反应,设计如图装置。左烧杯中加入50mL6mol·L-1硫酸,右烧杯中加入50mL6mol·L-1CaCl2溶液,盐桥选择氯化钾琼脂。当闭合开关K时,电流表中出现指针偏转,下列说法正确的是
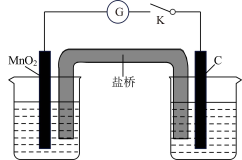
| A.该实验装置属于电解池 |
| B.左侧烧杯中的电极反应为MnO2+4H++2e-=Mn2++2H2O |
| C.右侧C电极上发生还原反应,产生的气体可使湿润的碘化钾淀粉试纸变蓝 |
| D.若将盐桥中氯化钾琼脂换成KNO3琼脂,则C电极上产生的气体的总量增加 |
您最近一年使用:0次
2024-04-08更新
|
89次组卷
|
2卷引用:云南省大理州实验中学2021-2022学年高二上学期化学期末考试题
7 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
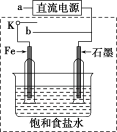
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
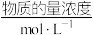 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
8 . 电解苯酚的乙腈(CH3CN)水溶液可在电极上直接合成扑热息痛(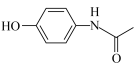 ),电极材料均为石墨。下列说法错误的是
),电极材料均为石墨。下列说法错误的是

| A.电极d为阴极 |
| B.装置工作时,乙室溶液pH增大 |
C.电极c的电极反应式为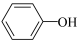 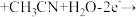 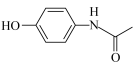 +2H+ +2H+ |
| D.合成1mol扑热息痛,理论上甲室质量增重96g |
您最近一年使用:0次
2024-03-15更新
|
487次组卷
|
5卷引用:湖南省益阳市第一中学2023-2024学年高二下学期期末考试化学试题
解题方法
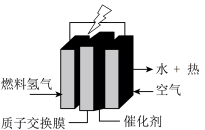
9 . 欧洲足球锦标赛事中的拍摄车,装着“绿色心脏”-质子交换膜燃料电池,其工作原理如图所示。下列叙述中正确的是

| A.装置中的能量变化为电能转化为化学能 |
| B.通入氢气的电极发生还原反应 |
| C.通入空气的电极反应式:O2+4e-+ 4H+=2H2O |
| D.装置中电子从通入空气的电极经过导线流向通入氢气的电极 |
您最近一年使用:0次
名校
10 . 肼 暴露在空气中容易爆炸,但是以其为燃料的电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示,下列叙述正确的是
暴露在空气中容易爆炸,但是以其为燃料的电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示,下列叙述正确的是
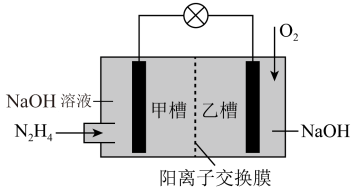
A.电池工作时,正极附近的  减小 减小 |
B.当消耗  时,有 时,有 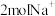 由甲槽向乙槽迁移 由甲槽向乙槽迁移 |
C.负极反应式为 |
| D.若去掉阳离子交换膜,电池也能正常工作 |
您最近一年使用:0次
2024-03-13更新
|
325次组卷
|
2卷引用:陕西省西安市铁一中学2023-2024学年高二上学期期末考试化学试题



