2024高三下·全国·专题练习
1 . 镓是优良的半导体材料。氮化镓是制作发光二极管的新材料,用于雷达、卫星通信设备等。某工厂利用铝土矿(主要成分为 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
②当溶液中可溶组分浓度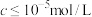 时,可认为已除尽。
时,可认为已除尽。
③金属离子氢氧化物的溶度积(25℃)
④ 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。
回答下列问题:
(1)“二次酸化”中 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为______ 。
(2)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式______ 。
(3)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式______ 。
 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
②当溶液中可溶组分浓度
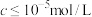 时,可认为已除尽。
时,可认为已除尽。③金属离子氢氧化物的溶度积(25℃)
 |  |  | |
 | 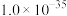 | 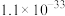 |  |
 、
、 均为两性,
均为两性, 的酸性略强于
的酸性略强于 。
。回答下列问题:
(1)“二次酸化”中
 与足量
与足量 发生反应的离子方程式为
发生反应的离子方程式为(2)“电解”可得金属镓(铝不干扰镓盐的电解),写出阴极电极反应式
(3)“合成”得到的三甲基镓与氨反应得到氮化镓,写出此反应的化学方程式
您最近半年使用:0次
2024高三下·全国·专题练习
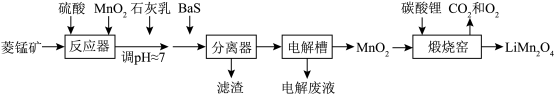
2 . LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如下:
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______ 。
(2)在电解槽中,发生电解反应的离子方程式为_______ 。
(3)煅烧窑中,生成LiMn2O4反应的化学方程式是_______ 。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)在电解槽中,发生电解反应的离子方程式为
(3)煅烧窑中,生成LiMn2O4反应的化学方程式是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为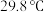 ;
;
② (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
回答下列问题:
(1)“电解精炼”装置如图所示,电解池温度控制在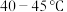 的原因是
的原因是_______ ,阴极的电极反应式为_______ ;
 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: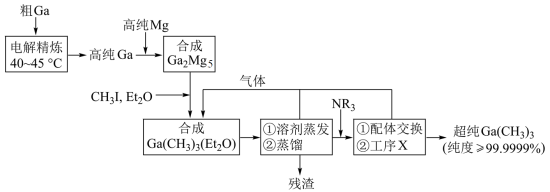
 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为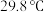 ;
;②
 (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;③相关物质的沸点:
| 物质 | 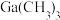 |  | 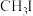 | 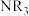 |
沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
(1)“电解精炼”装置如图所示,电解池温度控制在
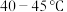 的原因是
的原因是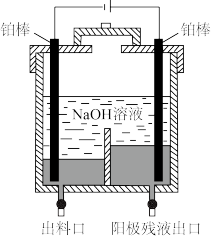
您最近半年使用:0次
解题方法
4 .  为高效绿色氧化剂,一种利用电催化法制备
为高效绿色氧化剂,一种利用电催化法制备 的方法如图所示:
的方法如图所示:
 为高效绿色氧化剂,一种利用电催化法制备
为高效绿色氧化剂,一种利用电催化法制备 的方法如图所示:
的方法如图所示: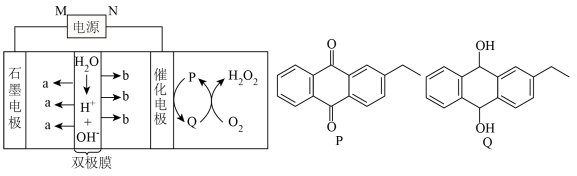
| A.催化电极的电势高于石墨电极的电势 |
B.a为 ,b为 ,b为 |
C.催化电极上的电极反应式: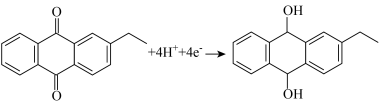 |
D.若电源用铅蓄电池,每制得 ,铅蓄电池正极质量增加32g ,铅蓄电池正极质量增加32g |
您最近半年使用:0次
5 . 相同金属在其不同浓度盐溶液中可形成浓差电池。如图所示装置是利用浓差电池电解 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH.下列说法错误的是
和NaOH.下列说法错误的是
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH.下列说法错误的是
和NaOH.下列说法错误的是
A.b电极的电极反应式为 |
| B.电池放电过程中,Cu(1)电极为该电池的正极 |
| C.电池从开始工作到停止放电,理论上可制得标准状况下44.8L气体 |
| D.若开始前两铜电极的质量相同,当电路中转移0.2mol电子时,两铜电极的质量相差12.8g |
您最近半年使用:0次
名校
解题方法
6 . 烟气脱硝技术是烟气治理的发展方向和研究热点。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
则该反应的ΔH=___________ kJ/mol。
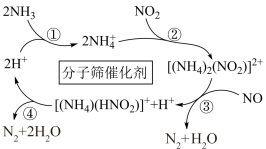
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。___________ 。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为___________ 。
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为___________ (用“→”标出其中的配位键)
(4)以连二硫酸根(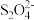 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:___________ 。
②NO吸收转化后的主要产物为 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为___________ mL。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
| 化学键 | NO中的氮氧键 | N-H | N≡N | O-H |
| 键能(kJ/mol) | a | b | c | d |
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为
(4)以连二硫酸根(
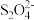 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示: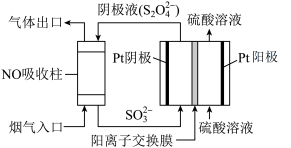
②NO吸收转化后的主要产物为
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
您最近半年使用:0次
解题方法
7 . 利用氟磷灰石[主要成分为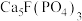 杂质为
杂质为 等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾(
等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾( ),工艺流程如下。
),工艺流程如下。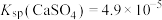 ,
,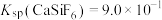 ,
,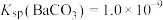 ,
,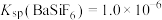 ,
,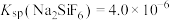 。
。
(1)“酸浸Ⅰ”中生成 ,其化学方程式为
,其化学方程式为______ 。
(2)“酸浸Ⅱ”中,滤渣的主要成分为______ 。
(3)“脱氟”中试剂X为______ (填“ ”或“
”或“ ”);当
”);当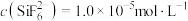 时,溶液中试剂X电离出的剩余金属阳离子的浓度为
时,溶液中试剂X电离出的剩余金属阳离子的浓度为______  。
。
(4)“中和法”为获得较高纯度的 ,控制pH范围为
,控制pH范围为______ ;在此pH范围内纯度的 溶液中各微粒浓度大小关系为
溶液中各微粒浓度大小关系为______ 。
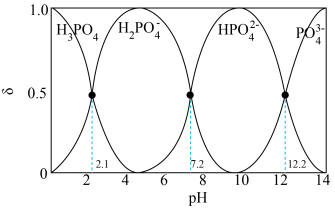
已知:溶液中 、
、 、
、 、
、 的分布分数
的分布分数 随pH变化曲线如图。[如
随pH变化曲线如图。[如 分布分数:
分布分数: ]
]______ 。
②分析产品室可得到 的原因
的原因______ 。
③相较于“中和法”,“电解法”的优点有______ (写出2条即可)。
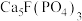 杂质为
杂质为 等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾(
等]为原料生产可应用于巨型激光器“神光二号”的磷酸二氢钾( ),工艺流程如下。
),工艺流程如下。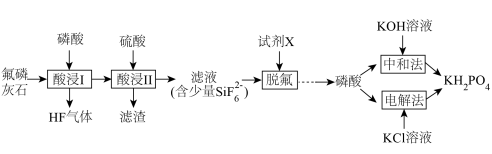
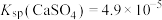 ,
,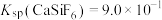 ,
,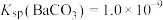 ,
,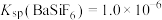 ,
,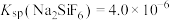 。
。(1)“酸浸Ⅰ”中生成
 ,其化学方程式为
,其化学方程式为(2)“酸浸Ⅱ”中,滤渣的主要成分为
(3)“脱氟”中试剂X为
 ”或“
”或“ ”);当
”);当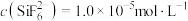 时,溶液中试剂X电离出的剩余金属阳离子的浓度为
时,溶液中试剂X电离出的剩余金属阳离子的浓度为 。
。(4)“中和法”为获得较高纯度的
 ,控制pH范围为
,控制pH范围为 溶液中各微粒浓度大小关系为
溶液中各微粒浓度大小关系为已知:溶液中
 、
、 、
、 、
、 的分布分数
的分布分数 随pH变化曲线如图。[如
随pH变化曲线如图。[如 分布分数:
分布分数: ]
]
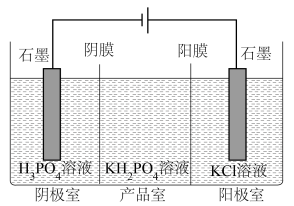
②分析产品室可得到
 的原因
的原因③相较于“中和法”,“电解法”的优点有
您最近半年使用:0次
8 . 我国科学家以海水为氯源合成 ,
, -二氯酮,其装置如图。并以其为原料合成药物米托坦c,合成路线为
-二氯酮,其装置如图。并以其为原料合成药物米托坦c,合成路线为
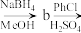
 。下列说法
。下列说法
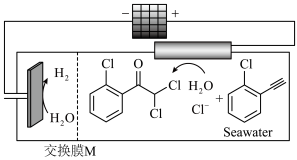
A.阳极反应: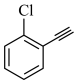 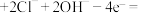   |
| B.M为阳离子交换膜 |
C.b为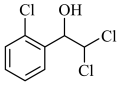 |
| D.整个转化中碳原子的杂化轨道类型有3种 |
您最近半年使用:0次
9 . 我国提出“碳达峰”目标是在2030年前达到最高值,2060年前达到“碳中和”。因此,二氧化碳的综合利用尤为重要。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚( )也有广泛的应用。
)也有广泛的应用。
反应I:
反应II:
反应III: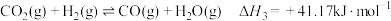
① 自发反应的条件是
自发反应的条件是____________ 。
②恒压、投料比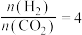 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如图所示:
消耗总量的百分比)如图所示:____________ 。
A.从反应体系中分离出 ,能使反应II反应速率加快
,能使反应II反应速率加快
B.使用更高效的催化剂能提高 的平衡产率
的平衡产率
C.考虑工业生产的综合经济效益,应选择较低温度以提高 的平衡产率
的平衡产率
D.若增大 与
与 的混合比例,可提高
的混合比例,可提高 平衡转化率
平衡转化率
II.当温度超过 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是____________ 。
(2)研究表明,在电解质水溶液中, 气体可被电化学还原。
气体可被电化学还原。
① 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(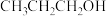 )的电极反应方程式为
)的电极反应方程式为____________ 。
②在电解质水溶液中,三种不同催化剂(a、b、c)上 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为____________ (用a、b、c字母排序)。 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示(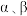 表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,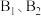 位点带部分负电荷)。
位点带部分负电荷)。 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;步骤II可描述为:
位点上;步骤II可描述为:____________ 。
(1)通过使用不同新型催化剂,实现二氧化碳加氢合成转化为二甲醚(
 )也有广泛的应用。
)也有广泛的应用。反应I:

反应II:

反应III:
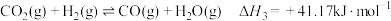
①
 自发反应的条件是
自发反应的条件是②恒压、投料比
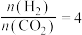 的情况下,不同温度下
的情况下,不同温度下 的平衡转化率和产物的选择性(选择性是指生成某物质消耗的
的平衡转化率和产物的选择性(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)如图所示:
消耗总量的百分比)如图所示: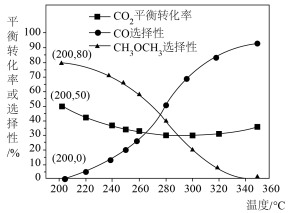
A.从反应体系中分离出
 ,能使反应II反应速率加快
,能使反应II反应速率加快B.使用更高效的催化剂能提高
 的平衡产率
的平衡产率C.考虑工业生产的综合经济效益,应选择较低温度以提高
 的平衡产率
的平衡产率D.若增大
 与
与 的混合比例,可提高
的混合比例,可提高 平衡转化率
平衡转化率II.当温度超过
 ,
, 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是(2)研究表明,在电解质水溶液中,
 气体可被电化学还原。
气体可被电化学还原。①
 在碱性介质中电还原为正丙醇(
在碱性介质中电还原为正丙醇(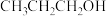 )的电极反应方程式为
)的电极反应方程式为②在电解质水溶液中,三种不同催化剂(a、b、c)上
 电还原为
电还原为 的反应进程中(
的反应进程中( 被还原为
被还原为 的反应可同时发生),相对能量变化如图。由此判断,
的反应可同时发生),相对能量变化如图。由此判断, 电还原为
电还原为 从易到难的顺序为
从易到难的顺序为
 参与的乙苯脱氢机理如图所示(
参与的乙苯脱氢机理如图所示(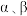 表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正电荷,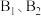 位点带部分负电荷)。
位点带部分负电荷)。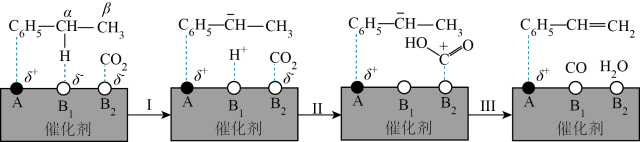
 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;步骤II可描述为:
位点上;步骤II可描述为:
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)一种脱除和利用水煤气中 方法的示意图如下:
方法的示意图如下: 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
___________ (该温度下 的
的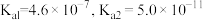 );
);
②再生塔中产生 的离子方程式为
的离子方程式为___________ ;
③利用电化学原理,将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为___________ 。
(1)一种脱除和利用水煤气中
 方法的示意图如下:
方法的示意图如下: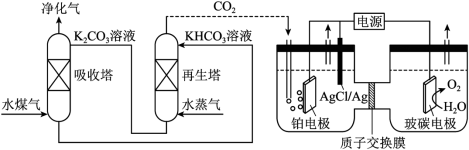
 溶液吸收一定量的
溶液吸收一定量的 后,
后, ,则该溶液的
,则该溶液的
 的
的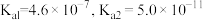 );
);②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理,将
 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为
您最近半年使用:0次



