2024·北京·模拟预测
名校
解题方法
1 . Ⅰ.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(MgxFe2-xSiO4)。回答下列问题:
(1)基态Fe原子的价电子排布式为_______ 。橄榄石中,各元素电负性大小顺序为_______ ,铁的化合价为_______ 。
Ⅱ.已知一些物质的熔点数据如下表:
(2)SiCl4的空间结构为_______ ,其中Si的轨道杂化类型为_______ 。
(3)以上四种氯化物熔点大小不同的原因是_______________________________ 。
Ⅲ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。_______ 。
(5)铁镁合金的化学式为_______ 。
Ⅳ.已知的晶胞属于立方体,晶胞参数 ,密度为
,密度为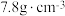 。
。
(6) 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,1pm=10-12m,阿伏加德罗常数的值为 )。
)。
(1)基态Fe原子的价电子排布式为
Ⅱ.已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
 | 800.7 |
 |  |
 | 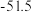 |
 |  |
(2)SiCl4的空间结构为
(3)以上四种氯化物熔点大小不同的原因是
Ⅲ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
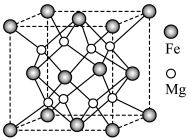
(5)铁镁合金的化学式为
Ⅳ.已知的晶胞属于立方体,晶胞参数
 ,密度为
,密度为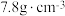 。
。(6)
 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。
您最近半年使用:0次
解题方法
2 . 硒 是人体必需微量元素之一,含硒化合物在药物和材料等领域具有广泛的应用。乙烷硒啉是一种抗癌新药,其结构式如下图所示:
是人体必需微量元素之一,含硒化合物在药物和材料等领域具有广泛的应用。乙烷硒啉是一种抗癌新药,其结构式如下图所示:_______ 区。
(2) 与S同主族,则基态硒原子的核外电子排布式为
与S同主族,则基态硒原子的核外电子排布式为_______ 。
(3) 、O、N的第一电离能由大到小的顺序为
、O、N的第一电离能由大到小的顺序为_______ 。
(4)比较键角大小:气态 分子
分子_______  离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是_______ 。
(5)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为_______ (用文字描述),其中 原子采用的轨道杂化方式为
原子采用的轨道杂化方式为_______ 。
(6)甲硒醇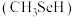 可增加抗癌效力,下表中有机物沸点不同的原因是
可增加抗癌效力,下表中有机物沸点不同的原因是_______ 。
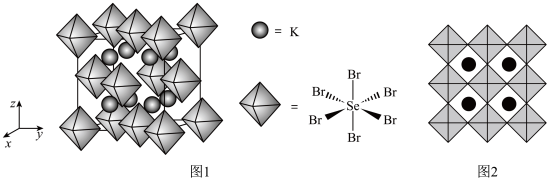
(7)化合物X是通过理论计算的方法筛选出的潜在热电材料之一,其晶胞结构如题图1,沿x、y、z轴方向的投影均为题图2。则X的化学式为_______ 。
 是人体必需微量元素之一,含硒化合物在药物和材料等领域具有广泛的应用。乙烷硒啉是一种抗癌新药,其结构式如下图所示:
是人体必需微量元素之一,含硒化合物在药物和材料等领域具有广泛的应用。乙烷硒啉是一种抗癌新药,其结构式如下图所示: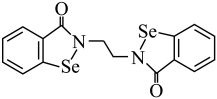
(2)
 与S同主族,则基态硒原子的核外电子排布式为
与S同主族,则基态硒原子的核外电子排布式为(3)
 、O、N的第一电离能由大到小的顺序为
、O、N的第一电离能由大到小的顺序为(4)比较键角大小:气态
 分子
分子 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(5)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为 原子采用的轨道杂化方式为
原子采用的轨道杂化方式为(6)甲硒醇
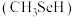 可增加抗癌效力,下表中有机物沸点不同的原因是
可增加抗癌效力,下表中有机物沸点不同的原因是| 有机物 | 甲醇 | 甲硫醇 | 甲硒醇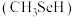 |
| 沸点/℃ | 64.7 | 5.95 | 25.05 |
(7)化合物X是通过理论计算的方法筛选出的潜在热电材料之一,其晶胞结构如题图1,沿x、y、z轴方向的投影均为题图2。则X的化学式为
您最近半年使用:0次
3 . 二氯草酸硼酸锂[LiBF2(C2O4)]是新型锂离子电池电解质,乙酸锰可用于制造离子电池的负极材料,他们的合成方法如下:
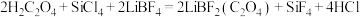

(1)基态 核外电子排布式为
核外电子排布式为___________ ,C、N、O第一电离能由小到大的顺序是___________ 。
(2)草酸(HOOCCOOH)分子中碳原子的杂化轨道类型是___________ , 草酸分子中含有σ键与
草酸分子中含有σ键与 键的数目之比为
键的数目之比为___________ 。
(3)与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为___________ 。
(4) 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为___________ 。
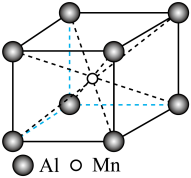
(5)镧锰合金的晶胞如图所示,锰原子除了1个在体心外,其余都在面心上。该合金中锰原子和镧原子的个数比为___________ 。 代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为
代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为___________  。
。
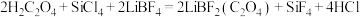

(1)基态
 核外电子排布式为
核外电子排布式为(2)草酸(HOOCCOOH)分子中碳原子的杂化轨道类型是
 草酸分子中含有σ键与
草酸分子中含有σ键与 键的数目之比为
键的数目之比为(3)与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)
 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为(5)镧锰合金的晶胞如图所示,锰原子除了1个在体心外,其余都在面心上。该合金中锰原子和镧原子的个数比为
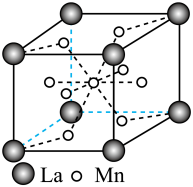
 代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为
代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为 。
。
您最近半年使用:0次
4 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。下列有关说法正确的是

A.电负性由大到小的顺序: |
B. 中 中 的键角大于该配合物中 的键角大于该配合物中 的键角 的键角 |
| C.该物质中存在的化学键有配位键、共价键、氢键 |
| D.从分子结构的角度分析可知甘氨酸易溶于水 |
您最近半年使用:0次
解题方法
5 . 钙钛矿是指通式为ABO3的一类化合物,最早发现钙钛矿石中的CaTiO3,因此而得名。钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等的功能材料。
1.基态 原子中未成对电子数为
原子中未成对电子数为___________ 。
2. 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
 的立方晶胞如图1所示。
的立方晶胞如图1所示。___________ 。
4.金属离子与氧离子间的作用力为 。
5.晶胞中与 距离最近且相等的
距离最近且相等的 数目为 。
数目为 。
一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子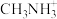 ,其晶胞如图2所示。
,其晶胞如图2所示。 具有相同的空间位置的微粒是 。
具有相同的空间位置的微粒是 。
7.有机碱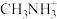 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是___________ 。
8.若晶胞参数为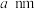 ,则晶体密度为
,则晶体密度为___________  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
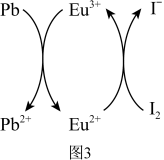
用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了的器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示。___________ 、___________ 。
1.基态
 原子中未成对电子数为
原子中未成对电子数为2.
 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是| 化合物 |  |  |  |  |
熔点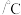 | 377 | -24.12 | 38.3 | 155 |
 的立方晶胞如图1所示。
的立方晶胞如图1所示。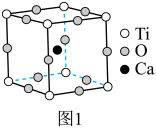
4.金属离子与氧离子间的作用力为 。
| A.离子键 | B.金属键 | C.共价键 | D.分子间作用力 |
 距离最近且相等的
距离最近且相等的 数目为 。
数目为 。| A.4 | B.8 | C.12 | D.16 |
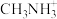 ,其晶胞如图2所示。
,其晶胞如图2所示。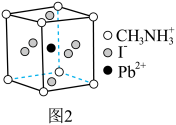
 具有相同的空间位置的微粒是 。
具有相同的空间位置的微粒是 。A. | B. | C. | D.无 |
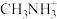 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是8.若晶胞参数为
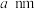 ,则晶体密度为
,则晶体密度为 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了的器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图3所示。
您最近半年使用:0次
6 . 因优越的光电特性, 与
与 成为稀磁半导体
成为稀磁半导体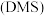 热门的基质材料。
热门的基质材料。
(1)锌原子的价层电子排布式为_____ 。核外电子占据的原子轨道共_____ 个。
(2)纳米二氧化钛是一种催化剂,如:_____ 。
②甲中碳原子的杂化方式为_____ ,乙中手性碳原子个数为_____ 。
③ 中
中 键的数目为
键的数目为_____ 。 离子位于
离子位于 离子围成的
离子围成的_____ 形空隙的中心。
②已知 离子和
离子和 离子的最短距离为
离子的最短距离为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,该晶体的密度为
,该晶体的密度为_____ 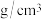 。(用计算式表示)
。(用计算式表示)
 与
与 成为稀磁半导体
成为稀磁半导体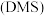 热门的基质材料。
热门的基质材料。(1)锌原子的价层电子排布式为
(2)纳米二氧化钛是一种催化剂,如:
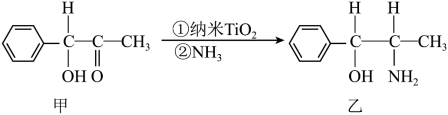
②甲中碳原子的杂化方式为
③
 中
中 键的数目为
键的数目为④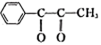 与甲的相对分子质量相似,但是甲的沸点比它高得多,其原因是
与甲的相对分子质量相似,但是甲的沸点比它高得多,其原因是
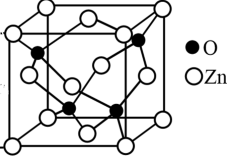
 离子位于
离子位于 离子围成的
离子围成的②已知
 离子和
离子和 离子的最短距离为
离子的最短距离为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,该晶体的密度为
,该晶体的密度为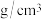 。(用计算式表示)
。(用计算式表示)
您最近半年使用:0次
7 . 氮、磷、铁及其化合物在工农业生产、生活和科研中有着广泛的应用。回答下列问题:
(1)基态 的价层电子轨道表示式为
的价层电子轨道表示式为______ 。
(2) 、
、 、
、 等易形成配合物,
等易形成配合物, 的空间结构名称为
的空间结构名称为______ 。
(3)已知 的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式
的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式______ 。
(4)下列关于 、
、 及其化合物结构与性质的论述正确的是______。
及其化合物结构与性质的论述正确的是______。
(5) 与
与 形成的某化合物晶体的晶胞如图,该化合物的化学式为
形成的某化合物晶体的晶胞如图,该化合物的化学式为______ 。 键,可记为
键,可记为 (右下角“6”表示6个原子,右上角“6”表示6个共用电子),杂环化合物咪唑结构如图,其分子中的大
(右下角“6”表示6个原子,右上角“6”表示6个共用电子),杂环化合物咪唑结构如图,其分子中的大 键可表示为
键可表示为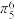 ,则其结合质子能力更强的氮原子是
,则其结合质子能力更强的氮原子是______ (填“①”或“②”),其原因是______ 。
(1)基态
 的价层电子轨道表示式为
的价层电子轨道表示式为(2)
 、
、 、
、 等易形成配合物,
等易形成配合物, 的空间结构名称为
的空间结构名称为(3)已知
 的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式
的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式(4)下列关于
 、
、 及其化合物结构与性质的论述正确的是______。
及其化合物结构与性质的论述正确的是______。A. 与 与 均为正四面体型的分子晶体,都难以分解和氧化 均为正四面体型的分子晶体,都难以分解和氧化 |
B. 的电负性比 的电负性比 的大,可推断 的大,可推断 分子的极性比 分子的极性比 的大 的大 |
C. 和 和 分子的 分子的 模型为四面体形, 模型为四面体形, 中键角 中键角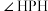 大于 大于 中 中 |
D.研究发现固态 中含有 中含有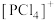 和 和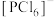 ,而 ,而 中则含有 中则含有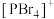 和 和 ,存在差异的原因是 ,存在差异的原因是 半径大 半径大 |
(5)
 与
与 形成的某化合物晶体的晶胞如图,该化合物的化学式为
形成的某化合物晶体的晶胞如图,该化合物的化学式为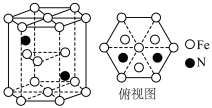
 键,可记为
键,可记为 (右下角“6”表示6个原子,右上角“6”表示6个共用电子),杂环化合物咪唑结构如图,其分子中的大
(右下角“6”表示6个原子,右上角“6”表示6个共用电子),杂环化合物咪唑结构如图,其分子中的大 键可表示为
键可表示为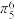 ,则其结合质子能力更强的氮原子是
,则其结合质子能力更强的氮原子是
您最近半年使用:0次
8 . A、B、C、D、E是五种原子序数依次递增的短周期元素。已知:A的一种同位素可以用于测定文物的年代;基态C原子含3对成对电子;D在同周期金属元素中第一电离能最大;基态E原子的3p轨道中含有自旋方向不同且数目之比为3:1的电子。下列说法正确的是
| A.简单离子的离子半径:B<C<D<E |
| B.简单氢化物的沸点:A<B<C<E |
| C.D的单质可以在A和C形成的某种化合物中燃烧 |
| D.Xe(氙)是目前最易形成化合物的稀有气体,XeC3为非极性分子 |
您最近半年使用:0次
解题方法
9 . 某钠离子电池以 的碳酸丙烯酯溶液作电解质溶液,
的碳酸丙烯酯溶液作电解质溶液,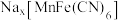 作正极材料,
作正极材料, 作负极材料。
作负极材料。
(1) 与环氧丙烷(
与环氧丙烷(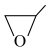 )在一定条件下反应制得碳酸丙烯酯。
)在一定条件下反应制得碳酸丙烯酯。
① 是
是___________ (填“极性”或“非极性”)分子。
②环氧丙烷中,O原子的杂化轨道类型是___________ 杂化。
③沸点:环氧丙烷___________  (填“>”或“<”),解释其原因:
(填“>”或“<”),解释其原因:___________ 。
(2) 溶液与
溶液与 溶液混合可制备
溶液混合可制备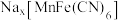 晶体。
晶体。
①基态Mn原子的电子排布式是___________ 。
② 的性质与卤素离子相近,被称为拟卤离子,
的性质与卤素离子相近,被称为拟卤离子, 被称为拟卤素。
被称为拟卤素。
i. 与
与 反应的生成物的结构式分别是
反应的生成物的结构式分别是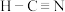 、
、___________ 。
ii. 有酸性但乙炔无明显酸性,
有酸性但乙炔无明显酸性, 的酸性比乙炔的强的原因是
的酸性比乙炔的强的原因是___________ 。
③为防止晶体缺陷过多,制备时反应需缓慢且平稳。先将 溶液与柠檬酸钠(
溶液与柠檬酸钠(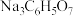 )溶液混合,发生反应:
)溶液混合,发生反应: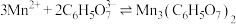 ,再加入
,再加入 溶液以制备
溶液以制备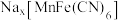 晶体。阐述制备晶体过程中柠檬酸钠溶液的作用:
晶体。阐述制备晶体过程中柠檬酸钠溶液的作用:___________ 。
(3)钠离子电池的正极材料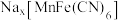 在充、放电过程中某时刻的晶胞示意图如下。
在充、放电过程中某时刻的晶胞示意图如下。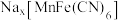 中存在的化学键有配位键、
中存在的化学键有配位键、___________ 。
②该时刻的晶胞所示的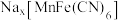 中,
中,
___________ 。
 的碳酸丙烯酯溶液作电解质溶液,
的碳酸丙烯酯溶液作电解质溶液,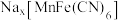 作正极材料,
作正极材料, 作负极材料。
作负极材料。(1)
 与环氧丙烷(
与环氧丙烷( )在一定条件下反应制得碳酸丙烯酯。
)在一定条件下反应制得碳酸丙烯酯。①
 是
是②环氧丙烷中,O原子的杂化轨道类型是
③沸点:环氧丙烷
 (填“>”或“<”),解释其原因:
(填“>”或“<”),解释其原因:(2)
 溶液与
溶液与 溶液混合可制备
溶液混合可制备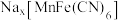 晶体。
晶体。①基态Mn原子的电子排布式是
②
 的性质与卤素离子相近,被称为拟卤离子,
的性质与卤素离子相近,被称为拟卤离子, 被称为拟卤素。
被称为拟卤素。i.
 与
与 反应的生成物的结构式分别是
反应的生成物的结构式分别是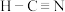 、
、ii.
 有酸性但乙炔无明显酸性,
有酸性但乙炔无明显酸性, 的酸性比乙炔的强的原因是
的酸性比乙炔的强的原因是③为防止晶体缺陷过多,制备时反应需缓慢且平稳。先将
 溶液与柠檬酸钠(
溶液与柠檬酸钠(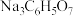 )溶液混合,发生反应:
)溶液混合,发生反应: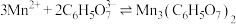 ,再加入
,再加入 溶液以制备
溶液以制备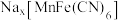 晶体。阐述制备晶体过程中柠檬酸钠溶液的作用:
晶体。阐述制备晶体过程中柠檬酸钠溶液的作用:(3)钠离子电池的正极材料
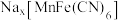 在充、放电过程中某时刻的晶胞示意图如下。
在充、放电过程中某时刻的晶胞示意图如下。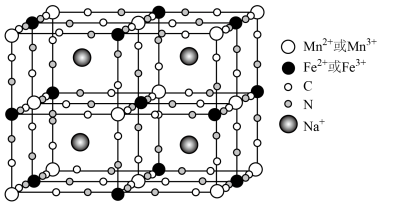
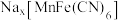 中存在的化学键有配位键、
中存在的化学键有配位键、②该时刻的晶胞所示的
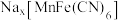 中,
中,
您最近半年使用:0次
解题方法
10 . 铜及其化合物在生活、生产中用途广泛。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为
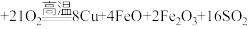 。回答下列问题:
。回答下列问题:
(1)基态铜原子的价层电子的轨道表示式(电子排布图)为______________ ,基态铜原子核外电子的空间运动状态(原子轨道)有__________ 种。
(2)高温下CuO能转化为 的原因是
的原因是_____________ (从原子结构角度分析)。
(3) 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________ ,属于极性分子的是___________ , 、
、 、
、 、
、 四种含硫微粒的空间结构分别为
四种含硫微粒的空间结构分别为____________ 、____________ 、____________ 、____________ 。
(4) 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是_______________ ,1360℃是__________ 的熔点。
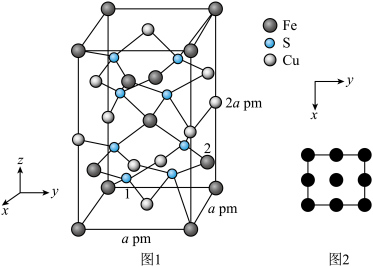
(5) 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为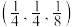 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为____________ 。晶胞参数分别为a pm,a pm、2a pm, 晶体的密度为
晶体的密度为___________  (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。

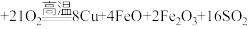 。回答下列问题:
。回答下列问题:(1)基态铜原子的价层电子的轨道表示式(电子排布图)为
(2)高温下CuO能转化为
 的原因是
的原因是(3)
 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是 、
、 、
、 、
、 四种含硫微粒的空间结构分别为
四种含硫微粒的空间结构分别为(4)
 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是(5)
 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为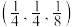 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为 晶体的密度为
晶体的密度为 (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次



