1 . 短周期主族元素W、X、Y、Z的原子序数依次增大。W的原子半径在短周期中最小;X、Z易形成两种常见的共价化合物,且其相对分子质量相差16;X、Z不属于同主族元素。下列说法正确的是
A.原子半径大小: | B.最高价氧化物对应的水化物的酸性: |
| C.X的氢化物的沸点一定低于Z的氢化物 | D.W、X、Y、Z四种元素可形成离子化合物 |
您最近半年使用:0次
解题方法
2 . 已知蓝色环保颜料 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
 由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是
由原子序数依次增大的W、X、Y、Z、R五种短周期主族元素组成,W、R位于同一主族,W元素原子的核外电子数是其周期序数的4倍;X、Y、Z、R位于同一周期,其原子序数之和为54,且只有Y、Z相邻;X的单质可与冷水剧烈反应,下列有关说法正确的是A.简单离子半径: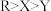 | B.最简单氢化物的稳定性: |
| C.Y的最高价氧化物对应的水化物为强酸 | D.W、Z形成的二元化合物为离子化合物 |
您最近半年使用:0次
名校
解题方法
3 . 下列化学用语或表述错误的是
A.乙烯的球棍模型: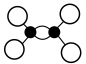 |
B.基态Al原子最高能级的电子云轮廓图: |
C.在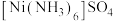 中,阴离子的VSEPR模型名称:正四面体形 中,阴离子的VSEPR模型名称:正四面体形 |
| D.次氯酸钠中含有的化学键类型:极性键、离子键 |
您最近半年使用:0次
7日内更新
|
349次组卷
|
3卷引用:东北三省2024届高三下学期三校二模联考化学试题
4 . 一种麻醉剂的分子结构式如图。其含有的五种元素中, 的原子核只有1个质子;元素
的原子核只有1个质子;元素 、
、 的原子序数依次增大,且均位于
的原子序数依次增大,且均位于 的下一周期;
的下一周期; 原子比
原子比 原子多8个电子。下列说法正确的是
原子多8个电子。下列说法正确的是
 的原子核只有1个质子;元素
的原子核只有1个质子;元素 、
、 的原子序数依次增大,且均位于
的原子序数依次增大,且均位于 的下一周期;
的下一周期; 原子比
原子比 原子多8个电子。下列说法正确的是
原子多8个电子。下列说法正确的是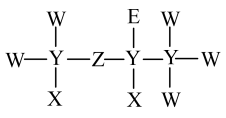
A.原子半径: |
B.由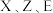 三种元素组成的酸均为强酸 三种元素组成的酸均为强酸 |
C.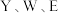 的氢化物中均只含有极性键 的氢化物中均只含有极性键 |
D.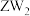 中, 中, 的化合价为-2价 的化合价为-2价 |
您最近半年使用:0次
解题方法
5 . 某阴离子由原子序数依次增大的同周期元素 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是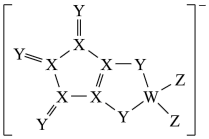
A.最高价含氧酸酸性: |
B. 、 、 的简单氢化物中 的简单氢化物中 的沸点高 的沸点高 |
C.原子半径: |
D.仅由 与 与 形成的化合物中可能含有非极性键 形成的化合物中可能含有非极性键 |
您最近半年使用:0次
名校
6 . 下列说法正确的是
| A.Na2O2和 NaOH 所含化学键类型完全相同 |
| B.NH3比 PH3稳定是因为NH3分子间存在氢键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.H2O2 是含极性键和非极性键的极性分子 |
您最近半年使用:0次
7 . 回答下列问题。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为___________ ,其电子占据的原子轨道数为 ___________ ,最高能层符号为 ___________ 。
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为___________ ,该离子更稳定的原因是 ___________ 。
(3)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是___________  填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是___________ ,属于共价化合物的是___________ 。
(1)V2O5是常见催化剂,V的基态原子的价电子排布式为
(2)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子简化的核外电子排布式为
(3)基态S原子电子占据最高能级的电子云轮廓图为
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S只由离子键构成的物质是
 填序号,下同
填序号,下同 ,由离子键和非极性共价键构成的物质是
,由离子键和非极性共价键构成的物质是
您最近半年使用:0次
解题方法
8 . 下列有关物质结构和性质的说法错误的是
A. 晶体中存在 晶体中存在 与 与 之间的离子键,为强烈相互作用 之间的离子键,为强烈相互作用 |
B.依据价层电子对互斥理论预测, 的空间结构为三角锥形 的空间结构为三角锥形 |
| C.液氧和煤油可做火箭推进剂,液氧分子间靠范德华力凝聚在一起 |
D.NaCl(800.7℃)的熔点远高于 (-68.8℃),原因是两者晶体类型不同 (-68.8℃),原因是两者晶体类型不同 |
您最近半年使用:0次
7日内更新
|
160次组卷
|
2卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
名校
9 . Ⅰ.A、B、C、D、E五种元素的核电荷数均小于18,且依次增大。A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子最外层电子数是次外层电子数的3倍,E的最高价氧化物对应水化物的碱性在短周期元素中最强。
(1)B元素原子的结构示意图:_______ 。
(2)甲、乙、丙、丁是由以上部分元素组成的10电子微粒。阳离子甲和阴离子乙在加热条件下生成的丙和丁,请写出该反应的离子方程式_______ 。
(3)化合物W是由元素D和E组成的淡黄色固体,则W的电子式为_______ 。
(4)由元素A、C、D组成的盐M,其中含有的化学键类型有_______ ,属于_______ (共价化合物或离子化合物)。
Ⅱ.最近,德国科学家实现了Rb原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知Rb的原子序数为37,相对原子质量是85。
(5)Rb在元素周期表中的位置为_______ 。下列关于Rb的说法中不正确的是_______ 。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)B元素原子的结构示意图:
(2)甲、乙、丙、丁是由以上部分元素组成的10电子微粒。阳离子甲和阴离子乙在加热条件下生成的丙和丁,请写出该反应的离子方程式
(3)化合物W是由元素D和E组成的淡黄色固体,则W的电子式为
(4)由元素A、C、D组成的盐M,其中含有的化学键类型有
Ⅱ.最近,德国科学家实现了Rb原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知Rb的原子序数为37,相对原子质量是85。
(5)Rb在元素周期表中的位置为
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
您最近半年使用:0次
名校
10 . 某种食品膨松剂由原子序数依次增大的R、W、X、Y、Z五种主族元素组成。五种元素分处三个短周期,X、Z同主族,R、W、X的原子序数之和与Z的原子序数相等,Y原子的最外层电子数是Z原子的一半。下列说法正确的是
| A.简单氢化物的稳定性:W>X>Z | B.R、W、X只能组成共价化合物 |
| C.最高正价:Y<W<X | D.Y的氧化物和NaOH溶液能发生反应 |
您最近半年使用:0次



