名校
解题方法
1 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是_______ 。
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:_______ ;在元素周期表中,该元素在_______ (填“s”“p”“d”“f”或“ds”)区。
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式_______ ,该阴离子中存在的化学键有_______ (填字母代号)
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
您最近半年使用:0次
昨日更新
|
61次组卷
|
2卷引用:江西省南昌市第十中学2023-2024学年高二下学期第一次月考化学试卷
解题方法
2 . 科学研究发现,甲醇( )和羰基硫(OCS)是火星上存在的有机物。回答下列问题:
)和羰基硫(OCS)是火星上存在的有机物。回答下列问题:
(1)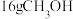 中含有
中含有___________ molσ键。
(2)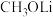 常用于酯交换等有机合成。下列各种Li原子轨道表示式表示的状态中,能量最高和最低的分别为
常用于酯交换等有机合成。下列各种Li原子轨道表示式表示的状态中,能量最高和最低的分别为___________ 、___________ (填标号)。 与
与 具有相同的电子结构,但
具有相同的电子结构,但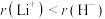 ,原因是
,原因是___________ 。
(3) 分子的键角为
分子的键角为___________ ;OCS分子中,键长:C=O___________ (填“>”或“<”,下同)C=S;键能:C=O___________ C=S。
 )和羰基硫(OCS)是火星上存在的有机物。回答下列问题:
)和羰基硫(OCS)是火星上存在的有机物。回答下列问题:(1)
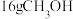 中含有
中含有(2)
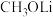 常用于酯交换等有机合成。下列各种Li原子轨道表示式表示的状态中,能量最高和最低的分别为
常用于酯交换等有机合成。下列各种Li原子轨道表示式表示的状态中,能量最高和最低的分别为A. 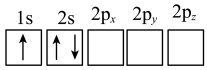 B.
B. 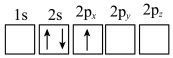
C.  D.
D. 
 与
与 具有相同的电子结构,但
具有相同的电子结构,但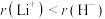 ,原因是
,原因是(3)
 分子的键角为
分子的键角为
您最近半年使用:0次
3 . 下列轨道表示式(电子排布图)能表示基态硫原子的最外电子层结构的是
A.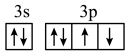 | B.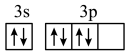 | C.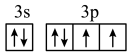 | D.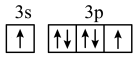 |
您最近半年使用:0次
名校
解题方法
4 . 二氧化锰是工业上常用的氧化剂、催化剂,以菱锰矿(主要成分 ,还含有
,还含有 ,
, 、
、 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图:
的工艺流程如图: ,
, ,
,
回答下列问题:
(1)在 中,元素Mn与O的基态原子核外未成对电子数较多的是
中,元素Mn与O的基态原子核外未成对电子数较多的是___________ 。
(2)“中和除杂1”是将铁、铝元素转化为沉淀除去,物质X最好选用___________(填标号)。
(3)“除杂2”除去的主要离子是___________ (填离子符号)。
(4)用惰性电极电解 溶液获得
溶液获得 的过程如图所示:
的过程如图所示:___________ 极。
②理论上,当电路中转移10 mol电子时,左室产生气体的质量为___________ g。
③右室的电极反应式为___________ 。
(5)电解后的废液中依然存在 ,通常用
,通常用 处理。25°C,向含有0.02 mol/L
处理。25°C,向含有0.02 mol/L  的溶液中通入一定量的
的溶液中通入一定量的 气体,当
气体,当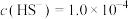 mol/L时,
mol/L时, 开始沉淀,此时溶液的
开始沉淀,此时溶液的
___________ 。[已知:25℃, 的电离常数
的电离常数 ,
,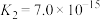 ,
, ]。
]。
(6) 溶液在碱性条件下可将烟气中的NO转化成
溶液在碱性条件下可将烟气中的NO转化成 ,反应的离子方程式为
,反应的离子方程式为___________ 。
 ,还含有
,还含有 ,
, 、
、 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图:
的工艺流程如图: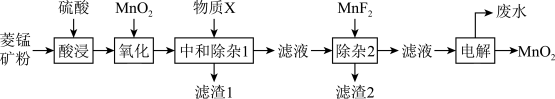
 ,
, ,
,
回答下列问题:
(1)在
 中,元素Mn与O的基态原子核外未成对电子数较多的是
中,元素Mn与O的基态原子核外未成对电子数较多的是(2)“中和除杂1”是将铁、铝元素转化为沉淀除去,物质X最好选用___________(填标号)。
A. | B. | C.NaOH | D. |
(3)“除杂2”除去的主要离子是
(4)用惰性电极电解
 溶液获得
溶液获得 的过程如图所示:
的过程如图所示: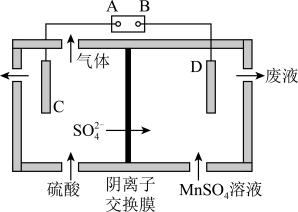
②理论上,当电路中转移10 mol电子时,左室产生气体的质量为
③右室的电极反应式为
(5)电解后的废液中依然存在
 ,通常用
,通常用 处理。25°C,向含有0.02 mol/L
处理。25°C,向含有0.02 mol/L  的溶液中通入一定量的
的溶液中通入一定量的 气体,当
气体,当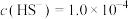 mol/L时,
mol/L时, 开始沉淀,此时溶液的
开始沉淀,此时溶液的
 的电离常数
的电离常数 ,
,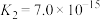 ,
, ]。
]。(6)
 溶液在碱性条件下可将烟气中的NO转化成
溶液在碱性条件下可将烟气中的NO转化成 ,反应的离子方程式为
,反应的离子方程式为
您最近半年使用:0次
名校
5 . 依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是___________ ;基态 的价电子排布图为
的价电子排布图为___________ 。
(2)下列有关微粒性质的排列顺序错误的是___________。
(3)下列基态原子或离子的电子排布式或排布图正确的是___________ (填序号,下同),违反能量最低原理的是___________ ;违反洪特规则的是___________ ;违反泡利原理的是___________ 。___________ 、___________ (填选项字母)。
(1)基态硅原子的电子排布式是
 的价电子排布图为
的价电子排布图为(2)下列有关微粒性质的排列顺序错误的是___________。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
C.离子半径: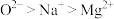 | D.原子的未成对电子数: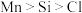 |
(3)下列基态原子或离子的电子排布式或排布图正确的是
① ②
② ③P:
③P: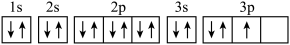
④ ⑤
⑤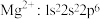 ⑥C:
⑥C: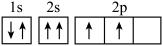
A.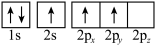 B.
B.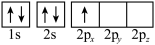 C.
C.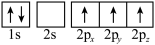 D.
D.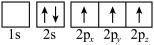
您最近半年使用:0次
解题方法
6 . 下面是第二周期部分元素基态原子的电子排布图:
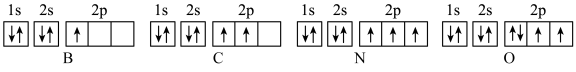
| A.每个原子轨道里最多只能容纳2个电子 |
| B.基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行 |
| C.每个能层所具有的能级数等于能层的序数 |
| D.N原子中有5种电子运动状态 |
您最近半年使用:0次
7 . 下列比较中前者大于后者的是
A.由镁原子核形成的微粒电离一个电子所需最低能量: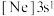 与 与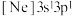 |
| B.基态氟原子:未成对电子数与成对电子数 |
C.H-O-H键角: 与 与 |
D.分子的极性: 与HCN 与HCN |
您最近半年使用:0次
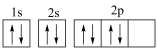
8 . 硅原子核外电子运动状态为___________ 种;基态Si原子,若其电子排布式表示为 违背了
违背了___________ 。
 违背了
违背了
您最近半年使用:0次
名校
9 . 六种36号以前的元素的性质或结构信息见表,试根据信息回答有关问题。
(1)A是___ (填元素名称),在元素周期表中的位置______ 。
(2)B的基态原子的核外电子占据的最高能级的轨道形状和该能级所能容纳的最多电子数分别为______ 、_______ 。
(3)写出C元素基态原子的价层电子轨道表示式_______ ,其基态原子的电子有____ 种空间运动状态。
(4)D、E的元素符号分别为______ 。
| 元素 | A | B | C | D、E |
| 性质或结构信息 | 基态原子有5个原子轨道填充有电子,有3个未成对电子 | 基态原子有16个不同运动状态的电子 | 基态原子的价电子排布为3d104sx,在化合物中只有一种常见化合价 | 两种元素的基态原子都只有一个未成对电子,它们相互形成的离子的电子层结构相同,并且最高能级的电子对数等于其最高能层的电子层数 |
(2)B的基态原子的核外电子占据的最高能级的轨道形状和该能级所能容纳的最多电子数分别为
(3)写出C元素基态原子的价层电子轨道表示式
(4)D、E的元素符号分别为
您最近半年使用:0次

 ,他违背了
,他违背了

