解题方法
1 . 已知:大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是A. 的第二电离能小于 的第二电离能小于 的第二电离能 的第二电离能 |
B. 与 与 均为直线形结构, 均为直线形结构, 中存在大x键,可表示为 中存在大x键,可表示为 |
C.基态 和基态 和基态 的核外电子排布中,未成对电子数之比为 的核外电子排布中,未成对电子数之比为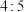 |
D. 中 中 的键角小于 的键角小于 分子中 分子中 的键角 的键角 |
您最近半年使用:0次
2 . 科学家合成了一种含硼阴离子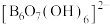 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是
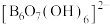 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是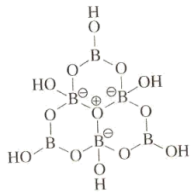
| A.基态硼原子的核外电子的空间运动状态有3种 |
| B.电负性大小为:O>B>H |
| C.该结构中硼原子的杂化方式为sp2、sp3 |
| D.该结构中共有4种不同化学环境的氧原子 |
您最近半年使用:0次
2024·北京·模拟预测
名校
解题方法
3 . Ⅰ.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(MgxFe2-xSiO4)。回答下列问题:
(1)基态Fe原子的价电子排布式为_______ 。橄榄石中,各元素电负性大小顺序为_______ ,铁的化合价为_______ 。
Ⅱ.已知一些物质的熔点数据如下表:
(2)SiCl4的空间结构为_______ ,其中Si的轨道杂化类型为_______ 。
(3)以上四种氯化物熔点大小不同的原因是_______________________________ 。
Ⅲ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。_______ 。
(5)铁镁合金的化学式为_______ 。
Ⅳ.已知的晶胞属于立方体,晶胞参数 ,密度为
,密度为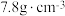 。
。
(6) 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,1pm=10-12m,阿伏加德罗常数的值为 )。
)。
(1)基态Fe原子的价电子排布式为
Ⅱ.已知一些物质的熔点数据如下表:
| 物质 | 熔点/℃ |
 | 800.7 |
 |  |
 | 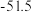 |
 |  |
(2)SiCl4的空间结构为
(3)以上四种氯化物熔点大小不同的原因是
Ⅲ.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
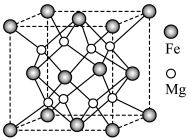
(5)铁镁合金的化学式为
Ⅳ.已知的晶胞属于立方体,晶胞参数
 ,密度为
,密度为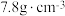 。
。(6)
 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。
您最近半年使用:0次
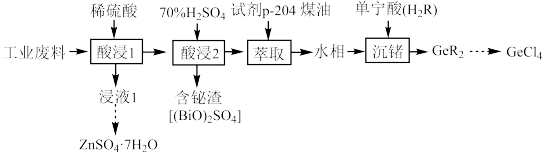
4 . 锌、铋(Bi)、锗(Ge)的单质及其化合物用途较广。利用某冶锌工业废料(主要含ZnO,还含有氧化铋、氧化锗)回收其金属化合物的流程如下(已知:Ge4+易水解,单宁酸为一种弱酸)。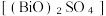 中铋的化合价为
中铋的化合价为_______ ,基态锌原子的价层电子排布式为_______ 。
(2)锌的第二电离能小于铜的第二电离能,原因是_______ 。
(3)提高“酸浸1”浸取率的措施有_______ (写出两条即可)。
(4)“酸浸2”时,Bi2O3发生反应的离子方程式为_______ 。
(5)“沉锗”操作中需调节pH值约为2.5,不能过低,也不能过高,原因是_______ 。
(6)由“浸液1”得到ZnSO4∙7H2O的操作是_______ 、_______ 、过滤、洗涤、干燥。
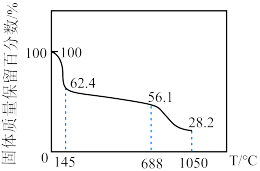
(7)加热ZnSO4∙7H2O,固体质量保留百分数与温度的关系如下图所示。688℃时所得固体的化学式为_______ 。
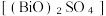 中铋的化合价为
中铋的化合价为(2)锌的第二电离能小于铜的第二电离能,原因是
(3)提高“酸浸1”浸取率的措施有
(4)“酸浸2”时,Bi2O3发生反应的离子方程式为
(5)“沉锗”操作中需调节pH值约为2.5,不能过低,也不能过高,原因是
(6)由“浸液1”得到ZnSO4∙7H2O的操作是
(7)加热ZnSO4∙7H2O,固体质量保留百分数与温度的关系如下图所示。688℃时所得固体的化学式为
您最近半年使用:0次
解题方法
5 . 金属材料对于促进生产发展、改善人类生活发挥了巨大作用。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式___________ 。涩法冶炼是以赤铜矿( )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为___ 。
(3)已知: 晶胞为立方体形,边长为
晶胞为立方体形,边长为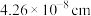 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为___________ 个。计算 晶体的密度
晶体的密度
___________  (结果保留两位小数)。
(结果保留两位小数)。
(4)基态Na原子的价层电子轨道表示式为___________ 。
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:
 ,加入
,加入 的目的是
的目的是___________ 。
(6)除去 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是___________ 。
Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7) 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是___________ 。
(8) 易与
易与 形成
形成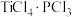 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(9)钛溶于盐酸制得的三氯化钛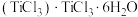 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、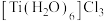 (紫色),两者配位数
(紫色),两者配位数___________ (选填“相同”或“不同”),绿色晶体中配体是___________ 。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式
 )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为
(3)已知:
 晶胞为立方体形,边长为
晶胞为立方体形,边长为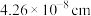 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为 晶体的密度
晶体的密度
 (结果保留两位小数)。
(结果保留两位小数)。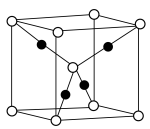
(4)基态Na原子的价层电子轨道表示式为
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:

 ,加入
,加入 的目的是
的目的是(6)除去
 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7)
 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是(8)
 易与
易与 形成
形成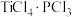 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。| A.键角为120° | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
(9)钛溶于盐酸制得的三氯化钛
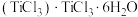 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、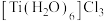 (紫色),两者配位数
(紫色),两者配位数
您最近半年使用:0次
6 . “中国天眼”探测到距离地球79光年的恒星光谱,经光谱分析该恒星的组成元素有硅、磷、铁、硫等。下列说法正确的是
| A.基态磷原子的未成对电子数为3 |
B.硅在周期表中的位置为第3周期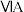 族 族 |
C.铁位于元素周期表的 区 区 |
D.基态硫原子的外围电子轨道表示式为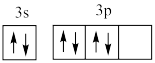 |
您最近半年使用:0次
名校
解题方法
7 . 某化学学习小组在学习元素周期系和周期的划分时提出以下观点:
①元素周期系的形成是由原子的结构决定的
②元素周期系中第ⅠA族元素统称为碱金属元素
③每一周期元素原子外围电子排布均是从ns1开始至ns2np6结束
④元素周期系的每一周期元素的种类均相等
⑤基态原子核外电子排布式为1s22s22p3和1s22s22p63s23p3的两元素位于同一周期
⑥周期序数越大,该周期所含金属元素一般越多
你认为正确的是
①元素周期系的形成是由原子的结构决定的
②元素周期系中第ⅠA族元素统称为碱金属元素
③每一周期元素原子外围电子排布均是从ns1开始至ns2np6结束
④元素周期系的每一周期元素的种类均相等
⑤基态原子核外电子排布式为1s22s22p3和1s22s22p63s23p3的两元素位于同一周期
⑥周期序数越大,该周期所含金属元素一般越多
你认为正确的是
| A.①⑥ | B.①②③⑤⑥ | C.①④⑥ | D.②③⑤ |
您最近半年使用:0次
解题方法
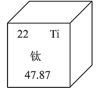
8 . 元素周期表中钛的数据如图所示,47.87的含义是___________ ;Ti在元素周期表中的位置是___________ ;基态钛原子的价电子排布式为___________ (填选项)。
您最近半年使用:0次
解题方法
9 . 锰、铬、铜、铁四种元素的基态原子中,有五个未成对电子的原子核外电子排布式为___________ 。
您最近半年使用:0次
10 . 中国科学家合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料: ,并获得该化合物的LED器件,为白光的应用提供新材料支持。
,并获得该化合物的LED器件,为白光的应用提供新材料支持。
(1)已知 与
与 同族,基态
同族,基态 原子价层电子的运动状态有
原子价层电子的运动状态有__________ 种,基态O原子的电子排布式不能表示为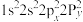 ,因为这违背了
,因为这违背了__________ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2) 、P与S是同周期中相邻的元素,
、P与S是同周期中相邻的元素, 、P、S的电负性由大到小的顺序是
、P、S的电负性由大到小的顺序是__________ ,第一电离能由大到小的顺序是__________ .
(3)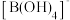 中硼原子的杂化轨道类型为
中硼原子的杂化轨道类型为__________ 。 中,
中, 与0之间不存在的化学键是
与0之间不存在的化学键是__________ (填选项)。
A. 键 B.
键 B. 键 C.配位键 D.极性键
键 C.配位键 D.极性键
(4)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较低的是__________ ,其原因是_______________ 。
(5)超高热导率半导体材料砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的原子坐标为__________ 。已知阿伏加德罗常数的值为 ,若晶胞中
,若晶胞中 原子到B原子最近距离为
原子到B原子最近距离为 ,则该晶体的密度为
,则该晶体的密度为__________ (列出含a、 的计算式即可)。
的计算式即可)。
 ,并获得该化合物的LED器件,为白光的应用提供新材料支持。
,并获得该化合物的LED器件,为白光的应用提供新材料支持。(1)已知
 与
与 同族,基态
同族,基态 原子价层电子的运动状态有
原子价层电子的运动状态有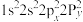 ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)
 、P与S是同周期中相邻的元素,
、P与S是同周期中相邻的元素, 、P、S的电负性由大到小的顺序是
、P、S的电负性由大到小的顺序是(3)
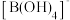 中硼原子的杂化轨道类型为
中硼原子的杂化轨道类型为 中,
中, 与0之间不存在的化学键是
与0之间不存在的化学键是A.
 键 B.
键 B. 键 C.配位键 D.极性键
键 C.配位键 D.极性键(4)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较低的是
(5)超高热导率半导体材料砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的原子坐标为
 ,若晶胞中
,若晶胞中 原子到B原子最近距离为
原子到B原子最近距离为 ,则该晶体的密度为
,则该晶体的密度为 的计算式即可)。
的计算式即可)。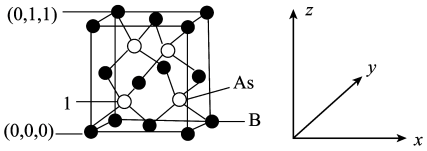
您最近半年使用:0次



