名校
解题方法
1 . 下列各物质的酸性强弱关系正确的是
| A.CH2ClCOOH>CHCl2COOH | B.CCl3COOH<CFCl2COOH |
| C.CH3CF2COOH>CHF2COOH | D.C17H35COOH>C4H9COOH |
您最近一年使用:0次
名校
2 . 已知X、Y元素同周期,且电负性X>Y,下列说法正确的是( )
| A.X与Y形成化合物时,X显正价,Y显负价 | B.第一电离能Y一定小于X |
| C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 | D.气态氢化物的稳定性:HmY小于HnX |
您最近一年使用:0次
2018-02-11更新
|
243次组卷
|
3卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时
3 . 已知A、B、D、E、G、X、Y、Z八种元素的原子序数依次增大。其中,A原子核外电子只有1种运动状态;基态B、E原子的2p轨道均含2个未成对电子;G是周期表中电负性最大的元素;Y和G同主族,X和Y同周期,且X离子是同周期元素简单离子中半径最小的;Z是八种元素中唯一的第四周期元素位于ds区,且基态原子核外只有1个未成对电子其余均为成对电子。推断出元素符号及相应化学式,并回答下列问题:
(1)基态Z原子的简化核外电子排布式:_______ ,基态E原子价层电子轨道表达式:_______ ,基态X原子的核外电子排布共有_______ 个能级。
(2)键能:G-G_______ Y-Y(填“>或<”,后同);B和D的第三电离能:B_______ D。
(3)A2E分子的VSEPR理想模型为_______ ;已知DA3溶于A2E溶液呈碱性,试在方框内画出DA3与A2E的分子间形成的氢键_______ 。

(4)B2A2分子中σ键和π键的比例_______ ;B2A2、E2在NaOH溶液中可构建燃料电池,试写出该燃料电池负极的电极反应式:_______ 。
(1)基态Z原子的简化核外电子排布式:
(2)键能:G-G
(3)A2E分子的VSEPR理想模型为

(4)B2A2分子中σ键和π键的比例
您最近一年使用:0次
名校
4 . 下列说法中错误的是
| A.根据对角线规则,铍和铝的性质具有相似性 |
| B.[Cu(H2O)4]2+中Cu提供空轨道,H2O中O提供孤对电子形成配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.手性分子互为镜像,它们的性质没有区别 |
您最近一年使用:0次
2016-12-09更新
|
526次组卷
|
6卷引用:河北省保定市保定三中2016-2017学年度第二学期3月月考高二化学试题
解题方法
5 . 宏观辨识与微观探析是化学学科的核心素养之一、下列有关物质的微观结构和其性质不相符的是
| 选项 | A | B |
| 微观结构 | 甲烷为正四面体结构 |  中存在分子间氢键 中存在分子间氢键 |
| 性质 | 甲烷为非极性分子 |  分子的稳定性增强 分子的稳定性增强 |
| 选项 | C | D |
| 微观结构 | F的电负性大于H | 石墨每一层的C原子中未参与杂化的电子形成遍布整个层面的大 键 键 |
| 性质 |  的酸性强于 的酸性强于 | 石墨能导电 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 下列说法错误的是
| A.在1个CsCl晶胞中含有1个Cs+ |
| B.SO2在水中的溶解度比CO2在水中的溶解度要大 |
| C.X、Y元素同周期,且电负性X>Y,第一电离能可能Y大于X |
| D.根据电子排布的特点,Cu和Ga在周期表中都属于d区 |
您最近一年使用:0次
名校
解题方法
7 . 硼(B)及其化合物是结构化学的重要研究对象。请回答下列问题:
(1)和B同主族电负性最小的元素[放射性元素(周期表中84号及其后的元素)除外]的价电子排布式为___________ ,Be、B、C的第一电离能由大到小的顺序是___________________ (用元素符号表示)
(2)无机苯(B3N3H6)与苯结构相似,其中B的杂化方式为______________ ,1mol B3N3H6中σ键的数目为______________________ 。
(3)Al和B同主族,其化合物氟化铝的熔沸点远远高于氯化铝,试解释其原因________________ 。
(4)将硼砂(NaB4O7)和NH4C1共热可得白色固体BN和B2O3、方程式_________________________ 。
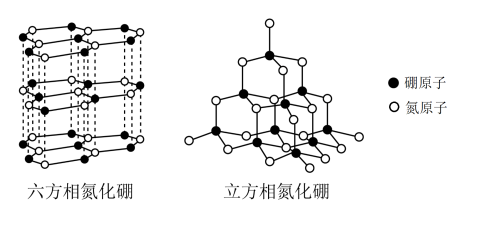
氮化硼有两种晶型结构,一种是六方氮化硼,其结构与石墨相似却不导电,原因是__________________ ;另一种是类似于金刚石结构的立方氮化硼,已知晶胞边长为361.5pm,N原子半径为a pm,则B原子半径为___________ pm(只要求列算式)。
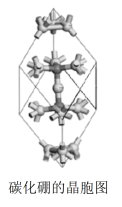
(5)碳化硼是除金刚石和氮化硼外最硬的固体,下图是碳化硼的晶胞简图,该图给出了晶胞中的所有原子,除“三原子”(中心原子和其相连的2个原子)外,晶胞的其余原子都是B12多面体中的1个原子,B12多面体的其他原子都不在晶胞内,均未画出。图中原子旁的短棍表示该原子与其他原子相连,若上述三原子都是碳原子,写出碳化硼的化学式_____________________ 。
(1)和B同主族电负性最小的元素[放射性元素(周期表中84号及其后的元素)除外]的价电子排布式为
(2)无机苯(B3N3H6)与苯结构相似,其中B的杂化方式为
(3)Al和B同主族,其化合物氟化铝的熔沸点远远高于氯化铝,试解释其原因
(4)将硼砂(NaB4O7)和NH4C1共热可得白色固体BN和B2O3、方程式
氮化硼有两种晶型结构,一种是六方氮化硼,其结构与石墨相似却不导电,原因是

(5)碳化硼是除金刚石和氮化硼外最硬的固体,下图是碳化硼的晶胞简图,该图给出了晶胞中的所有原子,除“三原子”(中心原子和其相连的2个原子)外,晶胞的其余原子都是B12多面体中的1个原子,B12多面体的其他原子都不在晶胞内,均未画出。图中原子旁的短棍表示该原子与其他原子相连,若上述三原子都是碳原子,写出碳化硼的化学式

您最近一年使用:0次
名校
8 . 下列各元素电负性大小顺序正确的是( )
| A.K>Na>Li | B.F>O>S | C.As>P>N | D.C>N>O |
您最近一年使用:0次
解题方法
9 . 有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)写出C元素基态原子的电子排布式:_________ 。
(2)用轨道表示式表示D元素原子的价电子构型:________ 。
(3)写出E离子的结构示意图:_________ 。
(4)元素B与D的电负性的大小关系:B________ D,C与E的第一电离能的大小关系:C________ E。(填>、<、=)
(5)由这五种元素组成的一种化合物是(写化学式)________ 。写出该物质的一种主要用途:________ 。
(1)写出C元素基态原子的电子排布式:
(2)用轨道表示式表示D元素原子的价电子构型:
(3)写出E离子的结构示意图:
(4)元素B与D的电负性的大小关系:B
(5)由这五种元素组成的一种化合物是(写化学式)
您最近一年使用:0次
10 . “嫦娥石”是中国首次在月球上发现的新矿物,其主要由Ca、Fe、P、O和Y(钇,原子序数比Fe大13)组成,下列说法正确的是
| A.Y位于元素周期表的第ⅢB族 |
| B.基态Ca原子的核外电子填充在6个轨道中 |
| C.Fe2+和 Fe3+中未成对电子个数之比为4:5 |
| D.5种元素中,电负性最大的是P |
您最近一年使用:0次



