名校
解题方法
1 . 如图为周期表的一小部分,A,B,C,D,E的位置关系如图所示。其中B元素最高化合价是最低化合价绝对值的3倍,它的最高价氧化物中含氧 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A | ||
| D | B | E |
| C |
| A.D,B,E三种元素的第一电离能逐渐减小 |
B.电负性: |
| C.D,B,E三种元素形成的简单离子的半径逐渐减小 |
D.气态氢化物的稳定性顺序: |
您最近一年使用:0次
2 . 下列关于原子结构与元素周期表的说法正确的是
| A.电负性最大的元素位于周期表的左下角 |
| B.基态原子最外层电子排布为ns2的元素都位于周期表IIA族 |
| C.某基态原子的电子排布式为[Ar]3d104s24p1,该元素位于周期表第四周期IIIA族 |
| D.基态原子p能级电子半充满的原子第一电离能一定大于p能级有一对成对电子的 |
您最近一年使用:0次
2020-06-25更新
|
215次组卷
|
3卷引用:河北省张家口市第一中学2021届高三上学期期中考试(普通、实验班)化学试题
3 . 镓、硅、锗、硒的单质及某些化合物如砷化镓、磷化镓等都是常用的半导体材料。
(1)基态锗原子的电子排布式为___________ 。其属于元素周期表中的___________ 区元素。
(2)锗、砷、硒三种元素的第一电离能由大到小的顺序为___________ ,As与Cl能形成AsCl3和AsCl5两种化合物,但N与Cl只能形成NCl3一种化合物的原因为___________ 。
(3)硅能与氢元素形成丁硅烯(Si4H8),该分子中σ键与π键个数之比___________ 。
(4)GaCl3分子中Ga原子的杂化轨道类型为___________ ,GeCl4分子的空间构型为___________ 。与GeCl4互为等电子体的离子为___________ (写2种,写化学式)。
(1)基态锗原子的电子排布式为
(2)锗、砷、硒三种元素的第一电离能由大到小的顺序为
(3)硅能与氢元素形成丁硅烯(Si4H8),该分子中σ键与π键个数之比
(4)GaCl3分子中Ga原子的杂化轨道类型为
您最近一年使用:0次
解题方法
4 . 短周期主族元素X、Y、Z、W的原子序数依次增大,元素Y是地壳中含量最多的元素,X与Z同主族且二者可形成离子化合物,W的最外层电子数是其电子层数的2倍。下列说法正确的是
| A.电负性:X<W<Y | B.第一电离能:Z<W<Y |
| C.元素W的含氧酸均为强酸 | D.Z的氧化物对应的水化物为弱碱 |
您最近一年使用:0次
解题方法
5 . 聚乙二醇(PEG)有良好的生物相容性,在水中可与 形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是

 形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
形成氢键,由“中性聚合物”转变为超分子“聚电解质”,下列说法错误的是
A.PEG中 和 和 的杂化方式相同 的杂化方式相同 | B. 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
C.键角: | D.电负性: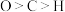 |
您最近一年使用:0次
6 . 下列有关元素周期表及元素周期律的说法错误的是
| A.N能层的能级数最多为3个 |
| B.Cu元素在元素周期表的ds区 |
| C.F元素在同周期中电负性最大 |
| D.根据对角线规则,铍和铝的化学性质具有相似性 |
您最近一年使用:0次
2017-02-17更新
|
402次组卷
|
7卷引用:2016-2017学年河北省邢台市高二上学期第四次月考化学卷
名校
7 . 下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高正化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.S、Cl的电负性和单质的氧化性均依次增强 |
| D.元素周期表中位于金属元素和非金属元素分界线附近的元素属于过渡元素 |
您最近一年使用:0次
2020-03-26更新
|
95次组卷
|
4卷引用:河北省正定中学2019-2020学年高二3月线上月考化学试题
8 . TiCl3是烯烃定向聚合的催化剂、TiCl4可用于制备金属Ti。
nCH3CH=CH2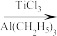
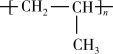
TiO2+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
TiCl4+2Mg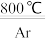 Ti+2MgCl2
Ti+2MgCl2
(1)Ti3+的基态核外电子排布式为__________ 。
(2)丙烯分子中,碳原子轨道杂化类型为______ 和____ 。
(3)Mg、Al、Cl第一电离能由大到小的顺序是___________ 。
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式________ 。
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为______ 。
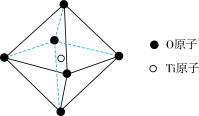
(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为_________ 。
nCH3CH=CH2
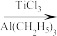
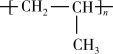
TiO2+2C+2Cl2
 TiCl4+2CO
TiCl4+2COTiCl4+2Mg
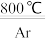 Ti+2MgCl2
Ti+2MgCl2(1)Ti3+的基态核外电子排布式为
(2)丙烯分子中,碳原子轨道杂化类型为
(3)Mg、Al、Cl第一电离能由大到小的顺序是
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为

(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为
您最近一年使用:0次
2019-12-17更新
|
118次组卷
|
2卷引用:河北省承德第一中学2020届高三上学期第三次月考化学试题
9 . 下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7种元素的代号。回答下列问题时,涉及元素书写的请用相应的元素符号。

(1)J基态原子的核外电子排布式为________ 。基态Q2+中未成对电子数为________ ;R和Y的简单离子与Na+半径大小顺序为________ 。
(2)X、Y、Z三种元素电负性由大到小的排序是________ ;X与Y的第一电离能:X________ (填“>”“<”或“=”)Y,其理由是________ 。
(3)检验某溶液中是否含有Q3+的方法是_____________________________ 。
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为________________ 。

(1)J基态原子的核外电子排布式为
(2)X、Y、Z三种元素电负性由大到小的排序是
(3)检验某溶液中是否含有Q3+的方法是
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为
您最近一年使用:0次
2018-02-11更新
|
155次组卷
|
2卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时
名校
解题方法
10 . 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是________ 、________ ;杂化轨道分别是________ 、________ ;a分子的立体结构是________ 。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是________ 晶体、________ 晶体。
(3)Y与Z比较,电负性较大的是________ ,W2+离子的核外电子排布式是________ 。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是
(3)Y与Z比较,电负性较大的是
您最近一年使用:0次



