名校
1 . 壳聚糖是最丰富的天然高分子多糖之一,可由甲壳素在碱性溶液中煮沸制得,其转化关系如图所示。
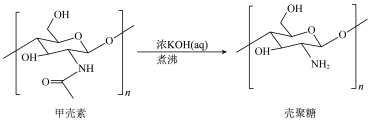
A.电负性: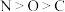 |
| B.水溶性:壳聚糖>甲壳素 |
| C.壳聚糖均既有酸性又有碱性 |
D.1mol甲壳素与足量浓KOH(aq)反应,消耗KOH的物质的量为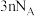 |
您最近一年使用:0次
2024-07-30更新
|
243次组卷
|
2卷引用:湖北省武汉市江岸区2023-2024学年高二下学期7月期末质量检测化学试题
2 . 某农药由原子序数依次增大的V、W、X、Y、Z五种前四周期元素组成。请根据下列相关信息,回答问题。
(1)Y元素在周期表中的位置为第______ 周期第______ 族;基态Z元素原子的最外层电子所占据的原子轨道的电子云轮廓图为______ 形。
(2)位于p区的元素有______ (填元素符号),基态X原子的核外电子的空间运动状态有______ 种。
(3)V、W、X三种元素的电负性由大到小的顺序是______ (用元素符号表示);W、X的最简单氢化物的熔、沸点由大到小的顺序是______ (用化学式表示),原因为______ 。
(4)Y、Z两种元素的最高价氧化物对应的水化物的酸性或碱性最强的是______ 。
| 元素 | 相关信息 |
| V | 核外电子数与周期序数相等 |
| W | 成对电子数与未成对电子数之比为3:1 |
| X | 在火山口附近可看到其淡黄色固体单质 |
| Y | 主族元素,有四个电子层,且最外层电子数与最内层电子数相等 |
| Z | 基态原子的价层电子排布式为3d104s1 |
(2)位于p区的元素有
(3)V、W、X三种元素的电负性由大到小的顺序是
(4)Y、Z两种元素的最高价氧化物对应的水化物的酸性或碱性最强的是
您最近一年使用:0次
3 . 阅读下列材料,完成下面小题:
电池有铅蓄电池、燃料电池(如 电池)、锂离子电池、
电池)、锂离子电池、 一次氯酸盐电池等,它们可以将化学能转化为电能。
一次氯酸盐电池等,它们可以将化学能转化为电能。 都可用作燃料电池的燃料。
都可用作燃料电池的燃料。 的燃烧热为
的燃烧热为 。电解则可以将电能转化为化学能,电解饱和
。电解则可以将电能转化为化学能,电解饱和 溶液可以得到
溶液可以得到 ,用电解法可制备消毒剂高铁酸钠
,用电解法可制备消毒剂高铁酸钠 。
。
1.下列说法正确的是
2.下列化学反应表示正确的是
3.下列物质结构与性质或物质性质与用途不具有 对应关系的是
4.电解法制备 的工作原理如图所示。下列说法正确的是
的工作原理如图所示。下列说法正确的是
电池有铅蓄电池、燃料电池(如
 电池)、锂离子电池、
电池)、锂离子电池、 一次氯酸盐电池等,它们可以将化学能转化为电能。
一次氯酸盐电池等,它们可以将化学能转化为电能。 都可用作燃料电池的燃料。
都可用作燃料电池的燃料。 的燃烧热为
的燃烧热为 。电解则可以将电能转化为化学能,电解饱和
。电解则可以将电能转化为化学能,电解饱和 溶液可以得到
溶液可以得到 ,用电解法可制备消毒剂高铁酸钠
,用电解法可制备消毒剂高铁酸钠 。
。1.下列说法正确的是
A. 中存在配位键 中存在配位键 |
B. 的空间构型为平面正方形 的空间构型为平面正方形 |
C. 中的键角比 中的键角比 中的小 中的小 |
D. 中心原子的轨道杂化类型为 中心原子的轨道杂化类型为 |
A.铅蓄电池的正极反应: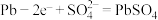 |
B.电解饱和 溶液: 溶液: |
C.表示 的燃烧热: 的燃烧热: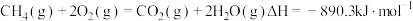 |
D.一定条件下 与 与 的反应: 的反应: |
A. 的电负性比B的大, 的电负性比B的大, 中 中 显负电性 显负电性 |
B. 的原子半径比 的原子半径比 的小,金属锂的熔点比钠的高 的小,金属锂的熔点比钠的高 |
C. 具有强氧化性,可作为火箭发射的助燃剂 具有强氧化性,可作为火箭发射的助燃剂 |
D. 的热稳定性较强,可用作燃料电池的燃料 的热稳定性较强,可用作燃料电池的燃料 |
 的工作原理如图所示。下列说法正确的是
的工作原理如图所示。下列说法正确的是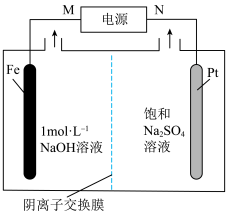
A. 为电源的负极 为电源的负极 |
B.阳极上的电极反应式为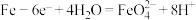 |
C.阴离子交换膜应能允许 通过而能阻止 通过而能阻止 的扩散 的扩散 |
D.理论上每转移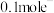 ,阴极上会产生 ,阴极上会产生 气体 气体 |
您最近一年使用:0次
名校
4 . 下列结构或性质的比较中,正确的是
A.微粒半径: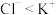 | B.电负性: |
| C.碱性:NaOH>CsOH | D.酸性:HCOOH>CH3COOH |
您最近一年使用:0次
2024-02-29更新
|
89次组卷
|
2卷引用:北京市朝阳区2023-2024学年高三上学期期末质量检测化学试试题
名校
解题方法
5 .  是原子序数依次增大的短周期主族元素,其中
是原子序数依次增大的短周期主族元素,其中 的电子只有一种自旋取向,第一电离能介于
的电子只有一种自旋取向,第一电离能介于 与
与 之间的同周期元素有4种,
之间的同周期元素有4种, 是氧化性最强的单质,
是氧化性最强的单质, 是地壳中含量第二的元素。下列说法错误的是
是地壳中含量第二的元素。下列说法错误的是
 是原子序数依次增大的短周期主族元素,其中
是原子序数依次增大的短周期主族元素,其中 的电子只有一种自旋取向,第一电离能介于
的电子只有一种自旋取向,第一电离能介于 与
与 之间的同周期元素有4种,
之间的同周期元素有4种, 是氧化性最强的单质,
是氧化性最强的单质, 是地壳中含量第二的元素。下列说法错误的是
是地壳中含量第二的元素。下列说法错误的是A.共价键极性: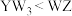 ,键能: ,键能: |
B. 在常温下与 在常温下与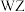 反应生成两种气体 反应生成两种气体 |
C. 的原子半径和电负性均依次减小 的原子半径和电负性均依次减小 |
D. 、 、 的单质晶体中熔点最高的为 的单质晶体中熔点最高的为 的单质 的单质 |
您最近一年使用:0次
解题方法
6 . 阅读下列材料,完成下面小题:
氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。HNO2有强氧化性;砷化镓(GaAs)是当前最重要,技术成熟度比较高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
1.下列说法不正确的是
2.下列说法正确的是
3.碳、氮及其化合物的转化具有重要应用。下列说法正确的是
氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。NaNO2是一种重要的化工原料,有毒,NaNO2也是一种食品添加剂,使用时须严格控制用量。HNO2有强氧化性;砷化镓(GaAs)是当前最重要,技术成熟度比较高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
1.下列说法不正确的是
| A. NaNO2有毒,不能作食品添加剂 |
| B.常温下N2的化学性质稳定,可用作粮食的保护气 |
| C.二氧化硅导光性好,可用作光导纤维 |
| D.硅、砷、砷化镓(GaAs)均可作半导体材料 |
| A.溶解性:CH4>NH3 |
| B.电负性:N>O>C |
| C.第一电离能:Se>As |
| D.C、N原子核外电子中未成对电子数之比为2:3 |
A.雷雨发庄稼: |
B.侯氏制碱法: |
C.实验室快速制备少量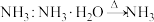 |
D.汽车尾气处理: |
您最近一年使用:0次
名校
7 . 短周期主族元素X、Y、Z、W的原子序数依次增大,基态Y原子有3个未成对电子,基态Z原子的价电子数等于其电子层数,这四种元素可形成离子化合物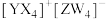 。下列叙述正确的是
。下列叙述正确的是
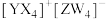 。下列叙述正确的是
。下列叙述正确的是A.氧化性: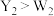 | B.电负性:Y>X>Z |
| C.Y的含氧酸一定是强酸 | D.第一电离能:Y<W |
您最近一年使用:0次
2023-12-30更新
|
489次组卷
|
2卷引用:河北省衡水市武强中学2023-2024学年高二上学期期末考试化学试题
名校
8 . 下列是某同学学习相关知识后总结的规律,其中错误的是
A.Zn、Fe、Cu单质活泼性依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
B.一定温度下,一元弱酸HA的 越小,则NaA的 越小,则NaA的 越大 越大 |
C.电解时, 、 、 、 、 放电能力依次减弱, 放电能力依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
| D.元素的电负性越大,该原子的第一电离能越大 |
您最近一年使用:0次
2024-01-22更新
|
55次组卷
|
2卷引用:河北省保定市部分重点高中2023-2024学年高三上学期12月期末化学试题
9 . 现有四种元素的基态原子的电子排布式如下:① ;②
;②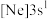 ;③
;③ ;④
;④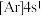 。则下列说法中正确的是
。则下列说法中正确的是
 ;②
;②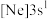 ;③
;③ ;④
;④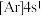 。则下列说法中正确的是
。则下列说法中正确的是| A.①和③元素均为非金属元素,并且位于同一主族 |
| B.②号元素的单质具有强氧化性 |
C.第一电离能: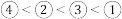 |
D.电负性: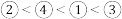 |
您最近一年使用:0次
2024-02-11更新
|
293次组卷
|
2卷引用:内蒙古呼和浩特市2023-2024学年高二上学期期末教学质量检测化学试卷
10 . 下列四种元素中,单质氧化性最强的是
| A.原子中p能级有3个电子的元素 |
| B.原子最外层电子排布为2s22p5的元素 |
| C.原子核外电子排布为[Ne]3s23p5的元素 |
| D.位于周期表中第三周期ⅢA族的元素 |
您最近一年使用:0次



